 Анаболики
Анаболики Витамины
Витамины
Инструменты пользователя
Инструменты сайта
- Life support
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Аспарагиновая кислота
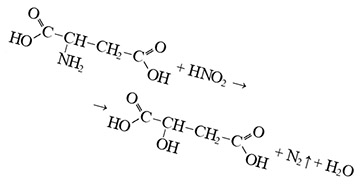 Аспарагиновая кислота (сокращенно Asp или D) - альфа-аминокислота с химической формулой HOOCCH (NH2) CH2COOH. Карбоксилат-анион, соль или сложный эфир аспарагиновой кислоты, известен как аспартат. L-изомер аспартата является одной из 20 протеиногенных аминокислот, входящей в строительные блоки белков. Его кодоны GAU и GAC.
Аспарагиновая кислота (сокращенно Asp или D) - альфа-аминокислота с химической формулой HOOCCH (NH2) CH2COOH. Карбоксилат-анион, соль или сложный эфир аспарагиновой кислоты, известен как аспартат. L-изомер аспартата является одной из 20 протеиногенных аминокислот, входящей в строительные блоки белков. Его кодоны GAU и GAC.
Аспарагиновая кислота, наряду с глутаминовой кислотой, классифицируются как кислые аминокислоты с рКа, равной 3,9, однако в пептиде рКа очень зависит от различных условий. Не является редкостью РКа, достигающая значения 14. Аспартат довольно распространен в биосинтезе. Как и у всех аминокислот, присутствие кислотных протонов зависит от окружающей среды химического остатка и рН раствора.
Фармакологическая группа: аминокислоты
Открытие
В 1827 году Плиссон впервые обнаружил аспарагиновую кислоту в аспарагине, веществе, которое было выделено из сока спаржи в 1806 году, путем кипячения с основанием.
Формы аспаргиновой аминокислоты
Существуют две формы или энантиомера аспарагиновой кислоты. Название «аспарагиновая кислота» может относиться к любому энантиомеру, или смеси двух. Из этих двух форм только одна, «L-аспарагиновая кислота», непосредственно включается в белки. Биологическая роль его аналога, «D-аспарагиновой кислоты», более ограничена. Если в результате ферментативного синтеза мы получим либо одну, либо другую форму кислоты, в результате большинства химических синтезов мы получим обе формы, «DL-аспарагиновую кислоту», известную как рацемическая смесь.
Роль в биосинтезе аминокислот
Аспартат у млекопитающих не является незаменимой аминокислотой, и при переаминирования производится из оксалоацетата. Он также может быть получен из орнитина и цитруллина в цикле мочевины. У растений и микроорганизмов аспартат является предшественником нескольких аминокислот, в том числе четырех незаменимых для человека: метионина, треонина, изолейцина и лизина. Превращение аспартата в эти другие аминокислоты начинается с превращение аспартата в его «полуальдегид» O2CCH (NH2) CH2CHO. Аспарагин производится от аспартата через трансамидирование:
-O2CCH (NH2) CH2CO2-+ GC (O) NH 3 + O2CCH (NH2) CH2CONH3 + + GC (O)
(Где GC (O) NH2 и GC (O) OH являются соответственно глутамином и глутаминовой кислотой)
Другие биохимические роли
Аспартат также является метаболитом в цикле мочевины и участвует в глюконеогенезе. Он несет восстановительные эквиваленты в малат-аспартатном челночном механизме, который использует готовое взаимопревращение аспартата и оксалоацетата, окисленного (дегидрированного) производного яблочной кислоты. Аспартат жертвует один атом азота в биосинтез инозина, предшественника пуриновых оснований. Кроме того, аспарагиновая кислота действует как акцептор водорода в цепи АТФ-синтазы.
Аспартат как медиатор нейрорецепторов
Аспартат (сопряженное основание аспарагиновой кислоты) стимулирует рецептор nmda, хотя и не так сильно, как нейромедиатор аминокислота Глутамат.
Пищевые источники аспарагиновой кислоты
Аспарагиновая кислота не является незаменимой аминокислотой, то есть она может быть синтезирована из центральных промежуточных продуктов метаболизма человека. Аспарагиновая кислота содержится в:
Животные источники: мясо, колбаса, дичь
Растительные источники: проростки семян, овсяные хлопья, авокадо, спаржа, молодой сахарный тростник и патока сахарной свеклы.
Пищевые добавки, такие как аспарагиновая кислота сама по себе или соли (такие как аспартат магния)
Подсластитель аспартам (NutraSweet, Equal, Canderel и т.д.)
Химический синтез аспарагиновой кислоты
Рацемическая аспарагиновая кислота может быть синтезирована из диэтилового фталимидомалоната натрия, (C6H4 (CO) 2 NC (CO 2 Et) 2).
Основным недостатком вышеуказанного метода является то, что, хотя производятся эквимолярные количества каждого энантиомера, организм использует только L-аминокислоты. С помощью биотехнологий, теперь можно использовать иммобилизованные ферменты для создания только однотипных энантиомеров вследствие их стереоспецифичности. Аспарагиновая кислота синтетически производится с использованием фумарата аммония и аспартазы из E.coli. E.coli обычно перерабатывают аспарагиновую кислоту в качестве источника азота, но при избыточных количествах фумарата аммония возможно изменение в работе фермента, и таким образом, аспарагиновая кислота будет производиться в очень больших количествах, 98,7 мм от 1 M.
Доступность:
Аспарагиновая кислота – это заменимая аминокислота, основными функциями которой являются поддержание здоровья нервной системы, регуляция эндокринной системы и помощь в выработке тестостерона, пролактина и гормона роста.
:Tags
Читать еще: Аутизм , Бетаметазон (бетаметазона дипропионат) , Вакцина против ветряной оспы , Гамма-оксимасляная кислота (ГОМК) , Форместан ,
Понравилась статья? Поделитесь ей в соцсетях:
Инструменты страницы
Боковая панель
Подпишитесь на новости
Если вы желаете быть в курсе новых материалов, которые публикуются на нашем сайте, подпишитесь на рассылку!
