Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Бромантан (Ладастен)

Бромантан (торговая марка Ladasten, также известен в России как адамантилбромидфениламин) 1) – это атипичный психостимулятор и анксиолитический препарат семейства адамантанов, который используется в России при лечении неврастении. Хотя было установлено, что эффекты бромантана зависят от дофаминергических и, возможно, серотонинергических нейротрансмиттерных систем, точный механизм его действия неизвестен и отличается по своим свойствам от типичных психостимуляторов, таких как амфетамин. Из-за своих уникальных свойств, бромантан иногда описывается как адаптоген и актопротектор. 2)
- Применение: перорально (таблетки)
- Легальное положение: США: не входит в списки, не одобрен FDA. Россия: отпускается только по рецепту
- Биодоступность: 42%
- Биологический период полувыведения: 11,21 часа (у людей)
- 7 часов (у крыс)
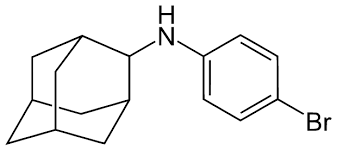
- Формула: C16H20BrN
- Молярная масса: 306,246 г / моль
История
В 1960-х годах было разработано адамантановое производное амантадина (1-аминоадамантан) в качестве противовирусного препарата для лечения гриппа. 3) Затем были изобретены другие адамантановые противовирусные препараты, такие как римантадин (1- (1-аминоэтил) адамантан) и адероман (1- (1-аминопропил) адамантан). В 1969 году было неожиданно обнаружено, что амантадин обладает центральными допаминергическими психостимулятороподобными свойствами 4), и последующее исследование показало, что такими же свойствами обладают также римантадин и адеромин. Затем Амантадин был разработан и внедрен для лечения болезни Паркинсона в связи с его способностью повышать уровень дофамина в мозге. Он также используется с тех пор, чтобы помочь облегчить усталость при рассеянном склерозе. 5) С учетом допаминергического психостимуляторного действия производных адамантана, в 1980-х годах в Государственном институте фармакологии им. Закусова РАМН в Москве был разработан бромантан, который представляет собой 1-амино-2-бромфениладамантан, «лекарственное средство, обладающее психоактивными и адаптогенными свойствами (гипоксия, высокая температура, физическое переутомление, эмоциональный стресс и т.д.)». Было обнаружено, что он вызывает более выраженные и длительные психостимуляторные эффекты, чем другие адамантаны. Этот препарат особенно широко был известен среди солдат советских и российских вооруженных сил, которые использовали его, чтобы «сократить время восстановления после сильных физических нагрузок». После распада Советского Союза в 1991 году, бромантан продолжал исследоваться, но его использование, в основном, ограничивалось спортивной медициной (например, для повышения спортивных результатов). В 1996 году препарат был замечен в качестве допингового вещества на летних Олимпийских играх 1996 года, когда тесты показали его употребление несколькими российскими спортсменами, и в 1997 году он был включен в список Всемирного антидопингового агентства в качестве стимулятора и маскирующего агента.6) Бромантан, в конечном счете, стал использоваться в 2005 году как средство для лечения неврастении. Была продемонстрирована эффективность и безопасность этого препарата для лечения этого состояния в обширных, в том числе, крупномасштабных клинических испытаниях, и он был утвержден для этого показания в России примерно в 2009 году.
Клинические исследования
Терапевтический эффект бромантана при астении начинается в течение 1-3 дней 7). Было высказано предположение, что комбинация психостимуляторной и анксиолитической активности может придать особую эффективность бромантану в лечении астении. В крупномасштабном многоцентровом клиническом исследовании 728 пациентов с диагнозом астения, бромантан назначали в течение 28 дней в суточной дозе 50 мг или 100 мг. Эффективность составила 76,0% и 90,8% на общих шкалах клинической эффективности, что свидетельствует о широком применении и высокой эффективности препарата. Терапевтическая польза при астении наблюдалась еще через один месяц после прекращения приема препарата, что указывает на длительные положительные эффекты бромантана. Качество жизни пациентов значительно увеличилось, и это увеличение продолжалось на продолжении одного месяца после прекращения приема бромантана. 3% пациентов испытали побочные эффекты; ни один из побочных эффектов не был серьезным; и 0,8% пациентов прекратили лечение из-за побочных эффектов. Было также отмечено, что бромантан нормализует цикл сон-бодрствование. Авторы пришли к выводу, что «бромантан в суточной дозе от 50 до 100 мг является высокоэффективным, хорошо переносимым и безопасным препаратом с широким спектром клинических эффектов. Таким образом, этот препарат можно рекомендовать для лечения астенических расстройств в неврологической практике».
Эффекты / преимущества
 Бромантан, прежде всего, считается мягким психостимулятором 8) и анксиолитиком. Кроме того, он обладает антиастеническими свойствами. Сообщается, что бромантан повышает физическую и умственную работоспособность и, следовательно, может считаться стимулирующим препаратом. Было обнаружено, что бромантан снижает уровни провоспалительных цитокинов IL-6, IL -17 и IL-4 и нормализует поведение в моделях депрессии у животных и может обладать клинической эффективностью в качестве антидепрессанта. 9) Было также установлено, что у крыс обоих полов повышается сексуальная восприимчивость и процептивность (поведение самки, стимулирующее сексуальную активность самца), что было обусловлено его дофаминергическими свойствами 10). Было предложено, что бромантан способен подавлять уровни пролактина также благодаря его дофаминергическим свойствам. Было обнаружено, что бромантан выступает в роли агониста стереотипии, вызванной амфетамином in vivo. Предположительно, вещество может потенцировать некоторые эффекты других психостимуляторов.
Бромантан, прежде всего, считается мягким психостимулятором 8) и анксиолитиком. Кроме того, он обладает антиастеническими свойствами. Сообщается, что бромантан повышает физическую и умственную работоспособность и, следовательно, может считаться стимулирующим препаратом. Было обнаружено, что бромантан снижает уровни провоспалительных цитокинов IL-6, IL -17 и IL-4 и нормализует поведение в моделях депрессии у животных и может обладать клинической эффективностью в качестве антидепрессанта. 9) Было также установлено, что у крыс обоих полов повышается сексуальная восприимчивость и процептивность (поведение самки, стимулирующее сексуальную активность самца), что было обусловлено его дофаминергическими свойствами 10). Было предложено, что бромантан способен подавлять уровни пролактина также благодаря его дофаминергическим свойствам. Было обнаружено, что бромантан выступает в роли агониста стереотипии, вызванной амфетамином in vivo. Предположительно, вещество может потенцировать некоторые эффекты других психостимуляторов.
Фармакология
Повышение синтеза дофамина
Хотя препарат часто маркируется как психостимулятор, бромантан отличается своей фармакологией и эффектами от типичных психостимуляторов, таких как фенэтиламины (например, амфетамин и его производные) и их структурные аналоги (например, метилфенидат, кокаин, мезокарб и др.). 11) В то время как последние непосредственно воздействуют на транспортер дофамина для ингибирования обратного захвата и / или индуцирования высвобождения дофамина, бромантан действует через косвенные геномные механизмы, производя быструю, выраженную и продолжительную повышенную регуляцию в различных областях экспрессии тирозингидроксилазы (ТГ) в мозгу и ароматической декарбоксилазы L-аминокислот (AAAD) (также известной как ДОФА-декарбоксилаза), ключевые ферменты в пути биосинтеза дофамина. Например, однократная доза бромантана приводит к увеличению экспрессии ТГ в гипоталамусе крысы в 2-2,5 раза от 1,5 до 2-х часов после введения 12). Биосинтез и высвобождение дофамина впоследствии усиливаются в тесной корреляции с повышением уровня ТГ и AAAD. Усиление дофаминергической нейротрансмиссии наблюдается в гипоталамусе, стриатуме, вентральной тегментальной области, прилежащем ядре и других областях. Таким образом, ключевым механизмом фармакологической активности и психостимуляторных эффектов бромантана является активация синтеза допамина de novo посредством модуляции генной экспрессии. Напротив, типичные психостимуляторы не влияют на экспрессию ТГ или AAAD и, таким образом, не оказывают влияния на биосинтез дофамина. В ряде выдержек из медицинской литературы подробно описаны различия между бромантаном и типичными психостимуляторами: «Бромантан не имеет психостимуляторной структуры фенилалкиламина и его аналогов (амфетамин, мезокарб, метилфенидат и т. д.) и не демонстрирует их специфической активности. Напротив, бромантан не обладает аддиктивным потенциалом и не обнаруживает излишнюю и истощающую активацию симпатикоадренергической системы и не замедляет восстановление работоспособности при профилактическом применении перед предстоящей активностью в сложных условиях (гипоксия, высокая температура окружающей среды, физическая переутомляемость, эмоциональный стресс и т.д.). Бромантан не обладает прогипоксической активностью. «Применение препарата, в отличие от типичных психостимуляторов, не связано с явлением гиперстимуляции и не вызывает никаких последствий, таких как функциональное истощение организма». «Применение бромантана в терапевтических целях характеризуется почти полным отсутствием побочных эффектов, включая проявления синдрома отмены и гиперстимуляции». «Бромантан обладает низкими периферическими симпатомиметическими эффектами. Кроме того, не было обнаружено признаков зависимости от бромантана и абстинентного синдрома». Таким образом, у бромантана практически нет побочных эффектов (включая периферические симпатомиметические эффекты и гиперстимуляцию), не вызывает толерантности или зависимости, не проявляет симптомов отмены при прекращении использования и демонстрирует отсутствие аддиктивного потенциала. Как и в исследованиях на людях, животные, подвергающиеся воздействию бромантана в течение длительных периодов времени, как представляется, не проявляют толерантности или зависимости. 13) Точный прямой молекулярный механизм действия, с помощью которого бромантан усиливает синтез дофамина, неизвестен. Однако, было установлено, что активация определенных цАМФ-, Ca2 + - и фосфолипидзависимых протеинкиназ, таких как протеинкиназа А и особенно протеинкиназа С, соответствует проявлению фармакологического действия бромантана. [25] [31] Таким образом, кажется, что бромантан активирует внутриклеточные сигнальные каскады с помощью определенного механизма (например, агонизируя некоторые пока еще неопределенные рецепторы), в свою очередь, активируя протеинкиназы, которые, в свою очередь, вызывают повышенную транскрипцию ТГ и AAAD 14). В 2004 году было обнаружено, что амантадин и мемантин связываются с агонистами σ1-рецептора (Ki = 7,44 мкМ и 2,60 мкМ соответственно), и что активация σ1-рецептора участвует в центральных дофаминергических эффектах амантадина в терапевтически значимых концентрациях. Эти результаты могут также распространяться на другие адамантаны, такие как апромивин, римантадин и бромантан, и могут объяснять психостимулирующие эффекты этого семейства соединений, возможно, включая соединения бромантана.
Подавление обратного захвата моноаминов
Ранее считалось, что бромантан действует как ингибитор обратного захвата серотонина и дофамина. 15) Действительно, бромантан ингибирует обратный захват серотонина, дофамина и, в меньшей степени, норадреналина in vitro в мозговой ткани крысы. Однако, концентрации, необходимые для этого, чрезвычайно высоки (50-500 мкМ) и, вероятно, не имеют клинической значимости. (Хотя одно исследование показало, что IC50 для транспорта дофамина составляет 3,56 мкМ, относительно 28,66 нМ для мезокарба, в противоположность этому ни один препарат не влияет на транспорт серотонина при тестируемых концентрациях). В любом случае, отсутствие типичных психостимулянтных эффектов, и побочные эффекты, наблюдаемые при приеме бромантана, подтверждают, что препарат действует не как ингибитор обратного захвата моноаминов, а через усиление синтеза дофамина.
Различные действия
Установлено, что бромантан увеличивает экспрессию нейротрофинов, включая нейротрофический фактор мозга и фактор роста нервов в определенных областях мозга крыс. Было обнаружено, что бромантан оказывает антихолинергическое действие, в том числе, антимускариновое и антиникотиновое действие при очень высоких дозах у животных, хотя это и не актуально для обычных клинических доз, и эти эффекты отвечают за токсичность препарата (то есть, LD50) у животных. 16)
Фармакокинетика
Начало действия психостимуляторных эффектов бромантана происходит постепенно, в течение 1,5-2 часов, и действие длится от 8 до 12 часов. Бромантан используется клинически в дозах от 50 мг до 100 мг в день при лечении астении. Основным метаболитом бромантана является 6β-гидроксибромантан.
Исследования бромантана
Исследование теплозащитных эффектов бромантана при различных уровнях перегрева
Были изучены термозащитные свойства бромантана во время перегрева. 1). Одновременно с известными эффектами на теплообмен и чувствительность к высоким температурам, бромантан вызывал уменьшение диапазонов тепловой толерантности, увеличивал скорость роста SVTK, а также изменял белковый обмен и антиоксидантную защиту, а также влиял на вегетативную регуляцию теплообмена, что было существенно при адаптации. В то же время, при эрготермической нагрузке, сопровождающейся какими-либо проблемами в испарении и теплообмене, сравнивалась эффективность термозащиты бромантана по его способности улучшать мышечную динамометрию и гемодинамику по сравнению с контрольными значениями.
Влияние бромантана на сексуальное поведение у крыс
Результаты экспериментов на крысах показали, что психотропный препарат бромантан влияет на сексуальное поведение и спаривание 2). Трехдневное применение бромантана (30 и 300 мг / кг перорально) преимущественно увеличивало половую восприимчивость, тогда как длительное введение (в течение 2 месяцев у самцов и 2 недель у самок) приводило к дозозависимому увеличению как процептивности, так и восприимчивости. Наблюдаемые эффекты, вероятно, связаны с дофамин-положительным действием бромантана.
Токсическое действие однократного применения бромантана на неврологический статус подопытных животных
Нейротоксикологический профиль актопротекторного средства бромантана изучался на крысах с использованием протокола мультисервисного наблюдения С. Ирвина 3). Препарат в дозах 30-300 мг / кг стимулировал, а в дозах 600-9600 мг / кг подавлял поведенческую активность. Спонтанная двигательная активность повышалась после однократной дозы бромантана 30-300 мг / кг, не изменялась после дозы 600 мг / кг и ингибировалась после доз выше 600 мг / кг. В дозах 300-600 мг / кг препарат уменьшал порог болевой чувствительности и в дозах выше 600 мг / кг повышал порог болевой чувствительности и тактильную чувствительность, а также реакцию на стук. Бромантан вызывал мидриаз во всех исследуемых дозах; в дозах выше 10 г / кг препарат вызывал блефароптоз. При дозах выше 5 г / кг бромантан незначительно увеличивает частоту и глубину дыхания (кусмауловидное дыхание). У некоторых животных, бромантан в высоких дозах вызывал регургитацию, диарею и полиурию. Ректальная температура снижалась на 0,5-1 градуса C после применения практически всех доз препарата. Поведенческие эффекты бромантана в дозах 30 и 600 мг / кг были связаны со стимуляцией центрального допамина и подавлением мускариновых и никотиновых холинергических структур, n-холинолитические эффекты бромантана были более выраженными при дозе 30 мг / кг, чем при дозе 600 мг / кг.
Влияние бромантана на неврологический статус крысы при двухмесячном курсе
При пероральном введении бромантана в течение двух месяцев на уровне токсической дозы у крыс наблюдалось зависимое от пола психодиплептическое действие 4): эффективная (30 мг / кг), промежуточная (150 мг / кг) и токсичная (600 мг / кг) дозы снижали двигательную активность у самцов, не затрагивая (или увеличивая) эту активность у самок. Эффективная доза стимулировала, а токсическая доза подавляла активность и увеличивала количество эпизодов ухаживания, что неоднозначно влияло на эмоциональное состояние крыс. На начальном этапе лечения, бромантан вызывает гипотермию; во втором месяце этот эффект заменялся незначительной гипертермией. Длительное применение большой дозы бромантана подавляло потребление пищи и слегка увеличивало потребление напитков. При лечении бромантаном, масса тела увеличилась у женщин и уменьшилась у мужчин. Курс лечения бромантаном увеличил мышечную силу крыс; оперантная активность была оптимизирована в течение первого месяца курса. Общие физиологические и поведенческие характеристики животных восстанавливались в течение двух месяцев после окончания курса лечения. В течение этого периода, у подопытных животных не наблюдалось существенных поведенческих симптомов, указывающих на развитие зависимости. Двухмесячный курс лечения не привел к развитию толерантности в отношении оптимизирующего действия препарата на физическую и оперантную способность.
Влияние бромантана на созревание потомства и развитие рефлексов
Бромантан (N- [2-адамантил] -N- [пара-бромфенил] амин) является «актопротекторным» лекарственным средством, широко используемым в России в качестве повышающего мышечную эффективность препарата для спортсменов и в качестве иммуностимулятора в медицине 5). Проводились эксперименты, чтобы определить, оказывает ли это соединение отрицательные эффекты на размножение и развитие потомства. Половозрелым самкам крыс весом 180-200 г, перорально вводили бромантан в дозах 30 мг / кг (группа 30 мг / кг), 150 мг / кг (группа 150 мг / кг) и 600 мг / кг (600 мг / кг) ежедневно в течение 16 дней, в то время как контрольные животные получали амиловый раствор. Впоследствии обработанных самок соединяли с необработанными самцами. Наблюдали изменение массы тела беременных крыс, а также продолжительность беременности, размер помета, соотношение полов и количество мертворожденных. Потомство взвешивали и наблюдались относительно внешних пороков развития, аномалий условных и безусловных рефлексов и поведения в камере «открытое поле». Наблюдение за самками крыс показало, что их общее состояние и активность во всех группах достоверно не различались как во время, так и после лечения бромантаном. Бромантан не оказывает неблагоприятного воздействия на массу тела и продолжительность беременности самок. Количество самок в группе не отличалось от контрольной группы. Во всех пометах были мертворожденные детеныши, но в контрольной группе их было меньше. Одна самка в первой группе родила детеныша с гематомой головы. Размер помета в группах 30 и 600 мг / кг был уменьшен (на 34,9 и 44,2% соответственно) и увеличился в группе 150 мг / кг (на 45,1%, Р <0,05) по сравнению с контрольной группой. Бромантан оказывал незначительное влияние на соотношение полов новорожденных во всех группах. Выживаемость потомства в течение первых 3 месяцев показала потерю 40% для группы 150 мг / кг и 20% для контрольной группы. В оставшееся время, смертность не превышала 3-6% и не отличалась от смертности в контроле. Крысята в группах 30 и 600 мг / кг показали значительно более высокий прирост массы тела в течение первой недели наблюдения на 83,69% и 58,02%, соответственно, по сравнению с контрольной группой; впоследствии эта разница в группе 600 мг / кг быстро уменьшилась до незначительных уровней, но группа 30 мг / кг все еще значительно отличалась до 35 послеродового дня, а затем снова на 77-112 послеродовой день. Динамика увеличения массы тела у крысят в группе 150 мг / кг в течение всего периода наблюдения (но не на 7 послеродовой день) была незначительной (при 14, 42 и 49-й послеродовой день) значительно ниже, чем у контрольной группы. Изучение функционального состояния нервной системы крысят на разных стадиях постнатального развития выявило незначительные различия в выраженности рефлексов по сравнению с контрольной группой. Отрицательный геотаксис был завершен к 8-му дню в контрольной группе и в группах лечения ранее в среднем на 1-2 дня. Установочный осязательный рефлекс наблюдался у контрольной группы на 8-й день, в группе 30 мг / кг на 6-й день и в других обработанных группах на 7-й день. Положительный результат теста уклонения от скалы наблюдалось на сутки быстрее у крысят в обработанных группах по сравнению с контрольными. Лабиринтный установочный рефлекс в группах 30 и 600 мг / кг наблюдался на день раньше, чем в контрольной группе. Значительные различия наблюдались только для двух параметров (отрицательный геотаксис и восстановление поверхности); в обоих случаях крысиные щенки группы 30 мг / кг отличались от контрольных и 150 мг / кг групп. Было также отмечено раннее развитие физических параметров, но существенные отличия от контрольной группы были получены только в группе 30 мг / кг относительно роста резцов. Хотя все крысята демонстрировали силу передних и задних конечностей на 16 постнатальный день, обработанные щенки увеличивали время поддержания сжатия конечностей (15 день после рождения). Открытые испытания (на 40й день после рождения) привели к незначительному снижению исследовательского и локомоторного поведения для групп 30, 150 и 600 мг / кг. Число эпизодов ухода было незначительно уменьшено для группы 30 мг / кг и незначительно увеличилось для группы 600 мг / кг. При тестировании пассивного избегания, в день удержания (72 часа спустя), латентность входа для щенков крыс в группах 30, 150 и 600 мг / кг увеличилась на 259,0%, 175,3% и 160,7% соответственно (P < 0.05), в течение дня, тогда как в контрольной группе время увеличилось только на 1,8%.
Влияние бромантана на сердечно-сосудистую и симпато-надпочечниковую системы у животных
 Введение бромантана заметно увеличивает ударный объём и минутный объём крови при сниженной частоте сердечных сокращений и периферическом сопротивлении у анестезированных крыс, в то время как системное артериальное давление проявляет незначительное кратковременное увеличение. Бромантан также слабо увеличивает прессорные эффекты адреналина и норадреналина. У анестезированных кошек, бромантан изменяет форму амплитудно-частотной характеристики ЭЭГ, измеряемой в верхнем шейном ганглии, уменьшая (против начального уровня) индуцированный потенциал в частотном диапазоне стимуляции преганглионарного волокна (1-10 и 25-30 Гц). У свободно перемещающихся крыс, способных к хорошо выученной оперантной активности Сидмэна (коррекция состояния Седмена), бромантан показал тенденцию к снижению скорости выделения норадреналина и адреналина с мочой.
Введение бромантана заметно увеличивает ударный объём и минутный объём крови при сниженной частоте сердечных сокращений и периферическом сопротивлении у анестезированных крыс, в то время как системное артериальное давление проявляет незначительное кратковременное увеличение. Бромантан также слабо увеличивает прессорные эффекты адреналина и норадреналина. У анестезированных кошек, бромантан изменяет форму амплитудно-частотной характеристики ЭЭГ, измеряемой в верхнем шейном ганглии, уменьшая (против начального уровня) индуцированный потенциал в частотном диапазоне стимуляции преганглионарного волокна (1-10 и 25-30 Гц). У свободно перемещающихся крыс, способных к хорошо выученной оперантной активности Сидмэна (коррекция состояния Седмена), бромантан показал тенденцию к снижению скорости выделения норадреналина и адреналина с мочой.
Нейро- и психофизиологические эффекты бромантана
Изучение ЭЭГ и психофизиологических параметров и их корреляции у 10 здоровых добровольцев после однократного перорального приема бромантана по сравнению с плацебо 6) выявило благоприятное влияние препарата на функциональное состояние испытуемых. По ЭЭГ-профилю (увеличение мощности альфа-ритма средней частоты при понижении мощности в дельта- и бета-полосах), бромантан похож на многие препараты с умеренными психостимулирующими, антиамнестическими и антигипоксическими свойствами. Бромантан не изменяет субъективное состояние и основные компоненты работы у неиспытуемых мужчин, но способствует появлению ЭЭГ-признаков умеренного повышения бдительности и формирования состояния продуктивного действия в сочетании с благоприятными условиями для точного снижения дрожания двигательной активности. Оптимизация функционального состояния приводит к расширению резервных возможностей и, вероятно, говорит об эффективности бромантана как хорошо известного средства для поддержания высокой работоспособности у уставших людей и в экстремальных условиях.










