Содержание
Олеоилэтаноламид
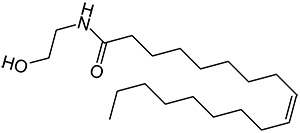 Олеоилэтаноламид(ОЭА) представляет собой молекулу, вырабатываемую в организме, обычно в кишечнике, отвечающую за чувство сытости после еды. Необходимы дальнейшие исследования, чтобы определить, обеспечивает ли пероральный прием ОЭА преимущества для потери веса.
Олеоилэтаноламид(ОЭА) представляет собой молекулу, вырабатываемую в организме, обычно в кишечнике, отвечающую за чувство сытости после еды. Необходимы дальнейшие исследования, чтобы определить, обеспечивает ли пероральный прием ОЭА преимущества для потери веса.
Резюме
Олеоилэтаноламид(ОЭА) представляет собой молекулу, вырабатываемую в организме, обычно находящуюся в кишечнике. Он отвечает за чувство сытости после еды. ОЭА иногда включают в состав жиросжигающих добавок. В настоящее время нет доказательств того, что пероральный прием ОЭА у человека способствует жиросжиганию. ОЭА действует на рецептор под названием альфа-рецептор, активируемый пролифераторомпероксисом (PPAR). При активации этого рецептора в кишечнике крыс, животные потребляют меньше пищи. Исследования на крысах показывают, что и инъекции, и пероральный прием ОЭА вызывают значительное снижение количества съеденной пищи. Ограниченные данные на людях свидетельствуют о том, что ОЭА может способствовать жиросжиганию путем воздействия на PPAR. При активации этого рецептора в жировой ткани, увеличивается расход энергии. Необходимо провести дальнейшие исследования ОЭА, прежде чем рекомендовать его для потери веса. Также известен как
- ОЭА, NOPE (предшественник)
Является
- Жиросжигателем
- Ноотропом
Сочетается с
- Тетрадецилтиоуксусной кислотой
ОЭА: инструкция по применению
Исследования на крысах показали, что эффекты наблюдаются при суточной дозе 10 мг/кг веса тела. Это примерно эквивалентно следующим дозировкам у человека:
- 100мг для человека весом 68 кг
- 145 мг для человека весом 90 кг
- 180 мг для человека весом 113 кг
Источники и структура
Источники
Олеоилэтаноламид (ОЭА) является эндогенным регулятором аппетита, который подавляет потребление пищи. 1) Он входит в класс молекул, известных как ацилетаноламиды, которые являются молекулами этаноламида, основанными на жирных кислотах и, как правило, связанными с производным арахидоновой кислоты и каннабиноида, известного как анандамид. Кроме того, в эту категорию молекул входит эндогенный регулятор снаолеамид, который структурно подобен анандамиду и ОЭА.
Биологическое значение
ОЭА считается эндогенным регулятором сытости. Базальные концентрации ОЭА в кишечнике (где он первоначально действует) без дополнительного приема добавок находятся в диапазоне от 300 нм в дневное время у крыс, когда они сыты, и эта концентрация является достаточной для того, чтобы полностью насытить рецептор, на который воздействует вещество (PPAR). 2) В ночное время, когда крысы обычно увеличивают потребление пищи, концентрация ОЭА падает до уровней, которые больше не насыщают рецептор. ОЭА синтезируется в естественных условиях из жирных кислот из клеточных мембран, и высвобождается во время приема пищи. ОЭА, по-видимому, присутствует в желудочно-кишечном тракте, и его концентрация в ткани, как представляется, связана с уровнем сытости у крыс. Его секреция увеличивается, когда пища попадает в организм, что указывает на связь между ОЭА и чувством сытости. ОЭА может быть синтезирован в нейронах крыс. ОЭА выводится из организма путем ферментативного гидролиза по аналогии с большинством ацилетаноламидов, когда ферменты, известные как амидазы, расщепляют ОЭА в компонент жирных кислот (в случае ОЭА, олеиновую кислоту), который затем может быть использован в производстве фосфолипидов, и этаноламин, который может использоваться в производстве фосфатидилэтаноламина. 3)
Лекарственные формы и варианты
N-ацил-фосфатидилэтаноламин (NAPE) представляет собой молекулу фосфатидилэтаноламина с трем стандартными глицериновыми участками связывания, содержащими жирные кислоты с аминогруппой,которая позже ацилируется другой жирной кислотой; если эта жирная кислота представляет собой олеиновую кислоту, получаемая в результате молекула представляет собой N-олеоил-фосфатидилэтаноламин (NOPE). NOPE является естественным компонентом соевого лецитина, а когда любая молекула NAPE расщепляется ферментом N-ацил-фосфатидилэтаноламинфосфолипазы D (NAPE-PLD),высвобождается липид, связанный с амином. В случае NOPE, высвобождаемый липид является олеоилэтаноламидом (ОЭА). NOPE может произведен эндогенно, когда фосфатидилхолин (ФХ) жертвует молекулу олеиновой кислоты из положения sn-1 к аминогруппе фосфатидилэтаноламина (ФЭ), создавая NOPE. Когда это происходит, стандартный обмен веществ с помощью NAPE-PLD может вновь производить ОЭА.
Молекулярные цели
PPARs
Олеоилэтаноламид (ОЭА), как известно, является агонистом PPAR, что обусловливает его подавляющие аппетит эффекты, так как эти эффекты не наблюдаются у мышей, не имеющих этого рецептора. Снижение потребления пищи может быть вызвано синтетическими агонистами PPAR. Это снижение потребления пищи, как представляется, связано с увеличением времени между кормлениями, а не с уменьшением потребления пищи у свободно питающихся крыс в зависимости от их модели питания. Однако у крыс,которых лишили пищи, ОЭА уменьшает потребление пищи за один прием пищи, а также увеличивает время между приемами пищи. 4) ОЭА активирует PPARα со значением ЕС50 120 нм, тогда как его действия на PPARβ/δ значительно слабее (1100 нМ или 1.1 мкм) и активность на PPARγ не была обнаружена до концентрации 50 мкм, что указывает на относительную селективность по отношению к PPARα. Эта активность на PPARα также значительно выше, чем у аналогично структурированных жирных кислот, таких как олеиновая кислота (ЕС50 10.3 мкм) и другие тестируемые ацилэтанламиды, такие как анандамид, который не показал никакого существенного эффекта.
GPRs
Рецептор, связанный с G-белком (GPR), известный как GPR119, вплоть до недавнего времени считался рецептором-сиротой (то есть, рецептором, не имеющим известного эндогенного лиганда); тем не менее, было установлено, что ОЭА является эндогенным агонистом GPR119 5) с EC50 около 2.3 мкм. Рецептор-сирота GPR55 также связывает ОЭА с EC50 около 4нм, и связан с функционированием периферических каннабиноидных рецепторов (не связанных с психогенной активностью каннабиноидов). 6) Эти рецепторы также присутствуют в кишечнике, где они играют роль в секреции кишечного гормона глюкагоноподобного пептида-1 (GLP-1) и в подавлении аппетита через рецептор GPR119, а также в регулировании перистальтики кишечника (что не связано с активностью PPAR). С ОЭА взаимодействуют два GPR рецептора, GPR55 и GPR 119, что может объяснить некоторые из его эффектов в организме.
Фармакология
Абсорбция
Олеоилэтаноламид (ОЭА) имеет плохую доступность, так как фермент, который разрушает его, амидгидролаза жирных кислот (FAAH), присутствует в больших количествах в желудочно-кишечном тракте и печени. 7) Только 0,48% от перорально введенной дозы 10 мг / кг остается в неповрежденном виде в кишечнике в течение 90 минут после приема внутрь у крыс, однако и такое количество увеличивает базальную концентрацию в ткани кишечника (0.354нм / г) в 11 раз до 3.91+ /-0.98нм/г. Такая доза была столь же эффективна в подавлении приема пищи, как и доза 5 мг / кг в виде периферических инъекций. Сочетание перорального олеата и этаноламина отдельно не повторяет эффект ОЭА даже при введении в той же пероральной дозе. Предполагается, что метаболиты ОЭА не влияют на кормление в этой концентрации (олеат сам по себе может подавлять аппетит, но требуется значительно более высокая его концентрация в кишечнике 8)). ОАЭ при пероральном приеме широко метаболизируется в кишечнике, но, несмотря на этот практически полный метаболизм, перорально принимаемый ОЭА по-прежнему эффективен в модификации потребления пищи у крыс.
Воздействие на организм
Неврология
Адренергическая нейротрансмиссия
Периферийные инъекции олеоилэтаноламида (ОЭА) крысам в дозе 5-20 мг / кг вызывали увеличение концентраций норадреналина в гипоталамусе на 13-26% в течение одного часа в зависимости от дозы.
Серотонинергическая нейротрансмиссия
Несмотря на увеличение концентраций норадреналина и дофамина, периферические инъекции ОЭА в дозе 5-20 мг / кг у крыс не вызвали изменения концентрации серотонина или его метаболита (5-HIAA) в гипоталамусе.
Дофаминергическая нейротрансмиссия
Инъекции ОЭА в дозе 5-20 мг / кг у крыс вызывали увеличение гипоталамических концентраций допамина в зависимости от дозы на 116-140%, тогда как концентрации основного метаболита дофамина (ДОРАС) были неизменными по истечении часа. Инъекции ОЭА непосредственно в мозг крыс также повышали уровни допамина в прилежащем ядре.
Разные механизмы
Окситоцин – это гормон, участвующий в разнообразных процессах в организме, в том числе в подавлении аппетита и действующий против ожирения 9). Что является нетипичным для гормонов, окситоцин, по-видимому, способен индуцировать свой собственный синтез и высвобождение. 10) ОЭА вызывает увеличение уровня окситоцина в мозге в зависимости от активации PPAR, и сам окситоцин стимулирует выработку ОЭА в адипоцитах (после интрацеребровентрикулярной инфузии и без стимуляции сывороточной ОЭА или метаболитов каннабиноидов), и, как представляется, также требует присутствия PPAR. Из-за положительного механизма обратной связи между ОЭА и окситоцином, оба вещества участвуют в повышении уровня друг друга. Увеличение центральных уровней окситоцина связано с возможностью транспортировки окситоцина в направлении адипоцитов и увеличением местного производства ОЭА.
Аппетит и потребление пищи
 Механизм, лежащий в основе способности ОЭА подавлять прием пищи, связан с активацией PPAR в кишечнике, поскольку мыши, лишенные PPAR, не испытывают снижения потребления пищи от ОЭА (с участием этого рецептора) и повреждение блуждающего нерва ниже диафрагмы также снижает эти эффекты (что говорит о том, что ОЭА не действует централизованно на подавление приема пищи). Тонкий кишечник, как известно, содержит большое количество рецепторов PPAR, 11) и, поскольку даже внутрибрюшинное введение ОЭА активирует PPAR в этой ткани, в то время как инъекции непосредственно в мозг не подавляют потребления пищи (несмотря на то, что, в конечном счете, воздействуют на мозг), 12) взаимодействие ОЭА с кишечными PPAR, как полагают, является начальным шагом в этом сигнальном каскаде.
Свойства ОЭА отличаются от подавляющего аппетит гормона холецистокинина (ХЦК), который не задерживает время до следующего приема пищи у свободно питающихся крыс, как это делает ОЭА. ХЦК выделяется из кишечника в ответ на еду, вызывая кратковременное чувство сытости. 13)
Олеоилэтаноламид действует в кишечнике, активируя рецептор, известный как PPAR, в конечном счете, влияя на мозг, уменьшая потребление пищи. Впрыскивание непосредственно в мозг не снижает потребление пищи, однако, влияет на мозг.
После инъекции 5 мг / кг ОЭА крысам, уровни стимулирующих аппетит пептидов NPY и AGRP не изменяются при кормлении или 24-часовом голодании по сравнению с контрольной группой, несмотря на то, что уровни обоих пептидов значительно увеличиваются в период голодания.
Концентрация анорексического (подавляющего аппетит) пептида, известного как кокаиновый и амфетаминовый регулирующий транскрипт (CART) изменяется при введении периферических инъекций ОЭА при измерении в паравентрикулярном ядре, но не в дугообразном ядре, где через два часа после инъекции ОЭА уменьшалось снижение CART, индуцированное голоданием (на 15-20%).
При рассмотрении центральных (действующих в головном мозге) пептидов, регулирующих потребление пищи, представляется, что прием ОЭА может сохранить снижение уровня пептидов, подавляющих аппетит,однако это не обязательно притупляет повышение уровня пептидов, способствующих аппетиту, во время голодания.
Те же инъекции 5 мг / кг ОЭА крысам вызывали зависящие от времени сокращения уровня пептида YY (PYY, гормон, секретируемый из кишечника), и в голодном, и в сытом состоянии.
Что касается периферических пептидов, регулирующих чувство голода, уровень PYY (аппетит-стимулирующего гормона), по-видимому, снижается при инъекциях ОЭА у крыс.
Инъекции ОЭА в дозе 5 мг / кг крысам уменьшают спонтанное потребление пищи в течение следующих четырех часов. Кратковременное подавление приема пищи у крыс, как известно, происходит при периферических инъекциях ОЭА. При сравнении сытых и голодных крыс, которым вновь дали пищу, введение ОЭА кажется более эффективным в последнем случае. В этом случае не наблюдается компенсации для этого аноректического эффекта.
Пероральный прием ОЭА (10 мг / кг) у голодных крыс за 90 минут до еды уменьшает потребление пищи на 15,5% по сравнению с контрольной группой.
Инъекции эффективны в снижении потребления пищи у крыс, и ОЭА также продемонстрировало эффективность в течение 90 минут после перорального приема у крыс.
Механизм, лежащий в основе способности ОЭА подавлять прием пищи, связан с активацией PPAR в кишечнике, поскольку мыши, лишенные PPAR, не испытывают снижения потребления пищи от ОЭА (с участием этого рецептора) и повреждение блуждающего нерва ниже диафрагмы также снижает эти эффекты (что говорит о том, что ОЭА не действует централизованно на подавление приема пищи). Тонкий кишечник, как известно, содержит большое количество рецепторов PPAR, 11) и, поскольку даже внутрибрюшинное введение ОЭА активирует PPAR в этой ткани, в то время как инъекции непосредственно в мозг не подавляют потребления пищи (несмотря на то, что, в конечном счете, воздействуют на мозг), 12) взаимодействие ОЭА с кишечными PPAR, как полагают, является начальным шагом в этом сигнальном каскаде.
Свойства ОЭА отличаются от подавляющего аппетит гормона холецистокинина (ХЦК), который не задерживает время до следующего приема пищи у свободно питающихся крыс, как это делает ОЭА. ХЦК выделяется из кишечника в ответ на еду, вызывая кратковременное чувство сытости. 13)
Олеоилэтаноламид действует в кишечнике, активируя рецептор, известный как PPAR, в конечном счете, влияя на мозг, уменьшая потребление пищи. Впрыскивание непосредственно в мозг не снижает потребление пищи, однако, влияет на мозг.
После инъекции 5 мг / кг ОЭА крысам, уровни стимулирующих аппетит пептидов NPY и AGRP не изменяются при кормлении или 24-часовом голодании по сравнению с контрольной группой, несмотря на то, что уровни обоих пептидов значительно увеличиваются в период голодания.
Концентрация анорексического (подавляющего аппетит) пептида, известного как кокаиновый и амфетаминовый регулирующий транскрипт (CART) изменяется при введении периферических инъекций ОЭА при измерении в паравентрикулярном ядре, но не в дугообразном ядре, где через два часа после инъекции ОЭА уменьшалось снижение CART, индуцированное голоданием (на 15-20%).
При рассмотрении центральных (действующих в головном мозге) пептидов, регулирующих потребление пищи, представляется, что прием ОЭА может сохранить снижение уровня пептидов, подавляющих аппетит,однако это не обязательно притупляет повышение уровня пептидов, способствующих аппетиту, во время голодания.
Те же инъекции 5 мг / кг ОЭА крысам вызывали зависящие от времени сокращения уровня пептида YY (PYY, гормон, секретируемый из кишечника), и в голодном, и в сытом состоянии.
Что касается периферических пептидов, регулирующих чувство голода, уровень PYY (аппетит-стимулирующего гормона), по-видимому, снижается при инъекциях ОЭА у крыс.
Инъекции ОЭА в дозе 5 мг / кг крысам уменьшают спонтанное потребление пищи в течение следующих четырех часов. Кратковременное подавление приема пищи у крыс, как известно, происходит при периферических инъекциях ОЭА. При сравнении сытых и голодных крыс, которым вновь дали пищу, введение ОЭА кажется более эффективным в последнем случае. В этом случае не наблюдается компенсации для этого аноректического эффекта.
Пероральный прием ОЭА (10 мг / кг) у голодных крыс за 90 минут до еды уменьшает потребление пищи на 15,5% по сравнению с контрольной группой.
Инъекции эффективны в снижении потребления пищи у крыс, и ОЭА также продемонстрировало эффективность в течение 90 минут после перорального приема у крыс.
Тревожность
Периферийные инъекции ОЭА достаточны, чтобы вызвать снижение потребления пищи, однако не изменяют уровень гормонов стресса или тревожности у крыс 14).
Депрессия
Мыши, которым давали 1,5-6 мг / кг ОЭА начиная с 7 дня 28-дневного хронического непредсказуемого мягкого стресса, показали улучшение симптомов депрессии (поведение в тесте на открытом поле и предпочтения сахарозы) до уровня, аналогичного введению 6 мг / кг флуоксетина. 15) Это сопровождалось изменением гормонального ответа на стресс и нормализацией уровней нейротрофического фактора мозга в гиппокампе и префронтальной коре.
Ожирение и жировая масса
Адипокины
Инъекции олеоилэтаноламида (ОЭА) в дозе 5 мг / кг у крыс в сытом состоянии, похоже, не оказывают существенного влияния на концентрации циркулирующего адипонектина, в то время как введение той же дозы ОЭА у голодающих крыс увеличило уровни адипонектина через два часа, но не через шесть часов. В другом исследовании было продемонстрировано увеличение уровня адипонектина при введении такой же дозы в течение шести непрерывных дней. Однако, увеличения на 11,8% уже не наблюдалось при совместном введении β3-адренергического агониста CL316243. 16) Хотя совместное применение CL316243 и ОЭА способно снижать концентрацию лептина у крыс (возможно, в связи с увеличением расхода энергии и снижением жировой массы), ни одно вещество в изоляции не влияет на лептин. Повторное введение дозы в течение шести дней, но не однократное введение ОЭА, может увеличить уровни адипонектина на 12% у крыс.
Расщепление жира
Бета-адренергические рецепторы, как известно, положительно опосредуют потерю жира в организме (мыши, лишенные этих рецепторов, испытывают ожирение 17)), и активация бета-3-адренергического рецептора стимулирует снижение потребления пищи и потерю жира у грызунов, в частности, через активацию разобщающих белков, таких как UCP1. 18) ОЭА нацелен на PPAR, и эффекты PPAR, как известно, повышаются при активации рецептора β3, что частично опосредует эффекты В3 на другие липолитические белки, такие как PGC-1альфа; и Разобщающий Белок 1 (UCP1) в бурой жировой ткани. 19) В соответствии с гипотезами, совместное введение ОЭА (5 мг / кг периферической инъекции) и бета-3 агониста имеет синергический эффект на снижение потребления пищи и на уменьшение жировой массы у крыс, связанного с увеличением расхода энергии (без влияния на двигательную активность). По крайней мере у крыс, увеличение PPAR и UCP1 (которое, предположительно, отражает увеличение расхода энергии) наблюдалось в белой и бурой жировой ткани, наряду с улучшением митохондриальных биомаркеров (Cox4i1, Cox4i2, Fgf21 и PRDM16). ОЭА, по-видимому, способно усиливать термогенное действие и митохондриальные эффекты активации рецептора бета-3-адренорецепторов у крыс в белых и коричневых жировых тканях, в той же дозе, что используется для подавления аппетита.
Вес
Одно исследование по оценке действий комплекса между NOPE (85 мг) и EGCG из катехинов зеленого чая (50 мг из 121 мг экстракта зеленого чая), принимаемого дважды в день наряду с небольшим дефицитом калорий в течение восьми недель у взрослых с избыточной массой тела показало, что прием добавки был связан с большей степенью соблюдения диеты (94% группы прошло испытание, по сравнению с 74% в группе плацебо). Лица, принимавшие комплекс NOPE-EGCG, продемонстрировали меньше симптомов переедания и симптомов депрессии и больше испытывали сытость после приема пищи, хотя в целом потеря веса во время испытания не отличалась между группами. В более позднем исследовании с использованием той же формулы с модифицированными дозами (120 мг NOPE и 105 мг EGCG) не было отмечено подобных эффектов после четырех недель, хотя после восьми недель положительные эффекты на соблюдение диеты и настроение уже не были очевидными.
Взаимодействие с гормонами
Грелин
Периферийные инъекции олеоилэтаноламида (ОЭА) крысам, лишенным пищи в течение 24 часов, не влияют на грелин в течение двух часов, однако через шесть часов наблюдалось значительное снижение этого гормона, стимулирующего аппетит, на 40-50%; ОЭА не оказал никакого влияния на концентрации грелина у откормленных крыс.
Пептид YY
Инъекции 5 мг / кг ОЭА крысам вызывают зависимые от времени сокращения уровня пептида YY (PYY, гормон, секретируемый из кишечника) и в голодном, и в сытом состоянии. Что касается периферических пептидов, регулирующих чувство голода, уровень PYY (аппетит-стимулирующего гормона), по-видимому, снижается при инъекциях ОЭА у крыс.
Периферические системы органов
Поджелудочная железа
 Олеоилэтаноламид (ОЭА) является известным эндогенным агонистом рецептора жирных кислот GPR119, и активация этого рецептора в поджелудочной железе или энтероэндокринных клетках кишечника мыши стимулирует высвобождение гормона GLP-1. 20)
Наблюдаются некоторые панкреатические защитные эффекты ОЭА в диапазоне концентраций 5-100 мкм (максимум при 60 мкм) in vitro, хотя это не имеет отношения к активации GPR119 или PPAR. Поскольку ингибирование гидролазы амидов жирных кислот (FAAH, фермент, который расщепляет ОЭА) отменяет этот защитный эффект, эти эффекты, как представляется, связаны с олеатом, который является метаболитом ОЭА.
Олеоилэтаноламид (ОЭА) является известным эндогенным агонистом рецептора жирных кислот GPR119, и активация этого рецептора в поджелудочной железе или энтероэндокринных клетках кишечника мыши стимулирует высвобождение гормона GLP-1. 20)
Наблюдаются некоторые панкреатические защитные эффекты ОЭА в диапазоне концентраций 5-100 мкм (максимум при 60 мкм) in vitro, хотя это не имеет отношения к активации GPR119 или PPAR. Поскольку ингибирование гидролазы амидов жирных кислот (FAAH, фермент, который расщепляет ОЭА) отменяет этот защитный эффект, эти эффекты, как представляется, связаны с олеатом, который является метаболитом ОЭА.
Взаимодействие с заболеваниями
Болезнь Паркинсона
В дофаминергических нейронах из черной субстанции in vitro, 0.5-15 мкм (0.16-4.8 мкг / мл) олеоилэтаноламида (ОЭА), до введения дофаминергического токсина 6-OHDA, связано с колоколообразной кривой защитных эффектов с обострением в эффективности при 1 мкм. 21) Считается, что это действие связано с рецептором PPAR, экспрессируемым в этих нейронах, поскольку было отмечено, что и другие агонисты PPAR (фибраты) проявляют защитную роль. Этот механизм действия, однако, не был непосредственно подтвержден, и антагонизм TRPV1 в качестве механизма действия ОЭА также считается возможным, так как эти рецепторы экспрессируются в одних и тех же нейронах. 22)










