Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Коллоидное серебро (наночастицы серебра)
 Наночастицы серебра представляют собой частицы размером от 1 до 100 нм. 1) Хотя их часто называют «серебром», некоторые из них состоят из большого процента оксида серебра из-за их большого отношения атомов серебра к поверхности. Многочисленные формы наночастиц могут быть построены в зависимости от конкретного применения. Обычно используются сферические наночастицы серебра, но также популярны ромбы, восьмиугольники и тонкие листы.
Чрезвычайно большая площадь поверхности наночастиц серебра позволяет координировать огромное количество лигандов. Свойства наночастиц серебра, применяемые для лечения человека, исследуются в лабораторных и животных исследованиях, оценивающих потенциальную эффективность, токсичность и затраты.
Наночастицы серебра представляют собой частицы размером от 1 до 100 нм. 1) Хотя их часто называют «серебром», некоторые из них состоят из большого процента оксида серебра из-за их большого отношения атомов серебра к поверхности. Многочисленные формы наночастиц могут быть построены в зависимости от конкретного применения. Обычно используются сферические наночастицы серебра, но также популярны ромбы, восьмиугольники и тонкие листы.
Чрезвычайно большая площадь поверхности наночастиц серебра позволяет координировать огромное количество лигандов. Свойства наночастиц серебра, применяемые для лечения человека, исследуются в лабораторных и животных исследованиях, оценивающих потенциальную эффективность, токсичность и затраты.
Синтетические методы
Жидкостная химическая обработка
Наиболее распространенные методы синтеза наночастиц относятся к категории влажной химии или к зарождению частиц в растворе. Это зарождение происходит, когда комплекс ионов серебра, обычно AgNO3 или AgClO4, восстанавливается до коллоидного серебра в присутствии восстанавливающего агента. Когда концентрация возрастает, растворенные ионы металлического серебра связываются вместе, образуя устойчивую поверхность. Поверхность энергетически невыгодна, когда кластер мал, поскольку энергия, получаемая за счет уменьшения концентрации растворенных частиц, не столь велика, как потеря энергии при создании новой поверхности. Когда кластер достигает определенного размера, известного как критический радиус, он становится энергетически выгодным и, следовательно, достаточно стабильным, чтобы продолжать расти. Это ядро затем остается в системе и растет по мере того, как атомы серебра диффундируют через раствор и прикрепляются к поверхности 2). Когда растворенная концентрация атомарного серебра достаточно уменьшается, больше невозможно сделать так, чтобы достаточное количество атомов связывалось вместе с образованием стабильного ядра. При этом пороге зарождения, новые наночастицы перестают формироваться, а оставшееся растворенное серебро поглощается диффузией в растущие наночастицы в растворе. По мере роста частиц, другие молекулы в растворе диффундируют и прикрепляются к поверхности. Этот процесс стабилизирует поверхностную энергию частицы и блокирует появление новых ионов серебра на поверхности. Прикрепление этих покрывающих / стабилизирующих агентов замедляет и, в конечном счете, останавливает рост частицы. Наиболее распространенными кэпинг-лигандами являются тринатрийцитрат и поливинилпирролидон (ПВП), но многие другие вещества также используются в различных условиях для синтеза частиц с определенными размерами, формой и свойствами поверхности. Существует множество различных методов мокрого синтеза, включая использование восстановительных сахаров, восстановление цитрата, восстановление через боргидрид натрия, реакция серебряного зеркала, полиольный процесс, рост, опосредованный семенами, и рост, опосредованный светом. [10] Каждый из этих методов или комбинация методов, связаны с различными степенями контроля над распределением по размерам, а также с распределением геометрических размещений наночастицы. 3) Эльсупике и др. обнаружили новый, очень перспективный метод мокрого химического синтеза. (2015). 4) Они разработали зеленый ультразвуковой синтез. При ультразвуковой обработке, серебряные наночастицы (AgNP) синтезируются с κ-каррагинаном в качестве естественного стабилизатора. Реакцию проводят при температуре окружающей среды и получают наночастицы серебра с кристаллической структурой кубических гранецентрированных кристаллитов без примесей. Концентрация κ-каррагинана используется для влияния на распределение частиц по размерам AgNPs 5).
Восстановление моносахаридов
Существует много способов синтезировать наночастицы серебра; один из них – через моносахариды, включая глюкозу, фруктозу, мальтозу, мальтодекстрин и т. д., но не сахарозу. Это также простой метод для восстановления ионов серебра обратно в наночастицы серебра, поскольку он обычно включает одностадийный процесс 6). Имеются методы, которые показывают, что эти восстановительные сахара являются существенными для образования наночастиц серебра. Многие исследования показали, что этот метод зеленого синтеза, в частности, с использованием экстракта Cacumen platycladi, позволил восстановить серебро. Кроме того, размер наночастицы можно регулировать в зависимости от концентрации экстракта. Исследования показывают, что более высокие концентрации коррелируют с увеличением числа наночастиц. Из-за концентрации моносахаридов, образуются меньшие наночастицы при высоких уровнях рН. Другой метод синтеза наночастиц серебра включает использование восстанавливающих сахаров с щелочным крахмалом и нитратом серебра. Редуцирующие сахара имеют свободные альдегидные и кетоновые группы, которые позволяют им окисляться в глюконат. Моносахарид должен иметь свободную кетоновую группу, потому что для того, чтобы действовать в качестве восстановителя, он сначала подвергается таутомеризации. Кроме того, если альдегиды связаны, они будут застревать в циклической форме и не смогут действовать в качестве восстановителя. Например, глюкоза имеет альдегидную функциональную группу, которая способна восстанавливать катионы серебра до атомов серебра и затем окисляться до глюконовой кислоты 7). Реакция окисления сахаров происходит в водных растворах. Каппинг-агент также отсутствует при нагревании.
Восстановление цитрата
Старым и очень распространенным методом синтеза наночастиц серебра является восстановление цитрата. Этот метод был впервые зарегистрирован М. С. Ли, который успешно произвел коллоид серебра, стабилизированный цитратом, в 1889 году. 8) Восстановление цитрата включает в себя востановление частиц серебра, обычно AgNO3 или AgClO4, до коллоидного серебра, с использованием тринатрийцитрата, Na3C6H5O7. 9) Синтез обычно проводят при повышенной температуре (~ 100 ° С), чтобы максимизировать монодисперсность (однородность по размеру и форме) частицы. В этом методе, ион цитрата традиционно действует как восстановитель, так и липидный буферный лиганд [18], что делает его полезным процессом для производства AgNP из-за его относительной легкости и короткого времени реакции. Однако, образовавшиеся частицы серебра могут иметь широкое распределение по размерам и одновременно формировать несколько различных геометрических форм. Добавление более сильных восстановителей к реакции часто используется для синтеза частиц более однородных размеров и формы.
Восстановление через боргидрид натрия
Синтез наночастиц серебра восстановлением боргидридом натрия (NaBH4) происходит по следующей реакции: 10)
- Ag + + BH4- + 3H2O → AgO + B (OH) 3 + 3,5H2
Восстановленные атомы металла образуют ядра наночастиц. В целом, этот процесс аналогичен описанному выше методу восстановления с использованием цитрата. Преимуществом использования боргидрида натрия является увеличение монодисперсности конечной популяции частиц. Причина увеличения монодисперсности при использовании NaBH4 заключается в том, что он является более сильным восстановителем, чем цитрат. Воздействие силы восстановительного агента можно увидеть, проверив диаграмму Ламера, которая описывает зарождение и рост наночастиц. Когда нитрат серебра (AgNO3) восстанавливается слабым восстановителем, таким как цитрат, скорость восстановления ниже, что означает, что новые ядра формируются, а старые ядра одновременно растут. Это является причиной того, что реакция цитрата характеризуется низкой монодисперсностью. Так как NaBH4 является значительно более сильным восстановителем, концентрация нитрата серебра быстро снижается, что сокращает время, в течение которого новые ядра формируются и растут одновременно с получением монодисперсной популяции наночастиц серебра. Частицы, образовавшиеся при восстановлении, должны иметь стабилизированные поверхности, чтобы предотвратить нежелательную агломерацию частиц (когда множественные частицы соединяются вместе), рост или огрубение. Движущей силой этих явлений является минимизация поверхностной энергии (наночастицы имеют большое отношение поверхности к объему). Этой тенденции к уменьшению поверхностной энергии в системе можно противостоять путем добавления видов, которые будут адсорбироваться на поверхности наночастиц и снижать активность поверхности частиц, предотвращая, таким образом, агломерацию частиц в соответствии с теорией DLVO и предотвращая рост, занимая места крепления для атомов металла. Химические вещества, которые адсорбируются на поверхности наночастиц, называются лигандами. Некоторые из этих стабилизирующих поверхность видов: NaBH4 в больших количествах, поливинилпирролидон (PVP), додецилсульфат натрия (SDS), и / или додекантиол. 11) После образования частиц в растворе, они должны быть отделены и собраны. Существует несколько общих методов удаления наночастиц из раствора, включая испарение фазы растворителя или добавление химических веществ к раствору, что снижает растворимость наночастиц в растворе. Оба метода вызывают осаждение наночастиц.
Полиольный процесс
Полиольный процесс является особенно полезным методом, поскольку он обеспечивает высокую степень контроля как по размеру, так и по геометрии полученных наночастиц. Обычно синтез полиола начинается с нагревания полиольного соединения, такого как этиленгликоль, 1,5-пентандиол или 1,2-пропиленгликоль7. Добавляют Ag + и капсюлирующий агент (хотя сам полиол также часто является укупорочным средством). Затем разновидность Ag + восстанавливается полиолом до коллоидных наночастиц 12). Процесс полиола является высокочувствительным к условиям реакции, таким как температура, химическая среда и концентрация субстратов. 13) Поэтому, изменяя эти переменные, можно выбирать различные размеры и геометрию для создания таких квази-сфер, пирамид, сфер и проводов. Дальнейшее исследование более подробно изучало механизм этого процесса, а также результирующие геометрии в различных условиях реакции.
Семенной опосредованный рост
Опосредованный семенами рост является синтетическим методом, при котором небольшие, стабильные ядра выращиваются в отдельной химической среде до желаемого размера и формы. Опосредованные семенами методы состоят из двух различных стадий: зародышеобразования и роста. Изменение определенных факторов в синтезе (например, лиганд, время зародышеобразования, восстановитель и т. д.) 14) может контролировать конечный размер и форму наночастиц, делая опосредованный семенами рост популярным синтетическим подходом к управлению морфологией наночастиц. Стадия нуклеации опосредованного семенами роста состоит из восстановления ионов металлов в предшественнике к атомам металлов. Чтобы контролировать распределение по размеру семян, период зародышеобразования должен быть сокращен для монодисперсности. Модель LaMer иллюстрирует эту концепцию. 15) Семена обычно состоят из небольших наночастиц, стабилизированных лигандом. Лиганды являются небольшими, обычно органическими молекулами, которые связываются с поверхностью частиц, предотвращая рост семян. Лиганды необходимы, так как они увеличивают энергетический барьер коагуляции, предотвращая агломерацию. Баланс между силами притяжения и отталкивания в коллоидных растворах может быть смоделирован с помощью теории DLVO. Для контроля формы и роста можно использовать аффинность связывания лиганда и селективность. Для синтеза семян следует выбирать лиганд со средней и низкой аффинностью связывания, чтобы обеспечить обмен в фазе роста. Рост наносерий включает в себя помещение семян в раствор для выращивания. Раствор для роста требует низкой концентрации предшественника металла, лигандов, которые будут легко обмениваться с существующими ранее лигандами семян, и слабой или очень низкой концентрацией восстановителя. Восстановитель не должен быть достаточно прочным для восстановления предшественника металла в растворе для выращивания в отсутствие семян. В противном случае, раствор для роста будет формировать новые центры зародышеобразования вместо роста на существующих (семенах). Рост является результатом конкуренции между поверхностной энергией (которая растет неблагоприятно с ростом) и объемной энергией (которая благоприятно падает с увеличением роста). Равновесие между энергетикой роста и растворения является причиной равномерного роста только на ранее существовавших семенах (без нового зарождения). Рост происходит за счет добавления атомов металлов из раствора для выращивания к семенам и лигандного обмена между лигандами роста (которые имеют более высокую аффинность связывания) и затравочными лигандами 16). Диапазон и направление роста можно регулировать наноразложением, концентрацией предшественника металла, лигандом и условиями реакции (тепло, давление и т. д.). Контроль стехиометрических условий роста раствора контролирует конечный размер частиц. Например, низкая концентрация металлических семян в предшественнике металла в растворе для выращивания будет приводить к образованию более крупных частиц. Было показано, что укупорочный агент контролирует направление роста и, тем самым, форму. Лиганды могут иметь различную аффинность для связывания через частицу. Дифференциальное связывание внутри частицы может привести к несходному росту частиц. Это создает анизотропные частицы с несферическими формами, включая призмы, кубы и стержни. 17)
Свет-опосредованный рост
Световые опосредованные синтезы также были изучены, когда свет может способствовать формированию различных морфологий наночастиц серебра.
Реакция серебряного зеркала
Реакция серебряного зеркала включает превращение нитрата серебра в Ag (NH 3) OH. Затем Ag (NH3) OH восстанавливают в коллоидное серебро с использованием альдегидосодержащей молекулы, такой как сахар. Реакция серебряного зеркала заключается в следующем:
- 2 (Ag (NH3) 2) + + RCHO + 2OH- → RCOOH + 2Ag + 4NH3 18)
Размер и форма образующихся наночастиц трудно контролировать. Тем не менее, этот метод часто используется для нанесения тонких покрытий частиц серебра на поверхности, и в настоящее время проводится дальнейшая работа по созданию наночастиц более равномерного размера.
Ионная имплантация
Ионная имплантация используется для создания наночастиц серебра, внедренных в стекло, полиуретан, силикон, полиэтилен и поли (метилметакрилат). Частицы внедряются в подложку посредством бомбардировки при высоких ускоряющих напряжениях. При фиксированной плотности тока ионного пучка до определенного значения, размер внедренных наночастиц серебра оказался монодисперсным в пределах населенности, после чего наблюдается только увеличение концентрации ионов. Было обнаружено, что дальнейшее увеличение дозы ионного пучка уменьшает размер наночастиц и плотность в подложке-мишени, в то время как ионный пучок, работающий при высоком ускоряющем напряжении с постепенно увеличивающейся плотностью тока, приводит к постепенному увеличению размера наночастиц. Существует несколько конкурирующих механизмов, которые могут привести к уменьшению размера наночастиц; разрушение НЧ при столкновении, распыление поверхности образца, слияние частиц при нагревании и диссоциация 19). Образование внедренных наночастиц является сложным, и все контролируемые параметры и коэффициенты еще не исследованы. Компьютерное моделирование по-прежнему является сложным, поскольку оно включает процессы диффузии и кластеризации, однако его можно разбить на несколько различных подпроцессов, таких как имплантация, диффузия и рост. После имплантации, ионы серебра достигают разной глубины внутри подложки, которая приближается к гауссовскому распределению со средним значением, центрированным на глубине X. Высокотемпературные условия на начальных стадиях имплантации увеличат диффузию примесей в подложке и, как следствие, ограничивают насыщение ионов, которое требуется для нуклеации наночастиц. И температура имплантата, и плотность тока ионного пучка имеют решающее значение для контроля, чтобы получить размер и распределение монодисперсных наночастиц. Низкую плотность тока можно использовать для противодействия тепловому перемешиванию от ионного пучка и накопления поверхностного заряда. После имплантации на поверхность, токи пучка могут повышаться по мере увеличения поверхностной проводимости. Скорость образования примесей быстро падает после образования наночастиц, которые действуют как подвижная ионная ловушка. Это говорит о том, что начало процесса имплантации имеет решающее значение для контроля расстояния и глубины получаемых наночастиц, а также для контроля температуры подложки и плотности ионного пучка. Присутствие и характер этих частиц можно проанализировать с использованием многочисленных методов спектроскопии и микроскопии 20). Наночастицы, синтезированные в субстрате, проявляют поверхностные плазмонные резонансы, о чем свидетельствуют характерные полосы поглощения; эти особенности подвергаются спектральным сдвигам в зависимости от размера наночастиц и неровностей поверхности, однако оптические свойства также сильно зависят от материала подложки композита.
Биологический синтез
Биологический синтез наночастиц предоставил средство для улучшенных технологий по сравнению с традиционными методами, которые требуют использования вредных восстановителей, таких как боргидрид натрия. Многие из этих методов могли бы улучшить их экологию, заменив эти относительно сильные восстановители. Проблемы химического производства наночастиц серебра обычно связаны с высокой стоимостью, а долговечность частиц коротка из-за агрегации. Жесткость стандартных химических методов вызвала использование биологических организмов для уменьшения ионов серебра в растворе в коллоидные наночастицы. 21) Кроме того, точный контроль формы и размера жизненно важен в процессе синтеза наночастиц, поскольку терапевтические свойства НЧ тесно связаны с такими факторами. Следовательно, основной фокус исследований в биогенном синтезе заключается в разработке методов, которые последовательно воспроизводят НЧ с точными свойствами. 22)
Грибы и бактерии
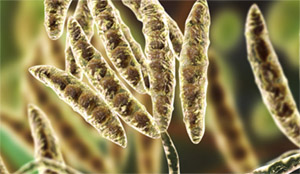 Бактериальный и грибковый синтез наночастиц практичен, потому что бактерии и грибы легко обрабатываются и могут легко модифицироваться генетически. Это обеспечивает средства для разработки биомолекул, которые могут синтезировать AgNP различной формы и размера с высоким выходом, который находится на переднем крае современных проблем синтеза наночастиц. Грибковые штаммы, такие как Verticillium, и бактериальные штаммы, такие как K. pneumoniae, могут быть использованы в синтезе наночастиц серебра. Когда гриб / бактерии добавляют в раствор, биомасса белка выделяется в раствор. Электронные донорские остатки, такие как триптофан и тирозин, уменьшают содержание ионов серебра в растворе, вносимом нитратом серебра. Было обнаружено, что эти методы эффективно создают стабильные монодисперсные наночастицы без использования вредных восстановителей.
Обнаружен способ восстановления ионов серебра за счет введения гриба Fusarium oxysporum. Образующиеся при этом наночастицы имеют размер от 5 до 15 нм и состоят из гидрозоля серебра. Считается, что восстановление наночастиц серебра происходит из ферментативного процесса, и полученные наночастицы серебра чрезвычайно устойчивы благодаря взаимодействию с белками, которые выводятся из организма грибами.
Бактерии, обнаруженные в серебряных рудниках, Pseudomonas stutzeri AG259, были способны создавать частицы серебра в форме треугольников и шестиугольников. Эти наночастицы имели большой диапазон размеров, а некоторые из них достигали размеров более крупных, чем обычные наномасштабы, в 200 нм. Серебряные наночастицы были обнаружены в органической матрице бактерий 23).
Для получения наночастиц серебра используют молочнокислые бактерии. Было установлено, что бактерии Lactobacillus spp., Pediococcus pentosaceus, Enteroccus faeciumI и Lactococcus garvieae способны восстанавливать ионы серебра в наночастицы серебра. Производство наночастиц происходит в клетке при взаимодействии между ионами серебра и органическими соединениями клетки. Было обнаружено, что бактерия Lactobacillus fermentum создает мельчайшие наночастицы серебра со средним размером 11,2 нм. Было также обнаружено, что эта бактерия продуцировала наночастицы с наименьшим распределением по размеру, а наночастицы были обнаружены, главным образом, снаружи клеток. Было также обнаружено, что увеличение рН увеличивает скорость, с которой производятся наночастицы, а также количество образующихся частиц 24).
Бактериальный и грибковый синтез наночастиц практичен, потому что бактерии и грибы легко обрабатываются и могут легко модифицироваться генетически. Это обеспечивает средства для разработки биомолекул, которые могут синтезировать AgNP различной формы и размера с высоким выходом, который находится на переднем крае современных проблем синтеза наночастиц. Грибковые штаммы, такие как Verticillium, и бактериальные штаммы, такие как K. pneumoniae, могут быть использованы в синтезе наночастиц серебра. Когда гриб / бактерии добавляют в раствор, биомасса белка выделяется в раствор. Электронные донорские остатки, такие как триптофан и тирозин, уменьшают содержание ионов серебра в растворе, вносимом нитратом серебра. Было обнаружено, что эти методы эффективно создают стабильные монодисперсные наночастицы без использования вредных восстановителей.
Обнаружен способ восстановления ионов серебра за счет введения гриба Fusarium oxysporum. Образующиеся при этом наночастицы имеют размер от 5 до 15 нм и состоят из гидрозоля серебра. Считается, что восстановление наночастиц серебра происходит из ферментативного процесса, и полученные наночастицы серебра чрезвычайно устойчивы благодаря взаимодействию с белками, которые выводятся из организма грибами.
Бактерии, обнаруженные в серебряных рудниках, Pseudomonas stutzeri AG259, были способны создавать частицы серебра в форме треугольников и шестиугольников. Эти наночастицы имели большой диапазон размеров, а некоторые из них достигали размеров более крупных, чем обычные наномасштабы, в 200 нм. Серебряные наночастицы были обнаружены в органической матрице бактерий 23).
Для получения наночастиц серебра используют молочнокислые бактерии. Было установлено, что бактерии Lactobacillus spp., Pediococcus pentosaceus, Enteroccus faeciumI и Lactococcus garvieae способны восстанавливать ионы серебра в наночастицы серебра. Производство наночастиц происходит в клетке при взаимодействии между ионами серебра и органическими соединениями клетки. Было обнаружено, что бактерия Lactobacillus fermentum создает мельчайшие наночастицы серебра со средним размером 11,2 нм. Было также обнаружено, что эта бактерия продуцировала наночастицы с наименьшим распределением по размеру, а наночастицы были обнаружены, главным образом, снаружи клеток. Было также обнаружено, что увеличение рН увеличивает скорость, с которой производятся наночастицы, а также количество образующихся частиц 24).
Растения
Восстановление ионов серебра в наночастицах серебра также было достигнуто с использованием листьев герани. Было обнаружено, что добавление экстракта листьев герани в растворы нитрата серебра приводит к быстрому восстановлению ионов серебра и повышению стабильности получаемых наночастиц. Полученные в растворе наночастицы серебра имели диапазон размеров от 16 до 40 нм. В другом исследовании для восстановления ионов серебра использовали различные экстракты листьев растений. Было обнаружено, что экстракт листьев магнолии был лучшим при создании наночастиц серебра, в сравнении с Camellia sinensis (зеленым чаем), сосной, хурмой, гинкго, магнолией и платаном. Этот метод создавал частицы с дисперсным размером от 15 до 500 нм, но было также обнаружено, что размер частиц можно регулировать, варьируя температуру реакции. Скорость, с которой ионы восстанавливались экстрактом листьев магнолии, была сопоставима со скоростью, которая наблюдалась при использовании химикатов для восстановления. 25) Использование растений, микроорганизмов и грибов в производстве наночастиц серебра ведет к более экологически безопасному производству наночастиц серебра. Доступен «зеленый метод» для синтеза наночастиц серебра с использованием экстракта листьев листьев Amaranthus gangeticus Linn.
Продукты и функционализация
Синтетические протоколы для производства наночастиц серебра могут быть модифицированы для получения наночастиц серебра с несферическими геометрическими формами, а также для функционализации наночастиц с различными материалами, такими как диоксид кремния. Создание наночастиц серебра различной формы и поверхностных покрытий позволяет лучше контролировать их размер-специфические свойства.
Анизотропные структуры
Серебряные наночастицы могут быть синтезированы в разнообразных несферических (анизотропных) формах. Поскольку серебро, как и другие благородные металлы, проявляет зависящий от размера и формы оптический эффект, известный как локализованный поверхностный плазмонный резонанс (LSPR) в наномасштабе, способность синтезировать наночастицы Ag различной формы значительно увеличивает способность настраивать их оптическое поведение. Например, длина волны, при которой локализованный поверхностный плазмонный резонанс происходит для наночастицы одной морфологии (например, сферы), будет различной, если эта сфера будет изменена на другую форму. Эта зависимость формы позволяет наночастице серебра испытывать оптическое усиление в диапазоне различных длин волн, даже сохраняя размер относительно постоянным, просто изменяя его форму. Использования этого расширенного по форме расширения оптического поведения варьируются от разработки более чувствительных биодатчиков до увеличения долговечности текстильных изделий. 26)
Треугольные нанопризмы
Наночастицы треугольной формы являются «каноническим» типом анизотропной морфологии, изученной как в отношении золота, так и в отношении серебра. 27) Несмотря на то, что существует много различных методов синтеза нанопризм серебра, в нескольких методах используется семенной метод, который включает в себя сначала синтез наночастиц серебра малого диаметра (3-5 нм), которые предлагают шаблон для направленного по форме роста в треугольные наноструктуры. Семена серебра синтезируют смешиванием нитрата серебра и цитрата натрия в водном растворе, а затем быстро добавляют в раствор боргидрид натрия. Нитрат серебра добавляется к затравочному раствору при низкой температуре, и призмы выращиваются путем медленного восстановления избытка нитрата серебра с использованием аскорбиновой кислоты. При опосредованном семенами подходе к синтезу серебрянной нанопризмы, селективность формы может частично контролироваться связывающим лигандом. Используя, по существу, ту же самую методику, которая указана выше, но изменяя цитрат на поливинилпирролидон (ПВП), вместо треугольных нанопризм создаются кубические и стержневые наноструктуры. Помимо метода, опосредованного семенами, серебряные нанопризмы также могут быть синтезированы с использованием фото-подхода, при котором ранее существовавшие сферические наночастицы серебра трансформируются в треугольные нанопризмы, просто путем воздействия реакционной смеси на свет высокой интенсивности. 28)
Нанокубы
Серебряные нанокубы могут быть синтезированы с использованием этиленгликоля в качестве восстановителя и ПВП в качестве защитного вещества в реакции синтеза полиола. Типичный синтез с использованием этих реагентов включает добавление свежего нитрата серебра и ПВП к раствору этиленгликоля, нагретого до 140 °С 29). Эта процедура может быть фактически модифицирована для получения другой анизотропной наноструктуры серебра, нанопроволоки, путем простого старения раствора нитрата серебра, прежде чем использовать его в синтезе. Если позволить раствору нитрата серебр\ а стареть, первоначальная наноструктура, образовавшаяся во время синтеза, несколько отличается от первоначальной наноструктуры, полученной при использовании свежего нитрата серебра, что влияет на процесс роста и, следовательно, на морфологию конечного продукта.
Покрытие кремнеземом
При этом методе, поливинилпирролидон (ПВП) растворяют в воде с помощью ультразвука и смешивают с коллоидными частицами серебра. Активное перемешивание гарантирует, что ПВП адсорбируется на поверхности наночастиц. Центрифугирование разделяет покрытые ПВП наночастицы, которые затем переносятся в раствор этанола для последующего центрифугирования и помещаются в раствор аммиака, этанола и Si (OEt4) (TES). Перемешивание в течение 12 часов приводит к формированию оболочки из диоксида кремния, состоящей из окружающего слоя оксида кремния с эфирной связью, доступной для добавления функциональности. Варьирование количества TES позволяет создавать оболочки различной толщины. Этот метод популярен благодаря возможности добавлять различные функциональные возможности к открытой поверхности кремнезема.
Использование
Катализ
Использование наночастиц серебра для катализа стало привлекать внимание в последние годы. Несмотря на то, что наиболее распространенные применения связаны с лекарственными или антибактериальными целями, было показано, что наночастицы серебра проявляют каталитические окислительно-восстановительные свойства относительно красителей, бензола, монооксида углерода и, вероятно, других соединений. Размер наночастицы значительно определяет свойства, которые она проявляет, благодаря различным квантовым эффектам. Кроме того, химическая среда наночастицы играет большую роль в каталитических связях. Имея это в виду, важно отметить, что гетерогенный катализ происходит путем адсорбции веществ-реагентов на каталитическом субстрате. Когда полимеры, комплексные лиганды или поверхностно-активные вещества используются для предотвращения коалесценции наночастиц, каталитическая способность часто затрудняется из-за снижения адсорбционной способности 30). Однако, эти соединения можно также использовать таким образом, чтобы химическая среда усиливала каталитическую способность.
Поддержание на сферах кремнезема – уменьшение красителей
Серебряные наночастицы были синтезированы на подложке из инертных сфер двуокиси кремния. Подложка не играет практически никакой роли в каталитической способности и служит в качестве способа предотвращения слипания наночастиц серебра в коллоидном растворе. Таким образом, наночастицы серебра были стабилизированы, и было возможно продемонстрировать их способность служить в качестве электронного реле для восстановления красителей боргидридом натрия. Без катализатора наночастиц серебра, практически не происходит никакой реакции между боргидридом натрия и различными красителями: метиленовым синим, эозином и бенгалрозом.
Мезопористый аэрогель – селективное окисление бензола
Наночастицы серебра, нанесенные на аэрогель, являются предпочтительными из-за большего количества активных участков. 31) Наивысшая селективность для окисления бензола до фенола наблюдалась при малом весовом проценте серебра в матрице аэрогеля (1% Ag). Полагают, что эта лучшая селективность является результатом более высокой монодисперсности в матрице аэрогеля образца Ag 1%. Было показано, что наночастицы сплава Au-Ag оказывают синергетическое воздействие на окисление монооксида углерода. Сама по себе, каждая наночастица из чистого металла демонстрирует очень низкую каталитическую активность для окисления СО; вместе, каталитические свойства значительно усиливаются. Предполагается, что золото действует как сильный связующий агент для атома кислорода, а серебро служит в качестве сильного окислительного катализатора, хотя точный механизм до сих пор полностью не понят. При синтезе в соотношении Au / Ag от 3: 1 до 10: 1, сплавленные наночастицы показали полную конверсию, когда 1% СО подавали на воздухе при температуре окружающей среды. Интересно, что размер сплавленных частиц не играет большой роли в каталитической способности. Хорошо известно, что наночастицы золота показывают каталитические свойства для CO, только когда они имеют размер ~ 3 нм, но сплавленные частицы до 30 нм демонстрируют отличную каталитическую активность – лучше, чем у наночастиц золота на активной подложке, такой как TiO2, Fe2O3 и т. д.
Световые эффекты
Плазмонические эффекты изучены довольно широко. До недавнего времени не было исследований, изучающих окислительное каталитическое усиление наноструктуры путем возбуждения ее поверхностного плазмонного резонанса. Определяющей особенностью для усиления окислительной каталитической способности была определена способность превращать пучок света в форму энергичных электронов, которые могут быть переданы адсорбированным молекулам. Следствием такого признака является то, что фотохимические реакции могут управляться непрерывным светом малой интенсивности, могут сочетаться с тепловой энергией. Сочетание непрерывного света низкой интенсивности и тепловой энергии было выполнено с помощью серебряных нанокубов. Важной особенностью серебряных наноструктур является то, что они позволяют осуществлять фотокатализ из-за своей природы для создания резонансных поверхностных плазмонов из света в видимом диапазоне. Добавление светового усиления позволило частицам работать в той же степени, что и частицы, которые были нагреты до 40 К и больше. Это важный вывод, если учесть, что снижение температуры на 25 К может увеличить срок службы катализатора почти в 10 раз при сравнении фототермического и термического процессов.
Биологическое исследование
Исследователи изучили использование серебряных наночастиц в качестве носителей для доставки различных грузов, таких как небольшие молекулы лекарств или большие биомолекулы, к конкретным мишеням. Как только у AgNP будет достаточно времени для достижения своей цели, выпуск полезного груза может быть потенциально вызван внутренним или внешним стимулом. Направление и накопление наночастиц может обеспечить высокую концентрацию полезных грузов в определенных целевых местах и может минимизировать побочные эффекты 32).
Химиотерапия
 Введение нанотехнологий в медицину, как ожидается, будет способствовать диагностическому обнаружению рака и стандартам для разработки лекарственных препаратов. Нанотехнологии могут раскрывать представление о структуре, функциях и организационном уровне биосистемы в наномасштабе 33). Наночастицы серебра могут подвергаться методам покрытия, которые обеспечивают однородную функционализированную поверхность, к которой могут быть добавлены субстраты. Когда наночастица покрыта, например, кремнеземом, поверхность существует в виде кремниевой кислоты. Таким образом, субстраты можно добавлять через стабильный эфир и сложноэфирные связи, которые не разрушаются непосредственно естественными метаболическими ферментами. Недавние химиотерапевтические применения разработали противораковые лекарственные средства с фоторастворимым линкером, таким как орто-нитробензиловый мостик, прикрепляющий его к субстрату на поверхности наночастиц. Комплекс наночастиц с низкой токсичностью может оставаться жизнеспособным при метаболическом воздействии в течение времени, необходимого для распределения по всем системам органов. Если раковую опухоль целенаправленно лечить, в область опухоли может быть введен ультрафиолетовый свет. Электромагнитная энергия света заставляет фоточувствительный линкер прорываться между лекарственным средством и субстратом наночастиц. 34) Теперь препарат расщепляется и высвобождается в неизмененной активной форме для воздействия на раковые опухолевые клетки. Предполагаемые преимущества этого метода заключаются в том, что препарат транспортируется без высокотоксичных соединений, лекарственное средство высвобождается без вредного излучения или полагается на специфическую химическую реакцию, которая может произойти, и лекарство может быть селективно высвобождено в ткани-мишени. Второй подход заключается в прикреплении химиотерапевтического лекарственного средства непосредственно к функционализированной поверхности наночастицы серебра в сочетании с нуклеофильным видом для осуществления реакции смещения. Например, как только лекарственный комплекс наночастиц попадает или находится вблизи ткани-мишени или клеток-мишеней, моноэфир глютатиона может вводиться на участок. 35) Кислород нуклеофильного эфира будет прикрепляться к функционализированной поверхности наночастицы посредством новой сложноэфирной связи, в то время как лекарство высвобождается в окружающую среду. Препарат теперь активен и может осуществлять свою биологическую функцию на клетках, непосредственно примыкающих к его окружению, что ограничивает нежелательные взаимодействия с другими тканями.
Введение нанотехнологий в медицину, как ожидается, будет способствовать диагностическому обнаружению рака и стандартам для разработки лекарственных препаратов. Нанотехнологии могут раскрывать представление о структуре, функциях и организационном уровне биосистемы в наномасштабе 33). Наночастицы серебра могут подвергаться методам покрытия, которые обеспечивают однородную функционализированную поверхность, к которой могут быть добавлены субстраты. Когда наночастица покрыта, например, кремнеземом, поверхность существует в виде кремниевой кислоты. Таким образом, субстраты можно добавлять через стабильный эфир и сложноэфирные связи, которые не разрушаются непосредственно естественными метаболическими ферментами. Недавние химиотерапевтические применения разработали противораковые лекарственные средства с фоторастворимым линкером, таким как орто-нитробензиловый мостик, прикрепляющий его к субстрату на поверхности наночастиц. Комплекс наночастиц с низкой токсичностью может оставаться жизнеспособным при метаболическом воздействии в течение времени, необходимого для распределения по всем системам органов. Если раковую опухоль целенаправленно лечить, в область опухоли может быть введен ультрафиолетовый свет. Электромагнитная энергия света заставляет фоточувствительный линкер прорываться между лекарственным средством и субстратом наночастиц. 34) Теперь препарат расщепляется и высвобождается в неизмененной активной форме для воздействия на раковые опухолевые клетки. Предполагаемые преимущества этого метода заключаются в том, что препарат транспортируется без высокотоксичных соединений, лекарственное средство высвобождается без вредного излучения или полагается на специфическую химическую реакцию, которая может произойти, и лекарство может быть селективно высвобождено в ткани-мишени. Второй подход заключается в прикреплении химиотерапевтического лекарственного средства непосредственно к функционализированной поверхности наночастицы серебра в сочетании с нуклеофильным видом для осуществления реакции смещения. Например, как только лекарственный комплекс наночастиц попадает или находится вблизи ткани-мишени или клеток-мишеней, моноэфир глютатиона может вводиться на участок. 35) Кислород нуклеофильного эфира будет прикрепляться к функционализированной поверхности наночастицы посредством новой сложноэфирной связи, в то время как лекарство высвобождается в окружающую среду. Препарат теперь активен и может осуществлять свою биологическую функцию на клетках, непосредственно примыкающих к его окружению, что ограничивает нежелательные взаимодействия с другими тканями.
Множественная лекарственная резистентность
Основной причиной неэффективности современных методов химиотерапии является множественная лекарственная резистентность, которая может возникать в результате нескольких механизмов 36). Наночастицы могут служить средством для преодоления МЛР. В общем, при использовании нацеливающего агента для доставки нанопереносчиков к раковым клеткам, необходимо, чтобы агент связывался с высокой избирательностью по отношению к молекулам, которые однозначно экспрессируются на поверхности клетки. Таким образом, НЧ могут быть сконструированы с протеинами, которые специфически обнаруживают лекарственно- резистентные клетки с избыточно экспрессируемыми транспортерными белками на их поверхности. Трудность, с которыми связаны распространенные системы доставки нанолекарств, состоит в том, что свободные лекарства, которые высвобождаются из нанопереносчиков в цитозоль, снова подвергаются воздействию транспортеров МЛР и экспортируются. Чтобы решить эту проблему, 8 нм частицы нанокристаллического серебра были модифицированы добавлением трансактивирующего транскрипционного активатора (ТАТ), полученного из вируса ВИЧ-1, который действует как пептид, проникающий в клетку (СРР). Как правило, эффективность AgNP ограничена из-за отсутствия эффективного клеточного поглощения; однако, CPP-модификация стала одним из наиболее эффективных методов улучшения внутриклеточной доставки наночастиц. После приема внутрь, экспорт AgNP предотвращается на основе исключения по размеру. Концепция проста: наночастицы слишком велики для того, чтобы их выкачивали транспортеры MDR, потому что функция эффлюкса строго подчинена размеру его субстратов, который обычно ограничивается диапазоном 300-2000 Да. Таким образом, наночастицы остаются невосприимчивыми к эффлюксу, обеспечивая средство для накопления в высоких концентрациях.
Антимикробная активность
Введение серебра в бактериальные клетки вызывает высокую степень структурных и морфологических изменений, которые могут привести к гибели клеток. По мере того, как наночастицы серебра контактируют с бактериями, они прилипают к клеточной стенке и клеточной мембране. 37) Связанная часть серебра проходит внутрь и взаимодействует с фосфатсодержащими соединениями, такими как ДНК и РНК, в то время как другая часть прилипает к серосодержащим белкам на мембране. Взаимодействия серебра и серы на мембране вызывают структурные изменения клеточной стенки, такие как образование ямок и пор. Через эти поры, клеточные компоненты высвобождаются во внеклеточную жидкость, просто из-за осмотической разницы. Внутри клетки, интеграция серебра создает область с низкой молекулярной массой, где затем конденсируется ДНК. Наличие ДНК в конденсированном состоянии тормозит репликацию клеток белками в контакте с ДНК. Таким образом, введение наночастиц серебра препятствует репликации и является достаточным, чтобы вызвать гибель клетки. В дальнейшем, эффект увеличивается, когда серебро контактирует с жидкостями, приводя к ионизации, увеличивая бактерицидную активность наночастиц. Это было связано с подавлением ферментов и ингибированием экспрессии белков, которые связаны со способностью клетки продуцировать АТФ. Было замечено, что, в общем случае, наночастицы серебра со средним размером 10 нм или менее показывают электронные эффекты, которые значительно повышают их бактерицидную активность, хотя этот эффект варьирует для каждого типа предлагаемой клетки, так как состав их клеточных мембран сильно различается. 38) Это также может быть отчасти связано с тем, что, по мере уменьшения размера частиц, реакционная способность увеличивается за счет увеличения площади поверхности и объема. Было отмечено, что введение наночастиц серебра проявляет синергическую активность с распространенными сегодня антибиотиками, такими как: пенициллин G, ампициллин, эритромицин, клиндамицин и ванкомицин против E.coli и S. aureus. 39) В медицинских условиях было показано, что наночастицы серебра резко снижают количество бактерий в используемых устройствах. Однако, проблема возникает, когда процедура завершена, и нужно проводить новую. В процессе мытья инструментов, большая часть наночастиц серебра становится менее эффективной из-за потери ионов серебра. Наночастицы серебра более широко используются в костных трансплантатах для жертв ожогов, поскольку наночастицы серебра, внедренные с имплантатом, обеспечивают лучшую противомикробную активность и приводят к значительному уменьшению рубцевания. Они также показывают перспективное применение в качестве метода очистки воды 40). Наночастицы серебра могут препятствовать росту бактерий или прилипанию к поверхности. Это может быть особенно полезно в хирургических установках, когда все поверхности, контактирующие с пациентом, должны быть стерильными. Интересно отметить, что наночастицы серебра могут быть использованы на многих типах поверхностей, включая металлы, пластик и стекло. Эти новые применения являются прямыми «потомками» более старых практик, в которых нитрат серебра использовали для лечения таких состояний, как язвы кожи. Теперь наночастицы серебра используются в бинтах и пластырях, чтобы помочь излечить определенные ожоги и раны. Они также показывают перспективное применение в качестве метода очистки воды. Вода может содержать многочисленных возбудителей болезней, и в некоторых частях мира чистая вода, да и вода вообще, считается роскошью. Метод использования серебра для удаления микробов не нов, но в этом эксперименте использовался карбонат в воде, чтобы сделать микробы еще более уязвимыми для серебра. Сначала ученые этого эксперимента используют наночастицы для удаления определенных пестицидов из воды, которые оказываются смертельными для людей, если они попадают в организм. Несколько других тестов показали, что наночастицы серебра способны удалять определенные ионы в воде, такие как железо, свинец и мышьяк. Но это не единственная причина, почему наночастицы серебра настолько привлекательны, что они не требуют какой-либо внешней силы (нет электричества в гидролизе) для реакции. 41)
Товары народного потребления
Бытовые применения
Имеются примеры использования наночастиц серебра и коллоидного серебра в потребительских товарах. Samsung и LG – две крупные технологические компании, планирующие использовать антибактериальные свойства наночастиц серебра во множестве приборов, таких как кондиционеры, стиральные машины и холодильники. 42) Например, обе компании утверждают, что использование наночастиц серебра в стиральных машинах поможет стерилизовать одежду и воду во время мытья и полоскания, а также позволит очистить одежду без необходимости горячей воды. Наночастицы в этих приборах синтезируются с помощью электролиза. Через электролиз, серебро извлекается из металлических пластин, а затем превращается в наночастицы серебра при помощи восстановителя. Этот метод позволяет избежать процессов сушки, очистки и повторной дисперсии, которые обычно требуются при альтернативных способах коллоидного синтеза. 43)
Безопасность
Хотя наночастицы серебра широко используются в составе различных коммерческих продуктов, в последнее время предпринимаются серьезные усилия для изучения их воздействия на здоровье человека. Было проведено несколько исследований, описывающих токсичность наночастиц серебра in vitro для различных органов, включая легкие, печень, кожу, мозг и репродуктивные органы 44). Механизм токсичности наночастиц серебра в клетках человека, по-видимому, обусловлен окислительным стрессом и воспалением, которые вызываются образованием активных форм кислорода (АФК), стимулированных либо NP-Ag, либо ионами Ag, либо обоими факторами. 45) Например, Park et al. показали, что воздействие линии клеток перитонеальных макрофагов мыши (RAW267.7) на наночастицы серебра снижает жизнеспособность клеток в зависимости от концентрации и времени. Они также показали, что внутриклеточный редуцированный глутатионин (GSH), который является поглотителем АФК, уменьшился до 81,4% контрольной группы наночастиц серебра при 1,6 частей на миллион.
Режимы токсичности
Поскольку наночастицы серебра подвергаются растворению, высвобождая ионы серебра, 46) которые, как известно, обладают токсическими эффектами, было проведено несколько исследований, чтобы определить, является ли токсичность наночастиц серебра результатом выделения ионов серебра, или она связана с самой наночастицей. Несколько исследований показывают, что токсичность наночастиц серебра объясняется высвобождением ионов серебра в клетках, так как сообщалось о том, что как наночастицы серебра, так и ионы серебра обладают сходной цитотоксичностью. 47) Например, в некоторых случаях сообщается, что наночастицы серебра облегчают высвобождение токсичных свободных ионов серебра в клетках с помощью «механизма типа троянского коня», когда частица попадает в клетки и затем ионизируется внутри клетки. Тем не менее, поступают сообщения о том, что комбинация наночастиц серебра и ионов ответственна за токсический эффект наночастиц серебра. Navarro et al., используя цистеиновые лиганды в качестве инструмента для измерения концентрации свободного серебра в растворе, установили, что, хотя первоначально ионы серебра в 18 раз более вероятно ингибировали фотосинтез водорослей Chlamydomanas reinhardtii, после 2 часов инкубации было обнаружено, что водоросли, содержащие наночастицы серебра, были более токсичными, чем только ионы серебра. Кроме того, имеются исследования, которые показывают, что наночастицы серебра индуцируют токсичность, независимую от свободных ионов серебра. 48) Например, Asharani et al. сравнивали фенотипические дефекты, наблюдаемые у рыбок данио, обработанных наночастицами серебра и ионами серебра, и установили, что фенотипические дефекты, наблюдаемые при обработке наночастицами серебра, не наблюдались у зародышей, обработанных ионным серебром, что указывает на то, что токсичность наночастиц серебра не зависит от ионов серебра. Белковые каналы и поры ядерной мембраны часто могут иметь размер от 9 нм до 10 нм в диаметре. Маленькие серебряные наночастицы такого размера обладают способностью не только проходить через мембрану, взаимодействовать с внутренними структурами, но и застревать в мембране. Отложения наночастиц серебра в мембране могут влиять на регуляцию растворения, обмен белков и распознавание клеток. Воздействие наночастиц серебра связано с «воспалительными, окислительными, генотоксическими и цитотоксическими последствиями»; частицы серебра накапливаются, главным образом, в печени. Но также было показано, что они токсичны в других органах, включая мозг. Нано-серебро, применяемое к клеткам, культивируемым тканевыми клетками, приводит к образованию свободных радикалов, что вызывает опасения в отношении потенциальных рисков для здоровья. 49)
- Аллергические реакции: было проведено несколько исследований, в которых было показано, что аллергенность наночастиц серебра является возможной. 50)
- Аргирия и окрашивание: ингредиенты серебра, включая коллоидное серебро, могут вызывать состояние, называемое аргирией, обесцвечивание кожи и органов. В 2006 году было проведено исследование 17-летнего мужчины, который имел устойчивые ожоги до 30% тела, и его кожа временно имела сине-серый оттенок после нескольких дней применения Acticoat, марки раневой повязки, содержащей наночастицы серебра. Аргирия – это отложение серебра в глубоких тканях, состояние, которое не может произойти на временной основе, поднимая вопрос о том, является ли причиной обесцвечивания человека аргирия или же это результат обработки серебром. Известно, что серебряные повязки вызывают «временное изменение цвета», которое рассеивается через 2-14 дней, но не является постоянным обесцвечиванием.
- Сердечный клапан Silzone: St. Jude Medical выпустила механический сердечный клапан с покрытой серебром манжетой (покрытой ионным пучком с помощью осаждения) в 1997 году. 51) Клапан был разработан для уменьшения случаев эндокардита. Клапан был одобрен для продажи в Канаде, Европе, США и на большинстве других рынков по всему миру. В исследовании, проведенном после коммерциализации, исследователи показали, что клапан предотвращает врастание ткани, создает паравольтную утечку, ослабление клапана и, в худшем случае, эксплантацию. Спустя 3 года на рынке и продажи 36000 имплантатов, Сент-Джуд прекратил работу и добровольно отозвал клапан с рынка.










