Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Пикеатаннол
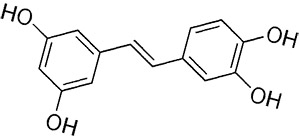
Пикеатаннол представляет собой стильбен, сходный по структуре и свойствам с ресвератролом - веществом, содержащимся в небольших количествах в некоторых из тех же продуктов, что и Пикеатаннол. Оба вещества обладают похожими свойствами, и Пикеатаннол, возможно, является достойной альтернативой ресвератролу, хотя в настоящее время нет достаточного количества научных фактов в пользу преимуществ первого. Другие названия: астрингинин
Источники и структура
Источники Пикеатаннола
Пикеатаннол является одним из основных диетических стильбенов (особый класс природных органических соединений, обладающих потенциальной пользой для нашего здоровья); к этому классу также относятся птеростильбен and ресвератрол1). Иногда Пикеатаннол называеют астрингинином, хотя последний считается гликозидом (Пикеатаннол-3'-O-β-d-глюкопиранозид).2) Из-за схожей структуры, эти вещества обладают одинаковыми свойствами,3) существуют лишь небольшие различия в химическом составе. Многие свойства Пикеатаннола являются уникальными, в частности, повышенное содержание полезных для здоровья веществ. По своей структуре, Пикеатаннол напоминает ресвератрол, не считая незначительных отклонений, и, наряду с ресвератролом и его производными стильбенами, содержится в растениях. В ходе исследования ресвератрола были выявлены полезные свойства Пикеатаннола, что подтолкнуло ученых со всего мира к дальнейшему изучению стильбенов. Ниже приведен список стандартных диетических продуктов, в которых содержится Пикеатаннол:
- Ягоды семейства Вакциниум, включая голубику высокорослую (Голубика; 186-422нг/г в сухих плодах) и чернику тычиночную (Черника; 138-195нг/г в сухих плодах), но в меньших количествах, чем ресвератрол
- Ягоды семейства ежевичных
- Обычно отсутствует или присутствует в незначительном количестве в винограде (Vitus genera), но содержание Пикеатаннола увеличивается (на 50-100%), в ходе послеуборочного облучения урожая, меры, также необходимой для выделения ресвератрола4); например, в свежих ягодах винных сортов винограда Каберне Совиньон содержится до 52нг/г Пикеатаннола;[5] в красных винах прочих сортов Пикеатаннол присутствует в различной концентрации от 0.54 до 5.22мг/л5) , либо вообще отсутствует6).
- Миндаль; Пикеатаннол обнаружен в воде после бланширования орехов (вместе с окси-ресвератролом) в концентрации 0.19-2.55нг/100г миндаля7)
- Семена мараккуйи - 2.2мг/г (вес сырых семян) и 4.8мг/г (вес высушенных сублимацией семян)8) , но не обнаружен ни в кожуре, ни в мякоти плодов.
- Ревень (Ревень обыкновенный), в котором также содержится дигликозид Пикеатаннола9).
- Арахис - до 18.69 ± 2.52 мкг/г, когда рост арахиса угнетен Botryodiplodia theobromae (грибным патогеном, поражающим растение); или 6.93+/-2.03мкг/г, если растение поражено другими грибами, такими, как Рейши10)
- Черный чай (ферментированная камелия китайская) - 14-53мкг/г Пикеатаннола (и 51-56мкг/г транс-ресвератрола); а ввиду того, что в зеленом чае (неферментированной камелии китайской) содержится 14-53мкг/г11) Пикеатаннола, маловероятно, что ферментация влияет на уровень содержания в чае стильбенов. В Цейлонском чае - 49+/-4мкг/г Пикеатаннола
- Ромашка аптечная- 11+/-0.2мкг/г
Во всех растениях, в которых содержится Пикеатаннол, наряду с ним всегда присутствует и ресвератрол. (И, наоборот, в большинстве растений, содержащих ресвератрол, также присутствует Пикеатаннол, хотя и в меньшей концентрации). При сравнении продуктов одной пищевой группы с продуктами из другой, концентрация Пикеатаннола варьируется значительнее, чем концентрация ресвератрола, и Пикеатаннол предположительно является более волатильным компонентом. Пикеатаннол также содержится в диетических пищевых добавках и в растениях, не входящих в список диетических, а именно: • Циссус четырехугольный12) • Горец Сахалинский - 0.025-0.067мг/г (астрингин - 0.98-1.22мг/г),[17] хотя в одном из подвидов (sachalinensis) Пикеатаннол был обнаружен в микроскопических количествах[17] , а в других растениях данного вида содержался только астрингин13). • Маклюра оранжевая14) • Александрийский лист15) Пищевые добавки, в составе которых присутствует ресвератол, обычно содержат следовые количества Пикеатаннола. Однако в настоящее время учеными не было найдено ни одной пищевой добавки или растения, в которых Пикеатаннол содержится в достаточно высоком количестве (либо сам по себе, либо в сочетании с другими стильбенами, такими, как ресвератол). В ягодах, содержащих Пикеатаннол, обычно присутствуют микроскопические дозы птеростильбена и, наоборот, в некоторых ягодах (голубика прутьевидная) содержится только птеростильбен, в других же (голубика высокорослая) содержится только Пикеатаннол; в некоторых видах (черника тычиночная) в различных количествах содержится либо то, либо другое вещество, но не оба. Подобная взаимосвязь характерна только для пары Пикеатаннол – птеростильбен и не имеет отношения к ресвератолу (он присутствует во всех ягодах). Установлено, что Пикеатаннол существует в природе в виде гомодимера или гетеродимеров в паре с ресвератолом (в винах).
Структура
По своей структуре Пикеатаннол очень напоминает ресвератол, ведь в его составе присутствует гидроксильная группа (3,5,4',3'-тетрагидроксистильбен), которая отличается от одноименной группы ресвератола всего на 3 углерода (3,5,4'-тригидрооксистильбен).16) Гликозидом Пикеатаннола является астрингин или Пикеатаннол-3'-O-β-d-гликопиранозид.
Физико-химические свойства
Пикеатаннол выглядит как белесоватый порошок с чуть более низкой температурой плавления (226–223°C), чем у ресвератола (253–255°C), и чуть более тяжелыми молекулами - 244.24 (у ресвератола - 228.24).17) Оба вещества растворяются в этиловом спирте и ДМСО (диметилсульфооксид), но не в воде, и, подобно ресвератролу, Пикеатаннол в большинстве случаев (связанных с химически более стабильной молекулой транс-Пикеатаннола) встречается либо в цис-, либо в транс-форме.
Молекулярные мишени
Фосфоинозитол-3-киназа
Недавно ученые установили, что Пикеатаннол эффективно блокирует сигналы фосфоинозитол-3-киназы, препятствуя перемещению и размножению клеток гладкой мышцы аорты человека.18) Несмотря на подобный эффект ресвератола, хоть и менее выраженный, способность Пикеатаннола активно подавлять сигналы фосфоинозитол-3-киназы считают уникальным свойством этого стильбена; Пикеатаннол блокировал сигналы фосфоинозитол-3-киназы в клетках гладкой мышцы аорты человека в диапазоне 10-20мкм, тогда как эффект от ресвератола в концентрациях до 20мкм был слабовыраженным. Примечательно, что Пикеатаннол блокировал сигналы фосфоинозитол-3-киназы как внутри организма, так и вне его с большей эффективностью, чем LY294002, популярный низкомолекулярный ингибитор фосфоинозитол-3-киназы. Пикеатаннол способен тормозить сигналы вышеупомянутого вещества, являясь непосредственным конкурентом АДФ на участке, связывающем АДФ и фосфоинозитол-3-киназу. Пикеатаннол является мощным блокиратором сигналов фосфоинозитол-3-киназы. Несмотря на наличие подобных свойств у ресвератола, Пикеатаннол в данном случае является гораздо более эффективным средством. Хотя все эксперименты производились вне живого организма. Известно, что Пикеатаннол блокирует сигналы тирозин киназы селезенки (Syk) в живом организме при росте тромбоцитов в эндотелиальной клетке,19) при этом Syk необходим для размножения клеток под влиянием тромбоцитного фактора роста.) При блокировке тирозин киназы селезенки в живых организмах и на животных моделях, Пикеатаннол обладает анти-аллергическими свойствами 20). Он блокирует Syk, напрямую прикрепляясь к нему на участке, связывающим его с белком-ингибитором, угнетающим киназу p40. Оказывается, Пикеатаннол является селективным ингибитором тирозин киназы селезенки, что делает его предметом многочисленных исследований, направленных на изучение функции тирозин киназы селезенки.
ЦОГ-2
В то время, как ресвератрол является ингибитором ЦОГ-2 с концентрацией полу-максимального ингибирования 530нМ,21) Пикеатаннол превосходит его по двум пунктам: будучи как более мощным ингибитором, так и более селективным в отношении ЦОГ-2; при блокировке ЦОГ-2 он обладает концентрацией полу-максимального ингибирования 11нМ и является в 417 раз более избирательным в отношении ЦОГ-2 (по сравнению с ЦОГ-1).22) То есть, Пикеатаннол чуть менее селективен, чем целекоксиб, который в 546 раз более избирателен в отношении ЦОГ-2 (по сравнению с ЦОГ-1) с концентрацией полу-максимального ингибирования 34нM, и гораздо более селективен, чем ресвератрол, не являющийся, по сути, селективным ингибитором. Пикеатаннол прикрепляется напрямую к Arg120, Ser530 и Tyr385 ЦОГ-2, не контактируя при этом со связующим участком, отвечающим за селективность ингибиторов ЦОГ-2 (второстепенной полостью[28]). Пикеатаннол является селективным ингибитором ЦОГ-2, а его избирательность в отношении последнего и потенциальные возможности гораздо более значительны, чем у ресвератрола (в живых организмах и при сравнении с целекоксибом). Ввиду значительных различий между Пикеатаннолом и ресвератролом, полезные свойства обеих пищевых добавок, связанные с блокировкой ЦОГ-2, также различаются.
АТФаза
Учеными было отмечено, что Пикеатаннол является ингибитором АТФазы смешанного типа,23) в частности, F-АТФазы (АТФаза во внутренней митохондриальной мембране) и части F1-АТФазы в особенности.24) Каталитическая единица F1 состоит из нескольких элементов (α3, β3, γ1, δ1 и ε1)25), тогда как элемент F0 фиксирует F1 на мембране и равномерно распределяет протоны. Пикеатаннол прикрепляется к элементу γ (в АТФазе у жвачных животных), блокируя АТФазу; данный процесс характерен также для ресвератрола и кверцитина,26) однако исследование бактериальной АТФазы (Escherichia coli) показало, что эти добавки препятствуют взаимодействию элемента γ с элементом β.27) Пикеатаннол, подобно ресвератролу, способен ингибировать АТФазу, но на сегодняшний день мы не знаем обо всех потенциальных возможностях первого и, как следствие, о целесообразности его применения на практике.
Фармакология
Усвоение организмом
Опыты показали, что Пикеатаннол усваивается крысами.28) Когда ученые обнаружили Пикеатаннол в 2-гидроксипропил-β-циклодекстрине, биодоступность первого составляла 50.7+/-15.0%; что выше, чем у ресвератрола, но ниже, чем у птеростильбена. После перорального введения Пикеатаннола крысам, вещество усваивается стенками их кишечника.
Сыворотка крови
 Пероральное употребление внутрь Пикеатаннола вызывает резкий скачок концентрации его уровня в сыворотке крови до 710+/-219нг/мл в течение 45-120 минут после употребления данной добавки.29)
Пикеатаннол присутствует в плазме крови крыс на протяжении 12 часов после внутривенного вливания 10мг/кг веса в концентрации 19+/-2нг/мл30) и при пероральном употреблении внутрь 10мг/кг в концентрации 28+/-3нг/мл. Суммарная концентрация Пикеатаннола в плазме крови после перорального приема внутрь 10мг/кг больше, чем при внутривенном вливании 4мг/кг. Спустя 12 часов после приема концентрация препарата в крови постепенно снижается.
Пикеатаннол проникает в плазму крысиной крови в пиковой нано-молярной концентрации, но, вероятно, более длительное (12 часов) и благоприятное воздействие на организм препарат оказывает в низкой нано-молярной концентрации.
Пероральное употребление внутрь Пикеатаннола вызывает резкий скачок концентрации его уровня в сыворотке крови до 710+/-219нг/мл в течение 45-120 минут после употребления данной добавки.29)
Пикеатаннол присутствует в плазме крови крыс на протяжении 12 часов после внутривенного вливания 10мг/кг веса в концентрации 19+/-2нг/мл30) и при пероральном употреблении внутрь 10мг/кг в концентрации 28+/-3нг/мл. Суммарная концентрация Пикеатаннола в плазме крови после перорального приема внутрь 10мг/кг больше, чем при внутривенном вливании 4мг/кг. Спустя 12 часов после приема концентрация препарата в крови постепенно снижается.
Пикеатаннол проникает в плазму крысиной крови в пиковой нано-молярной концентрации, но, вероятно, более длительное (12 часов) и благоприятное воздействие на организм препарат оказывает в низкой нано-молярной концентрации.
Распространение
Учеными было отмечено, что Пикеатаннол прикрепляется к транс-тиретину (ТТР), подобно тому, как ресвератрол оседает на связующем участке тироксина 31), и т.к. ТТР является транспортировочным белком небольших молекул в кровяной сыворотке и мозге, считается, что Пикеатаннол, ввиду плохой растворимости в воде, попадает в кровь непосредственно через ТТР. Учеными подтвержден тот факт, что Пикеатаннол связывает транспортировочные белки в человеческом организме, и, таким образом, циркулирует в крови и спинномозговой жидкости. Инъекционный Пикеатаннол попадает в кровь крыс в значительных количествах - 10.76+/-2.88л/кг; и, поскольку это происходит в объеме, большем, чем общий запас жидкости в организме, Пикеатаннол выходит из кровяной сыворотки и накапливается в тканях.32) На сегодняшний день ученые оперируют достаточным количеством фактов, свидетельствующих о последующем накоплении Пикеатаннола в тканях организма.
Метаболизм
Человеческая печень способна преобразовывать ресвератрол в Пикеатаннол33) с помощью изоферментов цитохромов CYP1B1 (трех метаболитов, из которых, наряду с 3,4,5,4′-тетра-гидроксистильбеном и 3,4,5,3′,4′-пента-гидроксистильбеном34) выделяется Пикеатаннол), либо с помощью ферментов CYP1A (ароматазы).35) Данные трансформации происходили в ходе опытов над мышами, когда им перорально давали 75мг/кг ресвератрола (который достигал кожи, печени, и через пять минут после введения его концентрация в крови доходила до 21.75+/-7.22мкM, 73.04+/-35.61мкM и 28.37+/-32.63мкM соответственно).36) Концентрация Пикеатаннола в кровяной сыворотке была на 1% ниже концентрации ресвератрола за одинаковый промежуток времени, причем глюкорониды ресвератрола в данном случае обладали теми же свойствами, что и сам ресвератрол. При метаболизме ресвератрол может превращаться в Пикеатаннол, но в живых организмах подобные трансформации незначительны (и мало изучены). После Фазы I структура Пикеатаннола не меняется,37) однако известно, что он превращается либо в ди-сульфат, либо в один-два моно-сульфата.38) Пикеатаннол, при участии UG–энзимов, продуцирует три отдельные моно-глюкоронида, причем как в кровяной сыворотке у крыс, так и в микросомах человеческой печени. Известно, что глюкорониды образуются при внутривенном вливании крысам 10мг/кг Пикеатаннола. Пикеатаннол образует соединения подобно ресвератролу, продуцируя сульфаты и глюкорониды, наиболее быстро в живых организмах.
Выведение из организма
У крыс Пикеатаннол выводится из организма преимущественно через печень после укола, по мере того, как скорости почечного (2.13+/-0.92 л/ч/кг) и печеночного клиренсов (1.43 л/ч/кг) приближаются к скорости движения плазмы печени (1.74 л/ч/кг).39)
Фаза I. Реакции ферментов
Один из ферментов, преобразующих ресвератрол в Пикеатаннол (CYP1A), ими же и блокируется (Ki на 5.33мкM и 9.67μM соответственно), но Пикеатаннол в концентрациях от 1 до 100мкM не может ингибировать CYP2E1, в отличие от ресвератрола (Ki на 2.1мкM).40)
Фаза II. Реакции ферментов
Пикеатаннол способен вступать в реакции с ферментом хинон-редуктазы-2 (NQO2) на том же участке, что и ресвератрол.41)
Неврология
Нейровоспаление
В микроглиальных клетках на фоне блокировки тирозин киназы селезенки Пикеатаннол проявляет анти-воспалительные свойства. В ходе исследования белка приона (PrP106-126,42) который на фоне активации микроглии43) становится нейротоксичным) было выявлено, что белок CD36, активируя микроглию, служит своего рода регулятором деятельности PrP106-126 (подобную ситуацию ранее наблюдали на примере PrP106-12644) и других нейротоксичных белков, таких как «белок Альцгеймера» Aβ1-42); известно также, что для прохождения сигналов CD36 необходима тирозин киназа селезенки; Пикеатаннол и PrP106-126 используют при выращивании микроглиальных клеток, и ученые предполагают, что эти вещества предотвращают индукцию иРНК индуцибельной синтазы оксида азота и воспалительных цитокинов, что обычно происходит при активизации микроглии.45) Таким образом, инкубируя тирозин киназу селезенки, Пикеатаннол способен уменьшать нейровоспаление.
Защита нервных клеток
Пикеатаннол позволяет непрерывно инкубировать нервные клетки в течение как минимум 6 часов (HT-22 ), тем самым обеспечивая временную защиту этих клеток от токсического воздействия глютаматов (в концентрациях 5-10мкM , но не 1мкM), и такой защитный эффект отчасти связан с антиоксидантными свойствами гемоксигеназы (HO-1), получаемой при помощи установки для нейронной радиографии Nrf2 с применением Пикеатаннола.
Укрепление сердечнососудистой системы
Эндотелий
Известно, что Пикеатаннол в концентрациях EC50 2.4+/-0.4мкM вызывает расслабление изолированной раздраженной адреналином ткани аорты (в концентрации 1мкM ткань расслабляется на 20%),46) а это свидетельствует о том, что Пикеатаннол в данном случае эффективнее других стильбенов (ресвератрола и дезоксирапонтигенина в концентрациях EC50 28.6мкM и 18.5мкм) и дистильбен ε-виниферина (EC50 8.4+/-1.7мкм). Расслабляющее действие Пикеатаннола распространялось на эпителий и блокировалось L-нитро-аргинин-метил-эфиром, предположительно, оба эффекта связаны с производством в клетках окиси азота. При пероральном употреблении, Пикеатаннол вызывает расслабление напряженных кровеносных сосудов, что, вероятно, связано с метаболизмом окиси азота. Известно, что под воздействием фактора роста тромбоцитов, клетки гладкой мускулатуры аорты способны размножаться при активизации тирозин киназы селезенки47) и PI3K, оба из которых являются «мишенями» Пикеатаннола. Вследствие паталогического размножения клеток гладкой мускулатуры при атеросклерозе (вследствие утолщения интимы аорты),48) считается, что вещества, препятствующие размножению, обладают терапевтическим эффектом. Ученые приписывают Пикеатаннолу антисклеротические свойства, обусловленные его способностью замедлять процесс утолщения стенок аорты, хотя механизмы действия данного вещества при пероральном употреблении еще недостаточно изучены.
Кровоток
Существует фермент под названием аргиназа, расщепляющий L-аргинин до L-орнитина, а его разновидность (Аргиназа II, которая существует вне печени, тогда как аргиназа I развивается внутри печени и фагоцитов49)) можно назвать новой «мишенью» терапевтов при лечении сердечно-сосудистых заболеваний, ведь по запасам аргинина и способности его блокировать в кровотоке, аргиназу можно поставить в один ряд с эндотелиальной синтазой оксида азота 50). Известно, что активность фермента (аргиназы II) усиливается при воспалениях (эндотоксин[65]), окислительных процессах (образовании липопротеидов низкой плотности51)) и кислородном голодании (гипоксии52)) в эндотелии. Учеными было отмечено, что астрингин (гликозид Пикеатаннола) блокирует аргиназу I (25-38% при концентрации 1-10мкм в клетках мышиной печени, IC50 при 11.22мкм) и аргиназу II (25-47% при концентрации 1-10мкм в клетках мышиных почек, IC50 при 11.06мкм53)) , не проявляя при этом свои селективные свойства. Это стало причиной повышенной био-доступности окиси азота в живых организмах и на животных моделях в эндотелии атерогенных мышей ApoE-/-.54) Однако, одного только исследования агликона (Пикеатаннола) было недостаточно, чтобы доказать какое-то значительное влияние данного стильбена на деятельность и экспрессию генов аргиназы в живых организмах.55) Способность Пикеатаннола блокировать развитие аргиназы в эндотелии играет важную роль в терапии, поддерживая кровоток, но той концентрации, в которой Пикеатаннол попадает в кровь человека, явно недостаточно для этого. Гликозид Пикеатаннола под названием астрингин обладает терапевтическим эффектом, но наиболее вероятно, что в ходе метаболизма после перорального употребления он большей частью превращается в Пикеатаннол и, таким образом, его концентрация в крови не достигает необходимого уровня. Ассиметричный диметиларгинин (ADMA), производная белка диметиларгинин диметиламиногидролазы (DDAH) 56) ,является эндогенным ингибитором окиси азота; иногда данный белок становится более активным во время оксидативного стресса, что приводит к блокировке окиси азота и производству ею меньшего количества сигналов. Терапевты стремятся нормализовать уровень ассиметричного диметиларгинина в крови, иначе он может вызывать различные паталогии.57) В эндотелиальных клетках с высоким содержанием глюкозы, Пикеатаннол (1мкM) показывает хорошие результаты в поддержании деятельности диметиларгинин диметиламиногидролазы, независимо от селективной радиотерапии 1 и несмотря на отсутствие блокирующих свойств (при обычной концентрации глюкозы в крови), благодаря чему Пикеатаннол нормализует концентрацию ассиметричного диметиларгинина в крови. Подобными свойствами обладает и ресвератрол, хотя для эффективности его концентрация должна быть в 10 раз больше (10мкM). Независимость от селективной радиотерапии 1 доказывает тот факт, что дегидроксильные аналоги ресвератрола эффективны, по-видимому, при ее проведении,58) и на основании этого можно утверждать, что действие Пикеатаннола напрямую связано с тремя изолированными радикалами (т.к. его потенциальные антиоксидантные свойства относятся к гидроксильным группам и они более выражены, чем у ресвератрола59)). И хотя механизмы действия Пикеатаннола при пероральном употреблении крайне мало изучены, препарат, вероятно, способствует снижению концентрации ассиметричного диметиларгинина в крови и способен оказывать защитное действие на кровоток во время оксидативных стрессов (напр., при перенапряжении сосудов и диабете). Ресвератрол обладает теми же свойствами, но Пикеатаннол в таких случаях эффективнее. Механизм действия Пикеатаннола непосредственно связан с его антиоксидантными свойствами, таким же, как и у любого другого эффективного лекарственного препарата-антиоксиданта. В изолированных клетках человеческого эндотелия (EA.hy926) 50мкM Пикеатаннола способны инкубироваться вплоть до 9 часов, благодаря чему укрепляютя РНК-молекулы эндотелиальной синтазы окиси азота и увеличивается количество белков в крови, тогда как Пикеатаннол в концентрации 20мкM эффективен в течение 48 и более часов.60) Подобная яркая экспрессия эндотелиальной синтазы окиси азота связана с увеличением доли ее фосфорилирования на 30% , что необходимо (в Ser-1177) для деятельности самого белка. Ученые не уверены, играет ли здесь роль пероральное употребление Пикеатаннола, потому что, хотя в ходе вышеописанного исследования была доказана польза препарата при пероральном употреблении в концентрациях 20-50мкM и установлено, что ресвератрол менее эффективен в данном случае; последний начинал активно действовать при крайне низкой концентрации 50нM в ЭКПВЧ в виде сигналов рецепторов эстрогена61); известно, что Пикеатаннол сохраняет свою эффективность и в низких концентрациях 62) , вызывая расслабление (1мкM) при блокировке его L-нитро-аргинин-метил-эфиром.63) Пикеатаннол, подобно ресвератролу, способствует повышению активности эндотелиальной синтазы окиси азота на фоне сигналов эстрогена, хотя нет полной уверенности в том, что препарат сохраняет эти свойства при пероральном употреблении человеком. Исходя из активных концентраций ресвератрола и похожих потенциальных возможностей обоих стильбенов, это кажется правдоподобным.
Тромбоциты
Опыты с Пикеатаннолом не показали, что препарат способен блокировать образующийся под действием коллагена или арахидоновой кислоты конгломерат тромбоцитов (до 3,000мкм), несмотря на то, что метоксилированные стильбены (рапонтигенин и дезоксирапонтигенин) потенциально эффективны в концентрациях от 20 до 100мкм. Пикеатаннол не оказывает значительного воздействия на тромбоциты.
Воспаления и иммунология
Макрофагациты
Если говорить об активизации макрофагоцитов, то Пикеатаннол считается более эффективным средством в борьбе с воспалениями, чем ресвератрол, судя по секреции TNF-альфа-превращающего фермента и рецептора интерлейкина-1. Это связано с индукцией гемоксигеназы-1 в макрофагоцитах молекулы гидроксильной группы, поскольку аналог ресвератрола с отсутствием гидроксильной группы молекул не способен продуцировать гемоксигеназу-1.64)
Лаброциты
Пикеатаннол способен блокировать сигналы Fcϵ-рецептора-1 в лаброцитах на фоне торможения белка Syk – одного из двух белков (второй белок Lyn), создающих помехи на пути сигналов этого рецептора.65) Действие Пикеатаннола зависит от его концентрации (5-50мкг/мл), в концентрациях 50мкг/мл (выделение серотонина из антигена) и 100мкг/мл (выделение гистамина) он блокирует практически все сигналы вышеупомянутого рецептора и по статистике в концентрации 30мкм препятствует выделению лейкотриенов и гистамина, хотя более низкие концентрации считаются неэффективными.
Нейтрофилы
Пикеатаннол считается более эффективным, чем птеростильбен, в подавлении раздраженных PMA нейтрофилов (судя по активизации протеин киназы C) в концентрациях 10-100мкм, тогда как в более низких концентрациях действует подобно ресвератролу.66)При хемилюминисцентном иммуно-анализе группы перикисных радикалов, Пикеатаннол показал себя как наиболее активный из всех стильбенов с концентрацией полумаксимального ингибирования 600нM (6.2% ингибируется при 100нM, 66% при 1мкм, максимум 99.3% при 10мкм).
Реакции с гормонами
Эстроген
Учеными было отмечено, что Пикеатаннол активирует альфа-группу рецепторов эстрогена (ERα) и, подобно самому эстрогену, способен прикрепляться к этому рецептору, при этом агонизм наблюдается в концентрации 10нM (в данном случае эффект от Пикеатаннола сравним с действием мирицетина67)) и препарат более близок по химическим свойствам к ERα, чем к ERβ. Пикеатаннол представляет собой эстроген растительного происхождения, но пероральное употребление препарата на практике не дает нам точной информации о том, каким эффектом чаще обладает Пикеатаннол – эстрогенным или анти-эстрогенным, связывая эстрогены.
Периферийные системы органов
Глаза
 Когда крысам в преддверии воспалительного инсульта внутривенно вводили 30мг/кг Пикеатаннола (ЛПС-инъекция) либо за 2 часа до, либо через час после наступления инсульта, препарат показал себя как эффективное средство по борьбе с воспалительными изменениями,68) в частности, предотвращая увеит (воспаление сосудистой оболочки глазного яблока).
Когда крысам в преддверии воспалительного инсульта внутривенно вводили 30мг/кг Пикеатаннола (ЛПС-инъекция) либо за 2 часа до, либо через час после наступления инсульта, препарат показал себя как эффективное средство по борьбе с воспалительными изменениями,68) в частности, предотвращая увеит (воспаление сосудистой оболочки глазного яблока).
Противораковые свойства Пикеатаннола
Принципы действия
Ученые изучают Пикеатаннол на предмет антираковых свойств не только с точки зрения пищевой добавки, но и как метаболит ресвератрола на фоне деятельности гена CYP1B1. Известно, что раковые клетки перенасыщены этим геном, по сравнению со здоровыми клетками69), а пролекарственные препараты (слабоактивные или неактивные до начала метаболизма), чувствительные к CYP1B1, считаются потенциальными противораковыми препаратами.70) Вероятно, гипотетически Пикеатаннол является противораковым метаболитом ресвератрола и полезные свойства первого, описанные ниже, относятся также к некоторым функциям ресвератрола. Ангиогенез (производство новых кровеносных сосудов) – это процесс, характерный для роста опухолей, и если он обусловлен эндогенными факторами (ангиотензин, фактор роста сосудистого эндотелия), то он частично затухает, когда малая энтерферирующая РНК поглощает тирозин киназу селезенки или ее блокирует Пикеатаннол (в концентрации 5мкM).71) Пикеатаннол не влияет на действие этих факторов на рецептор (VEGFr1/Flt-1), который, как известно, активизирует тирозин киназу селезенки через p38/c-Src.72) Активизация тирозин киназы селезенки (вследствие включения основного рецептора VEGFr1) положительно влияет на процес ангиогенеза. Блокируя Syk, Пикеатаннол тормозит этот процесс.
Простата
На фоне активизации нитро-хинолин-оксида-2, Пикеатаннол препятствует разрастанию раковых клеток в простате (CWR22Rv1) и, благодаря высокому содержанию в раковых клетках белка, который в ходе метаболизма превращает ресвератрол в пицетонол (CYP1B1) 73), ученые считают последний биологически активным метаболитом ресвератрола. В живых организмах Пикеатаннол препятствует разрастанию раковых клеток предстательной железы LNCaP в концентрации полу-максимального ингибирования 31.7мкм, будучи при этом менее эффективным, чем птеростильбен (22.9мкм) и ресвератрол (12.7мкм);74) наиболее эффективным считается синтетический 3-метилоксоресвератрол (2.5мкм). Противораковое действие этих препаратов распространяется раковые клетки простаты Du145 и PC3M. Способность Пикеатаннола активизировать нитро-хинолин-оксид-2 (на фоне активизации Nrf2) играет важную роль при лечении простатита. При пероральном употреблении 50мг/кг Пикеатаннола мышами раз в два дня на протяжении двух недель до появления опухоли (раковых клеток предстательной железы LNCaP) и в течение последующих пяти недель развитие опухоли замедлилось (так же, как при пероральном употреблении 50мг/кг ресвератрола. Несмотря на свою эффективность, в конце эксперимента Пикеатаннол не был обнаружен ни в кровяной сыворотке мышей, ни в самой опухоли (в отличие от ресвератрола, который в небольших концентрациях присутствовал как в сыворотке, так и в раковой опухоли), однако было зафиксировано снижение уровня ИЛ-6 в сыворотке. Противораковые свойства Пикеатаннола (в отношении рака простаты) при пероральном употреблении похожи на свойства ресвератрола.
Лейкемия
Фактор некроза опухолей альфа (ФНО-α) имеет как положительные (противораковые цито-токсические препараты), так и отрицательные (развитие воспаления) свойства, его важно блокировать при лечении некоторых видов рака, вызванных воспалительными процессами. ФНО-α может существовать как в форме раствора, так и на мембране, и поскольку во втором случае чаще активируется один из его рецепторов (РФНО-275)) вследствие шеддинга ФНО-α из мембраны, и здесь ключевую роль играют несколько белков, наиболее важный из которых - ADAM17.76) Ученые отмечают, что в изолированных (лейкемических) клетках Пикеатаннол (1мкM в течение 8-24 часов) способствует сокращению выделения ФНО-α и блокирует ядерный фактор «каппа-би».77) Такой вроде бы противовоспалительный эффект связан с супрессией белка ADAM17 (который способствует активизации ядерного фактора «каппа-би»), что напрямую связано с повышением уровня белка β-TrCP и ведет к деградации Sp1 (связующего звена между ADAM17 ядерным фактором «каппа-би»78)); другими словами, β-TrCP мешает ADAM17 активировать ядерный фактор. Увеличение запасов β-TrCP также связано с меньшим количеством сигналов гена FOXp3 (и его производной miR-183) вследствие блокировки протеин киназы B/мишени Рапамицина в клетках млекопитающих. Пикеатаннол не оказывает непосредственного воздействия на иРНК белка β-TrCP, а повышенное содержание белка связано со снижением содержания miR-183 (разлагающего β-TrCP79)). В лейкемических клетках KBM-5 Пикеатаннол в концентрации 50мкM блокирует сигналы ядерного фактора «каппа-би» (обусловленного не обязательно наличием протеина киназы B/мишени Рапамицина в клетках млекопитающих),80) и действие Пикеатаннола в данном случае, возможно, подчиняется тем же механизмам, поскольку здесь задействованы молекулы межклеточной адгезии JCaM-1, которым не хватает тирозин киназы селезенки и p56Ick (других механизмов действия Пикеатаннола) и которые не снижают эффективность 50мкM Пикеатаннола. Ингибирование сигналов протеин киназы B/мишени Рапамицина в клетках млекопитающих может быть связано либо с непосредственно блокировкой PI3K Пикеатаннолом, либо чисто с удалением белка ADAM17.81) Учеными отмечена способность Пикеатаннола усиливать апоптоз, вызываемый цитокином семейства факторов некроза опухоли, лигандом82), а также, наряду с механизмами саморазрушения, повышать эффективность цитарабина. Действие Пикеатаннола в лейкемических клетках задействует в них механизмы саморазрушения, что является следствием сокращения ФНО-α, высвобожденного из клеточной мембраны и, таким образом, препятствуя возможности воздействовать на рецептор ФНО-α (главным образом на TNRF2) и напрямую влияя на образование сигналов выживания клетки (ядерный фактор «каппа-би»). Это может быть вызвано блокировкой сигналов протеин киназы B/мишени Рапамицина в клетках млекопитающих, хотя принцип действия (будь то ингибирование сигналов ADAM17 или PI3K) не установлен. Вышеперечисленные механизмы (ADAM17 связывал сигнальные пути протеин киназы B) запускают апоптоз клеток U937[101] и других раковых клеток, а Пикеатаннол, как было отмечено, способствует повышению эффективности бета-1-глобулина Sp1 (который отличается от вышеупомянутого бета-2-глобулина Sp2), а также эффективности внешне-регулируемой киназы, в результате чего рецептор DR5 становится более экспрессивным и усиливается апоптоз, вызываемый цитокином семейства факторов некроза опухоли, лигандом (в клетках THP-1);83) в клетках U937 и других раковых клетках, Пикеатаннол (в концентрации 5мкM) способен блокировать активность внешне-регулируемой киназы (действие, противоположное эффекту в клетках THP-1), но все равно инициирует апоптоз раковых клеток, повышая уровень содержания иРНК и белков в Fas и FasL (на фоне сигналов киназы МАР-киназ p38 MAPKs,84) влияющих на c-Jun и ATF-2[105]), которые, наряду с DR5 и TRNF1, содействующими апоптозу раковых клеток, относятся к другому классу рецепторов смерти 85). Учеными была подтверждена способность Пикеатаннола в концентрации 5мкM, сокращать срок жизни лейкемических клеток до 48% спустя 24 часа после инкубационного периода. Различия между определенными рецепторами смерти (DR5 и Fas) способствуют повышению уровня цитотоксичности веществ, сигналы которых передавались бы по этим рецепторам, что не противоречит механизмам саморазрушения раковых клеток под действием Пикеатаннола. Пикеатаннол сам по себе способен сокращать жизненный цикл этих клеток, предполагая повышенную восприимчивость к эндогенным веществам (которые вырабатываются раковой клеткой для сдерживания своего же роста). Эффективность пицетамола в борьбе с лейкемией до сих пор не обоснована наукой.
Эстетическая составляющая
Влияние на кожу
Изолированный Пикеатаннол способен, в зависимости от концентрации, блокировать синтез меланина, начиная с концентрации 4.5мкM в клетках MNT-1 (блокировка менее 20% меланина) и ингибируя до 30% в концентрациях выше 20мкM; в низких концентрациях Пикеатаннол оказался эффективнее ресвератрола (когда ресвератрол не действовал, Пикеатаннол проявлял себя в концентрации полумаксимального ингибирования 1.5386)), и если по результатам одного исследования эффективность обоих препаратов в концентрации 20мкM считали одинаковой, то в ходе другого эксперимента было доказано, что Пикеатаннол в концентрации полумаксимального ингибирования был в 41 раз менее эффективным, чем ресвератрол. Блокировка синтеза меланина связана с антиоксидантными свойствами и повышенным содержанием глютатиона в Пикеатанноле. Пикеатаннол в концентрации 5мкM ускоряет синтез коллагена (приблизительно на 30%) и в данном случае считается эффективнее ресвератрола, хотя оба вещества сравнивали в концентрации 10мкM, и синтез коллагена в этом случае протекал на 50% быстрее, однако в концентрации 20мкM ни тот, ни другой не действовали. Пикеатаннол максимально эффективен (по сравнению с ресвератролом), когда речь идет о стимуляции синтеза коллагена и блокировке меланогенеза (процесса, благодаря которому наша кожа загорает), препарат эффективен даже в малых концентрациях, в которых ресвератрол не действует совсем. Что касается защиты от УФ-излучения, содержащийся в семенах мараккуйи Пикеатаннол (в также сирпузин B – гетеродимер пары Пикеатаннол - ресвератрол) обладает защитным эффектом, повышая уровень глютатиона в крови, в зависимости от концентрации (0.25-2мкг/мл, с лучшими индукционными свойствами в концентрации 2мкг/мл), и тем самым замедляя окислительные процессы в коже, вызванные УФ-лучами спектра Б (0.5-2мкг/мл). Индукция глютатиона, как и снижение концентрации раковых клеток MMP-1, наблюдались независимо от присутствия УФБ-излучения (которое, тем не менее, влияет на скорость окислительных процессов в коже, вызываемых им же). Из вышесказанного следует, что Пикеатаннол в концентрациях, релевантных при пероральном употреблении, защищает клетки кожи от вредного солнечного излучения, однако механизмы действия Пикеатаннола при пероральном употреблении до сих пор не изучены.
Помощь при лечении заболеваний
Болезнь Альцгеймера
 При лечении болезни Альцгеймера Пикеатаннол действует подобно ресвератролу, то есть обе молекулы прикрепляются к транспортному белку транстиретину (TTR) на связующем участке тирозина. TTR является транспортным белком, который обычно присутствует в тетрамерах (четырехзвенных полимерах), но способен распадаться на мономеры (однозвенные полимеры), которые способствуют образованию комплексов белков (амилоидов).87) Любая небольшая молекула, которая прикрепляется к тетрамеру, способна стабилизировать его, предотвращая его распад на мономеры; благодаря данному свойству, Пикеатаннол обладает терапевтическим эффектом.
Помимо этого, TTR сам по себе (независимо от веществ, которые он транспортирует) способен прикрепляться к амилоидным пептидам, тем самым препятствуя образованию более крупных комплексов белков88), и как ресвератрол, так и Пикеатаннол (а также и другие фенольные полимеры, такие как катехины, содержащиеся в зеленом чае) играют важную роль в повышении уровня TTR в клетках, воздействуя на рецепторы нано-молярного ряда.89)
Считается, что при ежедневном употреблении внутрь, Пикеатаннол, вступая в реакцию с транс-тирезином в клетках, обладает рядом защитных свойств, препятствующих развитию болезни Альцгеймера.
При лечении болезни Альцгеймера Пикеатаннол действует подобно ресвератролу, то есть обе молекулы прикрепляются к транспортному белку транстиретину (TTR) на связующем участке тирозина. TTR является транспортным белком, который обычно присутствует в тетрамерах (четырехзвенных полимерах), но способен распадаться на мономеры (однозвенные полимеры), которые способствуют образованию комплексов белков (амилоидов).87) Любая небольшая молекула, которая прикрепляется к тетрамеру, способна стабилизировать его, предотвращая его распад на мономеры; благодаря данному свойству, Пикеатаннол обладает терапевтическим эффектом.
Помимо этого, TTR сам по себе (независимо от веществ, которые он транспортирует) способен прикрепляться к амилоидным пептидам, тем самым препятствуя образованию более крупных комплексов белков88), и как ресвератрол, так и Пикеатаннол (а также и другие фенольные полимеры, такие как катехины, содержащиеся в зеленом чае) играют важную роль в повышении уровня TTR в клетках, воздействуя на рецепторы нано-молярного ряда.89)
Считается, что при ежедневном употреблении внутрь, Пикеатаннол, вступая в реакцию с транс-тирезином в клетках, обладает рядом защитных свойств, препятствующих развитию болезни Альцгеймера.
:Tags
Читать еще: Айяуаска , Никтурия , Ремерон (Миртазапин) , Триоксален (Тризорален) , Эшшольция калифорнийская ,










