Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Эводия (эводия лекарственная)
 Используется в традиционной китайской медицине для повышения тепла тела. Вероятно, может функционировать в качестве жиросжигателя, но исследования на эту тему не выявили значительной эффективности действия; может снизить восприятие холода как капсаицин, который опосредованно повышает тепло тела. Рекомендуется употреблять вместе с кашей зимой.
Используется в традиционной китайской медицине для повышения тепла тела. Вероятно, может функционировать в качестве жиросжигателя, но исследования на эту тему не выявили значительной эффективности действия; может снизить восприятие холода как капсаицин, который опосредованно повышает тепло тела. Рекомендуется употреблять вместе с кашей зимой.
Основная информация
Эводия кожистосемянная – это растение, которое плодоносит ягодами (плоды эводии). Эти ягоды согласно традиционной китайской медицине следует употреблять в пищу, чтобы согреться. Растение смягчает боли, оказывает лечебное воздействие при желудочно-кишечных расстройствах, а также обладает противораковыми свойствами. Изучалось его воздействие в качестве жиросжигателя, но на сегодняшний день значительной эффективности отмечено не было. Оно заставляет ощущать животных жар в теле, но этот эффект достигается увеличением расходов тепла (эффект жиросжигания) и снижением восприятия холода посредством агониста TRPV1, эффект схож с действием экстракта капсаицина из красного перца. Сочетание заставляет чувствовать тепло в теле, но не сильно повышает расход калорий. Два исследования на животных продемонстрировали свойства, способствующие борьбе с ожирением, но они не связаны с тепловым эффектом плодов эводии, и это совсем не означает, что ягоды оказывают жиросжигающий эффект. Помимо всего прочего, растение демонстрирует многообещающее противораковое действие, достигаемое с помощью уникального механизма. Но его употребление в качестве добавки ограничено, так при извлечении активных ингредиентов (эводиамин, рутакарпин) и помещении их в капсулу резко снижается пероральная биодоступность веществ. Изолированные вещества могут быть бесполезны вне толстой кишки и желудка, для достижения эффекта, необходимо, чтобы ягоды или этанольный экстракт ягод достиг крови в необходимом количестве.
Что следует знать
Также известна как: Учжуюй, У Чжу Юй, У Чжу Юй Тан, Плоды Эводии, Эводия Рутоплодная, Эводия Кожистосемянная, Evodia Fructae
Не путать с: Эводиамином (биоактивное вещество), Рутакарпином (биоактивное вещество)
Следует отметить:
- Изолированные эводиамин и рутакарпин плохо всасываются; это не проблема, если целью является желудок или толстый кишечник (пищеварение), но для доставления веществ в кровь необходимо использовать целые плоды эводии или этанольный экстракт плодов
Используется:
- как жиросжигатель
- в традиционной китайской медицине
- как ягода для еды
Хорошо сочетается с:
- корневищем коптиса китайского (усиливает всасываемость эводии)
Не сочетается с:
- корневищем коптиса китайского (усиливая всасываемость эводии, всасываемость самого коптиса резко падает)
- кофеин; рутакарпин (соединение эводии) повышает скорость метаболизма кофеина и снижает его воздействие на организм
Эводия лекарственная: инструкция по применению
На сегодняшний день не было проведено ни одного исследования ягод эводии лекарственной с участием человека. Традиционное использование предполагает приготовление отвара из 3-9 г ягод, который затем делят на два приема (утром и вечером) или три приема (утром, днем и вечером).
Источники и структура
Источники
Эводия лекарственная, высушенные незрелые ягоды, также известные как у чжу юй (учжуюй), или плоды эводии используются в традиционной китайской медицине в количестве 3-9 грамм (ягод) три раза в день для повышения тепла тела, кишечного комфорта (в частности смягчении боли в животе, устранение кислотной отрыжки, лечение тошноты и диареи),лечения дисменореи и для борьбы с воспалением и инфекцией.1) Часто используется в сочетании добавкой, которая носит название «у чжу юй тан», в состав которой входят плоды эводии, зизифус настоящий, женьшень обыкновенный (в соотношении 1:1:1) и корень имбиря (каждый из компонентов в двойном размере), принимается в виде отвара при гипертензии. Для лечения желудочно-кишечных расстройств используется добавка «цзо цзинь вань», в ее состав входит эводия и корневище коптидиса в соотношении 1:6. Также в лечебных целях применяется отвар «фань цзо цзинь вань, в состав которой входят эводия и корневище коптидиса в обратном соотношении. При употреблении у чжу юй тан традиционным способом рекомендуемое количество потребляемого рутакарпина составляет 16 мг каждый день (из расчета, что средняя доза потребления ягод составляет 9г три раза в день) и немного более высокий уровень эводиамина.2) Традиционно употребляется в холод; поднимает тепло тела, благотворительно воздействуя на желудок и кишечник. Оказывает противораковое действие.
Структура
- Рутакарпин и его метаболит 10-гидроксирутакарпин (а также гликозид рутакарпина - рутакарпин-10-O-рутинозид), являются формами другого основного квиназолинокарболинового алкалоида. Содержится в количестве 0.15-0.55% в ягодах эводии.
- Другие квиназолинокарболиновые алкалоиды, такие как вухуин и ретсинин 4) и эводиамин, обычно в количестве 0.005-0.08%, но в некоторых растениях содержится в более высоком количестве 0.4-0.6%
- Хинолиновые алкалоиды, такие как эвокарпин, дигидроэвокарпин, 1-метил-2-н-нонил-4(1H)хинолон,[ а также большое количество (17+) других5)
- Учжуюямид -I в небольшом количестве (0.00003%) и учжуюямид -II, соединения, схожие по структуре на эводиамин и рутакарпин 6)
- Флавоноиды и гликозиды флавоноида, такаие как изорамнетин-7-O-рутинозид и диосмеин-7-O-β-d-глюкопиранозид
- Ацилглюконовые кислоты, такие как трансферулилглюконовая кислота и транс –кофеилглюконовая кислота, 0.00003% и 0.0006% плода соответственно (могут быть изолированы в метан-этанольном экстракте)
- Лимоноидные соединения, такие как лимонин (не путать с лимоненом), а также эводирутанин, эводол и шихулимонин A7)
- Мио-инозитол, 8 г на 299,5 г образца (2%)
- Дибутиловый эфир фталевой кислоты, 8 г на 299,5 г образца (низкое количество)
- Эфирные масла β-пинена (72.82%), 1R-α-пинена (8.90%) и β-мирцена (1.99%)8)
Основными соединениями являются квиназолинокарболиновые алкалоиды, эводиамин и рутакарпин (термины происходят от названия растения). Флавоноиды, лимоноиды и другие алкалоиды также могут быть биоактивными, как и инозитол. Содержание основных биоактивных веществ достаточно низкое.
Структура
Ниже представлены два основных биоактивных соединения эводии лекарственной.9) Несмотря на схожий механизм действия с капсаицином (экстракт красного перца), изолированный эводиамин не обладает ни характерным вкусом, ни остротой.
Фармакология
Показатели сыворотки крови
После перорального приема 12 г/кг отвара у чжу юй (эводия, зизифус настоящий, женьшень обыкновенный в соотношении 1:1:1 и корень имбиря в двойном размере любого из компонентов; этанольный экстракт), из которого 2,4 г/кг приходится на этанольный экстракт эводии, были обнаружены следующие параметры для соединений эводии:
- Период полураспада эводиамина составляет 0.93 ± 0.45 часов, Tmax 1.49 ± 0.22 часа, Cmax 19.52 ± 8.17 мкг/мл и ППК 71.27 ± 15.52 мкг/ч/мл. Другое исследование показало, что Cmax составляет 49 ± 19 мкг/мл после приема 500 мг/кг изолированного эводиамина,10) первое исследование определяет биодоступность эводиамина в 0.1%, тогда как во втором случае она немного выше. Исследование, использующее этанольный экстракт эводии, отметило, что 40 мг/кг (30% эводиамина, то есть 14 мг/кг) имеют Cmax 164.8 ± 65.1 мкг/мл; это говорит о том, что в 35,7 раз меньшая дозировка этанольного экстракта ягоды имеет максимальную концентрацию вещества в крови в 3.36 раз выше. Tmax во всех исследованиях варьируется от 30 до 60 минут.
- Период полураспада рутакарпина составляет 0.98 ± 0.39 часов, Tmax 1.26 ± 0.23 часа, Cmax 13.46 ± 7.03 мкг/мл и ППК 62.44 ± 18.85 мкг/ч/мл. Другое исследование продемонстрировало более низкую биодоступность изолированного рутакарпина (концентрация 2.4 ± 3.0 нг/мл через 30 минут после 40 мг/кг лекарственного сырья), но при использовании рутакарпина в виде твердой дисперсии способствует повышению концентрации вещества в крови в 7,5 раз (до 18.1 ± 1.8 нг/мл). Наноэмульсии также демонстрируют повышение скорости абсорбции.11) Базовая концентрация этанольного экстракта у чжу юй из (недозрелых) ягод (40% пероральной дозы 40 мг/кг, то есть 16 мг/кг) достигает 215.3 ± 80.4 мкг/мл в крови крыс. Улучшения биодоступности рутакарпина схожи с эводиамином, так как пероральная доза в 2,5 раза ниже достигает концентрации вещества в 89,7 раз выше при приеме этанольного экстракта концентрированных ягод. Как и в случае с эводиамином Tmax во всех исследованиях составляет 30-60 минут независимо от Cmax.12)
- Период полураспада дегидроэводиамина составляет 0.79 ± 0.21 часов, Tmax 1.07 ± 0.15 часов, Cmax 7.64 ± 0.63 мкг/мл и ППК 12.39 ± 2.71 мкг/ч/мл. Изолированный дегидроэводиамин обладает лучшей биодоступностью (у крыс в среднем 15.35%). По меньшей мере, одно исследование изучало дегидроэводиамин и его циркулирующий уровень в крови в сочетании с другими растениями, сочетание эводии с корневищем коптиса ( соотношение 1:6, сочетание, известное как цзоцзиньвань) сохраняет Tmax (1.6 изолированное вещество, 1.8 часов в форме цзоцзиньвань), но повышает Cmax в 2.66 раза (с 15,383 ± 7166 до 40,992 ± 21,052), снижая Tmax (с 3.5 ± 3.0 до 1.5 ± 1.1), что вызывает повышение ППК на 174% (с 68,134 ± 19,162 до 186,715 ± 39,211).
Три основных компонента эводии лекарственной сильно взаимодействуют с другими растениями, всасываемость и циркулирующий уровень в крови выше в том случае, если используется целая эводия, а не изолированный компонент, при использовании в сочетании с другими отварами традиционной китайской медицины всасываемость и циркулирующий уровень становятся еще выше. Если целью является достижение веществ крови, то нет смысла использовать изолированный эводиамин и рутакарпин из-за плохой биодоступности, и наоборот, если целью является достижение толстой кишки.
- 10-гидроксирутакарпин имеет значение Cmax 0.76 ± 0.16 мкг/мл, Tmax 0.50 ± 0.25 и ППК 9.32 ± 2.93 мкг/ч/мл, период полураспада зафиксирован не был.
- 1-метил-2-н-нонил-4(1H)квинолон имеет значение Cmax 3.16 ± 1.28 мкг/мл при Tmax 0.77 ± 0.15 часа, ППК 9.83 ± 1.51 мкг/ч/мл и период полураспада 2.18 ± 0.47 часов.
- Период полураспада эвокарпина составляет 0.53 ± 0.18 часов и Tmax 0.88 ± 0.17 часов, Cmax 11.53 ± 6.97 мкг/мл и ППК 33.66 ± 10.52 мкг/ч/мл.
- Период полураспада дигидрокарпина составляет 0.49 ± 0.21 часа, Tmax 0.79 ± 0.15 часа, Cmax 6.05 ± 2.87 мкг/мл и ППК 16.53 ± 5.79 мкг/ч/мл.
- Период полураспада изорамнетин -7-O-рутинозид составляет 0.67 ± 0.30 часа, Tmax 0.95 ± 0.25 часа, Cmax 2.21 ± 0.32 мкг/мл и ППК 7.54 ± 1.03 мкг/ч/мл.
- Диосметин -7-O-β-d-глюкопиранозид имеет период полураспада 0.95 ± 0.51 часа, Tmax 1.53 ± 0.17 часа, Cmax 1.73 ± 0.51 мкг/мл и ППК 9.41 ± 3.57 мкг/ч/мл.
В целом, все соединения имеют низкую или умеренную биодоступность и сравнительно быструю фармакокинетика. Эводиамин и рутакарпин действительно проявляют благоприятное действие при использовании целых ягод, а не изолированных соединений.
Системное распределение
Эводиамин транспортируется в кровь и распространяется по органам, исследование на крысах обнаружило, что объем распространения составляет 560 мл/кг, а эводиамин и его метаболиты попадают в печень, почки, сердце, легкие и адипозную ткань в концентрации более высокой, чем в плазме крови, в других органах эводиамин попадает в более низкой концентрации, чем в плазме крови.
Распространение в мозге
При изучении дегидроэводиамина в организме крыс было отмечено, что данная молекула преодолевает гематоэнцефалический барьер и попадает в мозг по линейной кинетике.13) Тогда как концентрация вещества в крови крыс составила 4.82 ± 1.55 мкг/мл, концентрация в мозгу - 1.11 ± 0.4 (кора), 0.93 ± 0.24 (гиппокамп), 0.64 ± 0.28 (полосатое тело), 1.13 ± 0.33 (мозжечок), 1.04 ± 0.3 (мозговой ствол) и 1.18 ± 0.18 мкг/г (в других частях). В среднем концентрация дегидроэводиамина в мозгу в 3-4 раза ниже, чем в плазме крови.
Метаболизм и ферментативное взаимодействие
Дегидроэводиамин зависит от P450, циркулирующие метаболиты состоят из пяти глюкуронидов (в одном из исследований два из них были определены как углерод 10 и 11) и одного сульфата (дегидроэводиамин-12-сульфат) у свободно движущихся крыс. Рутакарпин метаболизируется в основном цитохромом P450 1A2 (ароматаза) в позиции углерод- 10, 11 и 12,14) а также метаболизируется в 3, 10, 11 или 12-гидроксирутакарпин. Метаболизирование в 3- и 10- гидроксирутакарпин подавляется кетоконазолом, это говорит о том, что метаболизм происходит с помощью CYP3A4; два других метаболита (11- и 12-гидроксирутакарпин) метаболизируются с помощью CYP1A или CYP3A4 и CYP2D6. Любопытно, что метаболит рутакарпина - 10-гидроксирутакарпин, который образуется с помощью CYP3A4, может выступать в роли ингибитор ароматазы, ингибируя CYP1A1 и CYP1A2 (изомеры ароматазы) при значении IC50 2.56 ± 0.04 мкм и 2.57 ± 0.11 мкм соответственно. Ингибирующий потенциал рутакарпина также распространяется на CYP1A2, но продолжительное (3 дня) использование рутакарпина, эводии или у чжу юй тан (свойства которой схожи с эводией) могут вызвать стимулирование CYP1A, что таким образом создает обратный ингибированию эффект. Технически рутакарпин является ингибитором ароматазы, но сравнительно быстро вызывает повышение активности ароматазы. 10-HRT ингибирует CYP1B1 при 0.09 ± 0.01 мкм. На CYP3A4 рутакарпин не оказывает влияния.15)
Выведение из организма
Спустя 24 часа после приема эводиамина 82% эводиамина и его метаболитов выводятся из организма, при этом 23% выводятся через мочу, а остальное количество через кал. При использовании 500 мг/кг дегидроэводиамина большая часть конъюгируется с помощью P450; количество неизмененных метаболитов в моче и кале составляет t 0.5% и 6% пероральной дозы соответственно. Большее количества рутакарпина выводится через кал (~42%) при пероральном приеме, основным мочевым метаболитом является 10-гидроксирутакарпин, который является продуктом взаимодействия рутакарпина и фермента CYP1A2.
Механизм действия
Ваниллоидные рецепторы
Эводиамин является агонистом ваниллоидного рецептора, таким же свойством обладает и экстракт красного перца капсаицин. Эффективность действия эводиамина немного ниже, чем у капсаицина, так как для максимального стимулирования рецепторов in vitro требуется концентрация в три раза выше.16) Через взаимодействие с ваниллоидными рецепторами проявляется болеутоляющее свойство растения.
Влияние на жировую массу и ожирение
Термогенез
Проводились исследования действия эводии лекарственной на жировую прослойку организма, так как традиционно она использовалась как согревающее средство; в китайской литературе имеются ссылки на термогенез. 1-3 мг/кг эводиамина, введенного подкожно натощак, снижают центральную температуру тела на 1C у мышей, для достижения того же эффекта, но после приема пищи мышам требуется 10 мг/кг. Такое же снижение внутренней температуры начиналось с хвоста крыс (индикатор термогенеза) практически сразу. Еще одна возможная способность эводиамина, посредством активации TRPV1, создавать участки терпимые к холоду; гипочувствительность к холоду (пониженная чувствительность к холоду) косвенно увеличивает восприятие холода. Повышение тепла не единственный способ жиросжигающего эффекта эводиамина.17) Эводиамин традиционно использовался для повышения тепла, как было отмечено, эводиамин одновременно повышает выработку тепла и снижает чувствительность к холоду. Но исследования, результаты которых описаны выше, проводились без участия человека.
Влияние на адипоциты
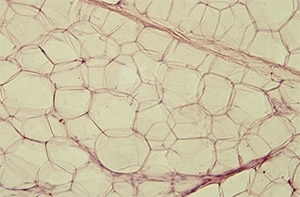 При инкубировании эводиамина в преадипоцитах, он способен активировать каскад MAPK, что снижает инсулин-индуцированное фосфорилирование протекиназы B и активность PPARγ, что таким образом понижает дифференциацию преадипоцитов. Классический механизм действия эводиамина, в качестве агониста рецепторов TRPV1, заключается в снижении дифференциации преадипоцитов; таким образом, могут наблюдаться два схожих механизма действия.
Ингибирование дифференциации преадипоцитов было отмечено и в других исследованиях, наибольшая эффективность была достигнута при концентрации 4 мкм или выше и в исследованиях in vivo при введении посредством инъекций.18) Авторы исследования отметили «негативное взаимовлияние» с инсулиновым сигналом, который искажает эффект эводиамина.
Эводиамин ингибирует дифференциацию преадипоцитов, проявляя эффективное действие при борьбе с ожирением.
При инкубировании эводиамина в преадипоцитах, он способен активировать каскад MAPK, что снижает инсулин-индуцированное фосфорилирование протекиназы B и активность PPARγ, что таким образом понижает дифференциацию преадипоцитов. Классический механизм действия эводиамина, в качестве агониста рецепторов TRPV1, заключается в снижении дифференциации преадипоцитов; таким образом, могут наблюдаться два схожих механизма действия.
Ингибирование дифференциации преадипоцитов было отмечено и в других исследованиях, наибольшая эффективность была достигнута при концентрации 4 мкм или выше и в исследованиях in vivo при введении посредством инъекций.18) Авторы исследования отметили «негативное взаимовлияние» с инсулиновым сигналом, который искажает эффект эводиамина.
Эводиамин ингибирует дифференциацию преадипоцитов, проявляя эффективное действие при борьбе с ожирением.
Исследования
Исследование, в ходе которого мыши получали 0,03% эводиамина и 1,35% экстракта эводии (что приблизительно соответствует 0.02% эводиамина) в течение 21 дня в сочетании с диетой, способствующей ожирению, показало отсутствие какого-либо различия с контрольной группой, но отмечалось снижение жировой массы мышей (уменьшение на 28% периренального жира, уменьшение на 11% жира в придатках яичника), снижение веса (-10.3% по сравнению с контрольной) и повышение термогенеза; все это говорит о действии эводиамина для борьбы с ожирением. Другое исследование, в котором испытуемые получали 0,03% эводиамина в течение 6 месяцев, продемонстрировало значительное снижение скорости набора веса (действие против ожирения), такое же эффект сохранялся у нокаутных мышей UCP1, неспособных на выработку тепла от эводиамина. Эводиамин замедляет скорость набора жира у мышей на диете, провоцирующей ожирение, но жиросжигающего эффекта при этом отмечено не было. Выработка тепла с помощью эводиамина может быть не связано с замедлением набора веса.
Воспаление
Эндотелий
При инкубировании эводиамина в эндотелиальных клетках он способен ингибировать ИЛ-1α (при 10 мкм) и секрецию тромбоксана B2 (TXB2) (при 10 мкм) в качестве реакции на воспалительные сигналы (ЛПС), а также снизить уровень E-селектина в эндотелиальных клетках; эффект достигается вне зависимости от дозировки.19)
Макрофаги
Эводиамин и рутакарпин ингибируют выработку PGE(2) в макрофагах, стимулированных ЛПС (провоспалительный сигнал), и в макрофагах под воздействием гипоксии.20) Эводиамин затем предотвращает повышенную регуляцию провоспалительного фермента ЦОГ-2, рутакарпин при этом не проявляет подобного воздействия. Дегидроэводиамин также снижает активность ЦОГ-2 и трансляцию мРНК, а рутакарпин скорее напрямую ингибирует, чем регулирует содержание белка в ферментах ЦОГ, он ингибирует ЦОГ-1 и ЦОГ-2 при значении IC50 8.7мкм и 0.28 мкм соответственно. Еще одно соединение, гошуюамид II, ингибирует 5-липоксигеназу и снижает синтез лейкотриенов.21)
Цитоплазматический сигнал
Сочетание отвара из плодов эводии и отвара из коптиса китайского в соотношении (цзо цзинь вань) in vitro ингибирует транслокацию NF-kB и сигнал AP-1 в клетках печени HepG2 при IC50 >200 и 22.9 мкг/мл для AP-1 и NF-kB. Берберин способен ингибировать AP-1 и NF-kB при значении IC50 9.5 и 50 мкм соответственно, в то время как эводиамин проявляет ингибирующее действие только на AP-1, при этом менее эффективно, чем берберин. Эводиамин ингибирует активацию NF-kB в макрофагах в концентрации 1-10 мкм в качестве реакции на провоспалительные сигналы.
Влияние на рак
Ингибирование топоимеразы
Топоимеразы (I и II) - это ферменты, которые вносят разрывы в нити ДНК, таким образом, ДНК может быть воспроизведено. Когда фенольные нуклеофилы атакуют 3' конец ДНК, образуется раскрученное ДНК, что образует связь с Tyr723 на ферменте TopoI; после атаки 5' ДНК два конца вновь соединяются в ходе процесса, известного как повторное лигирование. В процессе репликации ДНК топоизомераза I придерживает 3' конец на некоторое время.22) Ингибиторы топоизомеразы I могут предотвратить повторное лигирование ДНК и вызывают цитотоксичность (гибель клеток); что достаточно хорошо, так как раковые клетки гибнут намного быстрее, чем обычные клетки. Эводиамин имеет значение IC50 6.02 мкм в раковых клетках груди MCF-7, которые активируют высокий уровень топоизомеразы I, при этом цитотоксичность немного ниже, чем у кампотецина. Эводиамин предотвращает лигирование ДНК в зависимости от концентрации, механизм действия схож с кампотецином (создается комплекс из топоизомеразы I и нити 3' ДНК). Эводиамин проявляет цитотоксичность в раковых клетках груди в других исследованиях, в раковых клетках устойчивых к адриамицину эводиамин индуцирует смерть клеток in vitro и in vivo, при этом эффективность действия выше, чем у паклитаксела. Эводиамин является двойным каталитическим ингибитором топоизомеразы I и II, проявляет эффективное воздействие против клеток, резистентных к более мощному ингибитору топоизомеразу I (кампотецин), не вызывает повреждение ДНК.23) Флавоноид эводиамина также обладает двойным ингибирующим потенциалом. Действие, посредством которого плоды эводии могут демонстрировать противораковое действие; необходимы дальнейшие исследования для изучения общего клинического значения, но двойное ингибирующее действие выглядит очень многообещающим.
Апоптоз
Апоптоз, или процесс клеточной гибели, важный биомаркер при раковой терапии. Соединения эводии индуцируют апоптоз в раковых клетках желудка (SGC-7901) и (N-87), раковых клетках груди (MCF-7)24)и (NCI/ADR-RES), раковых клетках печени (HepG2), клетках лейкемии (HL-60) (THP-1) и (U937), клетках легких (H-460) и (LLC), толстой кишки (COLO-205), щитовидной железы (ARO),25) меланомы (A375-S2), и (B16-F10), раковых клетках шейки матки (HeLa), фибросаркомы (L929), проявляет ингибирующее действие in vivo на раковую модель саркома-180 при использовании отвара цзо цзинь вань.26) В большинстве случаев эффект обусловлен действием эводиамина и его метаболитами, хотя в некоторых случаях эффект обусловлен действием флавоноидных гликозидов.
Взаимодействие с питательными веществами
Кофеин
 При использовании рутакарпина (активный индол эводии) значения ППК и Cmax кофеина значительно снижаются; это говорит о том, что рутакарпин снижает воздействие кофеина на организм. Это действие распространяется и на ксантиновое соединение теофиллина. Такой же эффект демонстрирует сама эводия и сочетание отваров, таких как у цзу юй тан.
Данный эффект довольно значителен; предварительное использование 80 мг/кг рутакарпина перорально в течение 3 дней (довольно высокая доза, но биодоступность при этом остается неизменной) снижает значение Cmax до 31% по отношению к контрольной группе, Tmax до 22% и ППК до 5%, период полураспада уменьшается с 0.73+/-0.07 часа до 0.27+/-0.1 часа.27) Такое же действие оказывается на все метаболиты кофеина (параксантин, теофиллин, теобромин).
Рутакарпин повышает активность ферментов печени, таких как CYP1A2, CYP2B и CYP2E1; стимулирование CYP2E1 наблюдается у крыс при пероральном использовании 80 мг/кг рутакарпина, тогда как для стимулирования CYP1A2 необходимо всего лишь 20 мг/кг. Так как кофеин метаболизируется ферментами CYP1A and CYP2E1, усиление их активности вызывает повышенный метаболизм кофеина в более короткий промежуток времени и ограничивает системное воздействие.
Рутакарпин эффективно подавляет циркулирующие уровни кофеина, ускоряя его распад в печени и кишечнике; высокоантагонистическое соединение.
При использовании рутакарпина (активный индол эводии) значения ППК и Cmax кофеина значительно снижаются; это говорит о том, что рутакарпин снижает воздействие кофеина на организм. Это действие распространяется и на ксантиновое соединение теофиллина. Такой же эффект демонстрирует сама эводия и сочетание отваров, таких как у цзу юй тан.
Данный эффект довольно значителен; предварительное использование 80 мг/кг рутакарпина перорально в течение 3 дней (довольно высокая доза, но биодоступность при этом остается неизменной) снижает значение Cmax до 31% по отношению к контрольной группе, Tmax до 22% и ППК до 5%, период полураспада уменьшается с 0.73+/-0.07 часа до 0.27+/-0.1 часа.27) Такое же действие оказывается на все метаболиты кофеина (параксантин, теофиллин, теобромин).
Рутакарпин повышает активность ферментов печени, таких как CYP1A2, CYP2B и CYP2E1; стимулирование CYP2E1 наблюдается у крыс при пероральном использовании 80 мг/кг рутакарпина, тогда как для стимулирования CYP1A2 необходимо всего лишь 20 мг/кг. Так как кофеин метаболизируется ферментами CYP1A and CYP2E1, усиление их активности вызывает повышенный метаболизм кофеина в более короткий промежуток времени и ограничивает системное воздействие.
Рутакарпин эффективно подавляет циркулирующие уровни кофеина, ускоряя его распад в печени и кишечнике; высокоантагонистическое соединение.
Корневище коптидиса
Сочетание плодов эводии и корневища коптидиса (корневище коптидиса китайского) известно как цзо цзинь вань и используется в традиционной китайской медицине в виде отвара для лечения желудочно-кишечных расстройств. Для приготовления отвара используют 6 частей корневища коптидиса и 1 часть плодов эводии (соотношение 6 к 1). Изменение соотношения в пользу эводии превращает цзо цзинь вань в фань цзо цзинь вань, еще один китайский отвар. Они пригодны только для кратковременного использования.28) Коптидис и эводия образуют дихотомию холодного и горячего (инь и ян), коптидис индуцирует холодное состояние, а эводия теплое. Коптидис понижает внутреннюю температуру тела и поглощение кислорода у мышей и увеличивает время пребывания в теплой среде (теплые подушечки), а эводия увеличивает время пребывания в холодной среде, повышает температуру тела и поглощение кислорода. Цзо цзинь вань классифицируется как охлаждающее средство, а фань цзо цзинь вань как согревающее. Единственным известным на данный момент биомаркером температур является ативность АТФазы печени.29) Коптис китайский и плоды эводии являются антагонистами в процессе влияния на внутреннюю температуру тела; но они часто используются вместе в отварах и микстурах (при острых заболеваниях и при кратковременном использовании; сочетание теплого и холодного). Сочетание «теплого» эффекта эводии и «холодного» эффекта коптиса, видимо, достаточно эффективно, что и демонстрирует тест на предпочтение на крысах, биорегулирующий их температуру. Корневище коптидиса улучшает фармакокинетику и циркулирующие уровни некоторых биоактивных веществ эводии, таких как дегидроэводиамин на 274% (по отношению к использованию эводии отдельно), несмотря на одинаковую дозировку. Эводия незначительно влияет на фармакокоинетику молекул коптидиса, улучшает общую всасываемость, но снижает ППК различных алкалоидов (коптизин, палматин, джатеоррифин) при длительном приеме, а также понижает значение ППК и Cmax берберина, содержащегося в корневище коптидиса, в течение длительного или короткого времени. Но основным свойством плодов эводии считается повышение экспрессии фермента UGT1A1 в печени, который сопрягает соединения в корневище коптидиса.30) Корневище коптидиса китайского повышает биодоступность и циркулирующий уровень эводии, но эводия тормозит абсорбцию и циркулирующий уровень активных ингредиентов коптидиса китайского.
Пеонифлорин
Пеонифлорин – основное биоактивное вещество пиона молочноцветкового, его биодоступность и циркулирующий уровень повышается в сочетании с другими растениями. Прием пеонифлорина в сочетании с плодами эводии повышает относительное поглощение до 123,62%, показатель более низкий, чем при сочетании пеонифлорина с фенхелем (который повышает биодоступность до 226.02% по сравнению с биодоступностью изолированного пеонифлорина). Пеонифлорин не оказывает особого воздействия на эводию, но эводия повышает биодступность пеонифлорина.
Безопасность и токсичность
Согласно результатам тестирования изолированного эводиамина и рутакарпина LD50 для мышей составляет 77.79 мг/кг и 65мг/кг при введении инъекций.
:Tags
Читать еще: Водяной кресс (Жеруха лекарственная) , Галантамин (Реминил) , Генерализированное тревожное расстройство , Древогубец метельчатый , Протриптилин ,










