 Анаболики
Анаболики Витамины
Витамины
Инструменты пользователя
Инструменты сайта
- Life support
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Жгун-корень Моннье
 Жгун-корень Моннье – это проэректильное растение Традиционной китайской медицины. Его основной биоактивный компонент, известный как «остол», оказывает схожее с виагрой воздействие на пениальную ткань и гиппокамп. Воздействие Жгун-корня Моннье на тестостерон и когнитивные функции остаётся неизученным.
Жгун-корень Моннье – это проэректильное растение Традиционной китайской медицины. Его основной биоактивный компонент, известный как «остол», оказывает схожее с виагрой воздействие на пениальную ткань и гиппокамп. Воздействие Жгун-корня Моннье на тестостерон и когнитивные функции остаётся неизученным.
Справка
Также известен как:
Ши Чжуан Цзы, остол, Джашоши, плоды жгун-корня
Не путать с:
Бакопой Моннье, жгун-корнем лекарственным (похожие, но отдельные растения)
Полезная Информация:
остол, основной биоактивный компонент жгун-корня Моннье, не растворяется в воде; рекомендуется употреблять либо этаноловый экстракт плодов жгун-корня, либо, по меньшей мере, добавлять его в пищу
Разновидность:
- Афродизиака
- Традиционной Китайской Медицины
Плохо сочетается с: виагрой в составе силденафила (не нейтрализуют друг друга, однако действуют одинаково, притом, что друг друга никак не дополняют; принимать оба сразу – пустая трата денег)
Происхождение и Состав
Происхождение
Жгун-корень Моннье используется в Традиционной китайской медицине. Само растение называется жгун-корнем Моннье, его стержневой корень называют Ризомом жгун-корня,1) а семена – Ши Чжуан Цзы, или, по-японски – Джашоши. Плоды растения используются в традиционной китайской медицине для лечения кожной и угревой сыпи, в качестве противовирусного препарата, афродизиака (для мужчин), гинекологического препарата (для женщин), а также противоостеопорозного, противодиабетического и иногда даже в качестве противовоспалительного препарата. Изредка, и безо всяких научных оснований, можно даже услышать неопределённые заявления о том, что это растение также может препятствовать старению и способствовать усилению организма.
Состав и структура
В состав жгун-корня Моннье входят: • Кумариновые соединения, такие как остол (18.85-20.12мг/г в сухом плоде) и императорин (0.79-1.02мг/г), а также Ксантотоксин (Метоксален). В составе также были обнаружены исопимпинелин и бергаптен. В высушенных плодах жгун-корня содержится от 1.67 до 2.88% остола.2)
- Тетраметилпиразин
- Фуранокумарины похожие на императорин, такие как книдилин
- Секвитерпены, например торилин, торилолон и 1-гидрокситорилин3)
- Хромоны – умтатин, синдимол и карентин
- Даукостерол
- Терпеноиды – альфа-пинен, камфен и Лимонен
Остол – это основной биоактивный компонент растения ввиду того, что является наиболее выделенным производным кумарина и его соединения в жгун-корне Моннье. его химическое название - 7-метокси-8{3-метилпент 2-энил}кумарин, его структура изображена ниже. В Традиционной Китайской Медицине используются плоды растения, однако биоактивные компоненты находятся и в его семенах. Ввиду наличия дополнительного пятиядерного кольца в императорине, это соединение рассматривается как фуранокумарин. Это по-прежнему кумарин, просто следующая его ступень в классификации. Остол плохо растворяется в воде, что затрудняет его выделение.4) Жгун-корень Моннье содержит в себе кумариновые соединения, схожие по своему действию с остолом, который считается основным биоактивным компонентом растения. Концентрация этих соединений в высушенных плодах может быть довольно высока Следует отметить, что остол также можно найти и в растении дудник пушистый,5) а впервые он был выделен из горичника настурциевого (Peucedanum ostruthium), от которого и получил своё название.
Родственные травы
Жгун-корень лекарственный является традиционным аналогом жгун-корня Моннье в китайской и корейской медицине, по-корейски его название звучит Чон-Гун. Это растение известно своим «восточным» вкусом и запахом и содержит в себе различные эфирные масла.6) Жгун-корень лекарственный – это многолетнее растение из семейства зонтичных, в медицине используется в качестве седативного средства, а также для лечения анемии, заболеваний мозга, а также воспалительных заболеваний женских гениталий, таких как менструальное расстройство.7) В состав жгун-корня лекарственного входят:
- Феруловая кислота (этаноловый экстракт ризомы) – от 0.69 до 1.65мг/г
- Хлорогеновая кислота (этаноловый экстракт ризомы) – от 0.84 до 5.35мг/г
- Фталид Сенкинолид А в пределах от 0.32мг/г (+/-0.02) до 1.14мг/г (+/-0.06) и Z-лигустилид (этаноловый экстракт ризомы) – от 0.74мг/г (+/-0.04) до 4.39мг/г (+/-0.31) (усреднённые показатели, по результатам исследования 15 трав, составили 0.65 мг/г и 1.56мг/г соответственно). Также в составе присутствуют и другие фталиды, например Сенкинолид Н и 6-гидрокси-7метокси-дигидролигустилид.
- Фалкариндиол (гептадека-1,9(цис)-диен-4,6-диен-3,8-ол), а также противовоспалительная молекула при показателе IC50 = 4.31 ± 5.22мкм, которая отвечает за ингибирование окиси азота из стимулированных ЛПС макрофагов.
Фармакология
Поглощение и сыворотка крови
Мышам перорально вводили 40мг/кг остола, затем, при помощи мицеллярной экстракции, получили следующие результаты: Cmax = 2.72 ± 0.89мкг/мл при Tmax = 0.56 ± 0.18 часов, AUC = 11.27 ± 2.63мкг/ч/мл и AUC0-t = 10.49 ± 2.81мкг/ч/мл, а период полураспада составил 5.26 ± 1.67 часов. Единственный показатель, который существенно различался между пероральным и внутривенным введением препарата оказался Tmax (существенное различие, 0.093 часов внутривенно) и немного Cmax, ввиду прекрасной биоусовяемости инъекций. Динамика выделений в этом исследовании не измерялась.8) Было решено использовать микроэкстракцию жидкой фазы пустотелого волокна + ВЭЖХ (что, предположительно, даёт более надёжные результаты, чем мицеллярная экстракция[19]) в результате чего 20мг/кг остола, введённых перорально, дали показатель Cmax = 366 ± 89нг/мл при Tmax = 0.61 ± 0.09 часа, показатель AUC0-t = 780 ± 585нг/ч/мл, а период полураспада составил 4.94 ± 1.84 часа. Пероральный приём 40мг/кг препарата дал показатели AUC = 11.27 ± 2.63мкг/ч/мл и Cmax = 2.72 ± 0.89мкг/мл, а инъекции 8мг/кг дали AUC = 10.52 ± 2.34мкг/ч/мл и Cmax of 4.35 ± 0.65мкг/мл, что позволяет вывести среднюю биоусвояемость в 26.8% при введении крысам. Биоусвояемость может быть ограничена метаболизмом, что получило подтверждение в лабораторных условиях, когда 80% остола подверглись метаболизму в течение 20 минут, а 40% – в течение 5 минут контакта с клетками кишечника посредством конъюгации первой стадии. Сам по себе, остол не обладает высокой проходимостью через мембраны кишечных клеток посредством пассивной диффузии,9) a апикальное значение к базально-латеральному имеет примерно такое же соотношение, как базально-латеральное к апикальной диффузии. В поддержку утверждения, что пассивная диффузия – это механизм поглощения, свидетельствует тот факт, что ингибиторы МРП не оказывают никакого воздействия на кинетику и не похоже, чтобы процесс диффузии зависел от температуры (нейтрализация ферментов-транспортёров). Будучи выделенным, остол обладает умеренной биоусвояемостью (не лучший показатель, но достаточно высокий в сравнении с другими компонентами, выделенными из растений), а также сравнительно быстрый показатель Tmax, который подскакивает в крови в течение часа после перорального приёма. Хотя в одном исследовании показатели указаны в микрограммах, а в другом – в нанограммах, это различие обусловлено лишь разными подходами к анализу. При употреблении этанолового экстракта плодов жгун-корня (высушенных и дважды промытых в этаноле, с последующим введением полученного концентрата), 10г/кг этого препарата (в общей сложности – 131мг/кг остола), введённых мышам, даёт похожий показатель Tmax (1 +/- 0.3 часа), а также период полураспада (3.6 +/- 0.6 часа), показатель AUC = 3.55 ± 0.385мкг/ч/мл, а Cmax = 0.776 ± 0.069мкг/мл. Остол, употребляемый в составе Розмарина бухтарминского, обладает меньшим усвоением, чем выделенный остол.10) В отличие от плода Эводии кожистосеменной, употребление остола посредством этанолового экстракта из плода не повышает биоусвояемость этого компонента. В теории – способен, однако употребление плода не обязательно.
Метаболизм
Метаболизму посредством деметилирования (в О-деметил остол[20]) может способствовать CYP2D6 или CYP3A4, но ингибиция CYP2D6 с Йохимбином в лабораторных условиях не оказала никакого влияния на печёночный метаболизм остола. Судя по всему, ингибиция CYP3A4 повышает продолжительность полураспада в лабораторных условиях, несмотря на то, что вышеупомянутые метаболиты являются O-деметилированными и не N-деметилированными. Тем не менее, эти результаты, полученные в лабораторных условиях отличаются от полученных в живом организме крысы, что позволяет сделать вывод о том, что гидроксилация, деметилирование и гидрогенизация двойных связей явились основным способом метаболизма в течение первой стадии. Низкая биоусвояемость остола, по большей части, обусловлена чрезмерным и слишком быстрым метаболизмом на первой стадии, притом сам метаболизм имеет множество путей.
Выведение из организма
После перорального приёма 20мг/кг остола показатель иммунного клиренса составил 0.67 ± 0.15 мл/кг/ч.
Взаимодействие с печенью
Жировая инфильтрация печени
 Остол может понижать жировую инфильтрацию печени, вызванную Алкоголем; в ходе исследования рацион мышей на 52% состоял из этанола в течение 4 недель, а затем, в течение 6 недель, им давали по 10-40мг/кг остола. Препарат нормализовал изменения в степени транскрипции CPT1A и CYP2E1 (которая была нарушена длительными введением алкоголя, что спровоцировало дальнейшее накопление жира), а также понизил содержание жира в печени. Аналогичное воздействие оказывает та же дозировка остола, если его вводить совместно с актиокислительными и противовоспалительными препаратами, хотя остол, по всей видимости, способствует активации рАПП, который, в свою очередь, снижает активность ДГАТ и ГМГ-КоА, т.е. это процесс способствует, скорее, активации липидов, нежели их накоплению.11) Наблюдается минимальная зависимость от дозировки – большая дозировка остола оказывает большее защитное воздействие, а 10мг/кг считается идеальным соотношением затрат / эффективности. Положительное воздействие оказывается и на жировую инфильтрацию печени, вызванную диетой, особенно обогащённой содержанием молочного жира.12) Причина жировой инфильтрации печени не столь важна, роль играет лишь наличие жирных кислот в принципе. В ходе одного исследования испытуемым в течение шести недель давали по 10-40мг/кг остола, а затем, в течение 2 недель – жирное молоко и было обнаружено, что содержание триглицерида в печёночной ткани опустилось даже ниже исходного значения. Остол, активный компонент жгун-корня Монньери, способен понижать уровень триглицерида в печени (в случае жировой инфильтрации) повышенный вследствие как чрезмерного употребления алкоголя, так и слишком жирной пищи. Исследования на людях не проводились, однако проводились безрезультатные исследования на крысах, Вышеописанный механизм активации рАПП на фоне вызванной Алкоголем жировой инфильтрации печени также наблюдался и в случае того же гепатоза, спровоцированного жирной пищей (НАЖБП), затем рАПП понижает чрезмерно завышенные в результате такого состояния печени показатели DGAT и CYP7A1, а также повышает активность подавленного CPT1A. Самостоятельным альтернативным механизмом является модуляция протеинов SREBP-1c/2, при которой 10-40мг/кг остола подавляют иРНК SREBP-1c и SREBP-2 у мышей, страдающих от жировой инфильтрации печени на 36.6%–54.6% и 64.5%–107.7% соответственно, а 40мг/кг остола нормализуют SREBP-2 до исходного значения. Степень транскрипции иРНК синтазы жирных кислот понижается на 9.1%–38.7%, а рецепторов ЛНЛП – на 54.7%–78.9% после введения 10-40мг/кг остола в печень подопытных крыс. Неизвестно, происходит это на фоне модуляции БССРЭ или активации рАПП. Два уникальных механизма действия были изучены в связи со своей способностью взаимодействовать с остолом и оба либо выводят жирные кислоты из печени, либо используют их для получения энергии.
Остол может понижать жировую инфильтрацию печени, вызванную Алкоголем; в ходе исследования рацион мышей на 52% состоял из этанола в течение 4 недель, а затем, в течение 6 недель, им давали по 10-40мг/кг остола. Препарат нормализовал изменения в степени транскрипции CPT1A и CYP2E1 (которая была нарушена длительными введением алкоголя, что спровоцировало дальнейшее накопление жира), а также понизил содержание жира в печени. Аналогичное воздействие оказывает та же дозировка остола, если его вводить совместно с актиокислительными и противовоспалительными препаратами, хотя остол, по всей видимости, способствует активации рАПП, который, в свою очередь, снижает активность ДГАТ и ГМГ-КоА, т.е. это процесс способствует, скорее, активации липидов, нежели их накоплению.11) Наблюдается минимальная зависимость от дозировки – большая дозировка остола оказывает большее защитное воздействие, а 10мг/кг считается идеальным соотношением затрат / эффективности. Положительное воздействие оказывается и на жировую инфильтрацию печени, вызванную диетой, особенно обогащённой содержанием молочного жира.12) Причина жировой инфильтрации печени не столь важна, роль играет лишь наличие жирных кислот в принципе. В ходе одного исследования испытуемым в течение шести недель давали по 10-40мг/кг остола, а затем, в течение 2 недель – жирное молоко и было обнаружено, что содержание триглицерида в печёночной ткани опустилось даже ниже исходного значения. Остол, активный компонент жгун-корня Монньери, способен понижать уровень триглицерида в печени (в случае жировой инфильтрации) повышенный вследствие как чрезмерного употребления алкоголя, так и слишком жирной пищи. Исследования на людях не проводились, однако проводились безрезультатные исследования на крысах, Вышеописанный механизм активации рАПП на фоне вызванной Алкоголем жировой инфильтрации печени также наблюдался и в случае того же гепатоза, спровоцированного жирной пищей (НАЖБП), затем рАПП понижает чрезмерно завышенные в результате такого состояния печени показатели DGAT и CYP7A1, а также повышает активность подавленного CPT1A. Самостоятельным альтернативным механизмом является модуляция протеинов SREBP-1c/2, при которой 10-40мг/кг остола подавляют иРНК SREBP-1c и SREBP-2 у мышей, страдающих от жировой инфильтрации печени на 36.6%–54.6% и 64.5%–107.7% соответственно, а 40мг/кг остола нормализуют SREBP-2 до исходного значения. Степень транскрипции иРНК синтазы жирных кислот понижается на 9.1%–38.7%, а рецепторов ЛНЛП – на 54.7%–78.9% после введения 10-40мг/кг остола в печень подопытных крыс. Неизвестно, происходит это на фоне модуляции БССРЭ или активации рАПП. Два уникальных механизма действия были изучены в связи со своей способностью взаимодействовать с остолом и оба либо выводят жирные кислоты из печени, либо используют их для получения энергии.
Защита
В лабораторных условиях, жгун-корень Моннье был введён в клетки печени человека с целью нейтрализации воздействия такрина посредством компонентов торилина. Как показали значения EC50, торилин и торилолон защищают клетки печени от воздействия такрина в 3.34 и 19.1 раз эффективней чем силибин, входящий в состав Расторопши.
Диабет
Хотя остол (входящий в состав жгун-корня) считается активатором АМФК, который может понижать воздействие диабета на организм (см. раздел о метаболизме глюкозы), понижение жира в печени также может способствовать борьбе с диабетом.13) Взаимодействие с раковыми клетками
Общая информация
Остол оказывает неселективное цитотоксическое воздействие на раковые клетки, особенно на клетки рака груди(MCF-7), лёгких (SK-LU-1), печени (HepG2) и на клетки эпидермальной карциномы (KB).
Рак груди
В лабораторных исследованиях клеточных линий MCF-7 и MDA-MB-231 было установлено, что остол способен ингибировать пролиферацию раковых клеток при раке груди при показателе IC50 = 25.8мкм and 30.2мкм соответственно. Ингибирование умеренно эффективное. Возможным механизмом действия этой цитотоксичности может оказаться ингибирование синтазы жирных кислот, что вызывает цитотоксичность прекурсоров. Остол также оказывает цитотоксичное воздействие на клетки, вырабатывающие HER2, что повышает активность синтазы жирных кислот. Это провоцирует уменьшение ингибиции Akt/mTOR в раковых клетках груди, так как HER2 воздействует через них на синтазу жирных кислот и это говорит о том, что остол имеет такой же механизм действия, что и катехины зелёного чая. Фенотип синтазы жирных кислот является типичным явлением при раке груди,14) как минимум 30% (по результатам анализа HER2). В лабораторных исследованиях остола также наблюдалась ингибиция МПМ2, что объясняет способность препарата подавлять инвазию и метастаз клеток рака груди. Вероятно, этот процесс связан с синтазой жирных кислот, так как клетки, которые вырабатывают HER2 сверх нормы, обычно более склонны к метастазу.15) Потенциально, может бороться с раком груди, однако исследований в живом организме не проводилось. Воздействует на синтазу жирных кислот и Akt/mTOR примерно так же, как и катехины зелёного чая, однако сравнительный анализ эффективности провести невозможно.
Неврология
Глутаминергическая нейротрансмиссия
В лабораторных условиях, выделенный остол (биоактивный компонент жгун-корня Моннье) и клетки гиппокампа вместе увеличивают выработку глутамата из нейронов во время потенциала действия (ПД) с 7.9±0.2нмоль/мг каждые 5 минут (без остола) до 11.7±0.5нмоль/мг каждые 5 минут (3мкм остола, увеличение на 48.1%), не оказывая при этом никакого воздействия на обычную выработку глутамата. Тот же эффект достигается при использовании императорина, другого биоактивного элемента. Показатель IC50 при этой реакций составил 3.5мкм (4.7мкм императорина) и не зависел от концентрации препарата. Механизм действия опосредован инфлюксом Ca2+ в нейроны во время ПД, тогда как остол, при концентрации в 3мкм, повышает максимальный уровень Ca2+ с 138.3±3.1нмоль (ПД, без остола) до 159.5±2.3нмоль (3мкм остола) и действует путём активации ПКС, так как фосфорилирование ПКС повышается со 112.5+/-3.8% (ПД, без остола) до 134.6+/-5% (3мкм остола во время ПД). Остол не влияет на остаточный потенциал мембраны. В исследованиях в живом организме нейротрансмиссия цГМФ ускорила не только глутаминергическую нейтротрансмиссию, но также и аккумуляцию самой цГМФ – молекулы, ускоряющей нейротрансмиссию ПКС.16) Этому способствует ингибиция протеин киназы цГМФ (зависимая от цГМФ протеин киназа, или ПКГ), что также предотвращает высвобождение глутамата из остола. Активация цГМФ может вызвать все вышеописанные процессы, а инкубация нейронов посредством виагры (силденафила) может повысить цГМФ (посредством ингибиции ФДЭ5), создавая видимость того, что остол уже начал своё действие. Силденафил и остол обладают схожей эффективностью, учитывая показатели EC50 равные 5мкм и 4мкм соответственно. Были также обнаружены два других активатора цГМФ и отсутствие дополнительных воздействий остола. Эти результаты позволяют предположить, что остол и виагра имеют схожие механизмы действия, однако не дополняют и не усиливают действие друг друга. Помимо усиления инфлюкса Ca2+ и предаксональных воздействий цГМФ, остол (равно как и императорин), может также усилить экзоцитоз глутаминергических везикул, что способствует активному высвобождению глутамата. Усиление экзоцитоза везикул вызывается инфлюксом Ca2+, тогда как ингибиция этого инфлюкса предотвращает подобный результат. Усиление гиппокампальной глутамиргической нейротрансмиссии может объяснить проэректильное воздействие жгун-корня (см. раздел о сексуальности), так как глутаминергические процессы в гиппокампе связаны в эрекцией.17) После введения в гиппокамп или гипоталамус, агонисты глутамата вызывают эрекцию, которая нейтрализуется антагонистами рецепторов глутамата. Во время эрекции повышенный уровень глутамата наблюдается также в цереброспинальной жидкости и гипоталамусе. Повышает глутаминергическую нейротрансмиссию посредством усиления кальциевого инфлюкса в нейроны во время потенциала действия. Это происходит ввиду повышения уровня цГМФ в нейронах. Процесс можно локализовать в гиппокампе и некоторых других отделах мозга, например, в гипоталамусе Подобный механизм действия предполагает, что он способен усиливать нейронную стимуляцию, сам по себе стимулятором не являясь.
Седативный эффект и ГАМК нейротрансмиссия
Остол способствует усилению седации под воздействием фенобарбитола, а также снимает гипервозбудимость животных, вызванную Кофеином. Остол не принимает участия в связывающем участке бензодиазепина, так как его воздействие не ингибируется флумазенилом при концентрации в 1мкм. Возможным механизмом действия остола является взаимодействие с рецепторами ГАМК. Остол, также как императорин и книдилин, способен усиливать действие потока хлорида спровоцированного активацией ГАМК на 273.6%±39.4% (остол), 109.8%±37.7% (императорин) и на 204.5%±33.2% (книдилин). Исследования препарата проводились только при его концентрации в 100мкм и 300мкм, указанные выше результаты получены при 300мкм. Судя по всему, они могут изменяться в зависимости от дозировки. Это воздействие наблюдалось совместно с субпопуляцией ГАМК α1β2γ2S, значение остола EC50 было равно 14+/-1мкм. Сам по себе, жгун-корень, при дозировке от 50 до 500мг/кг, не оказывает седативного эффекта на крыс, страдающих от аллергии (см. раздел об аллергиях).
Защитное воздействие
Жгун-корень способен предотвращать нарушения пространственного ориентирования у крыс, которые могут наблюдаться в результате либо овариэктомии, либо перорального введения 3-10мг/кг скополамина.
Взаимодействие с метаболизмом глюкозы
Скелетная мускулатура
Остол, в зависимости от дозировки и времени, усиливает всасывание глюкозы миоцитами (как C2C12, так и L6), что происходит под воздействием АМФК. Концентрация препарата в этом исследовании оставалась в пределах 12.5-50мкм, хотя на гепатоциты он воздействует и при меньшем количестве. Инкубация мышечных клеток при 12.5 и 50мкм препарата повышает усвоение глюкозы посредством транслокации ГЛУТ4 (что происходит под воздействием АМФК) в 1.6 или 2 раза соответственно. Такое воздействие АМФК может оказывать посредством изменения соотношения АМП к АТП, чему, в свою очередь, способствует остол – понижая АТП, он повышает АМП, а это, как известно, является основным стимулятором АМФК в скелетной мускулатуре.18) Остол, в живом организме, и при концентрации в 50мг/кг проявил противогликемические свойства ещё до того, как была обнаружена его взаимосвязь с АМФК.[49] Этот эксперимент был продублирован в организме мыши, у которой вызвали диабет при помощи стрептозотоцина – ей перорально вводили 100мг/кг остола в течение 8 недель и обнаружили то же противогликемическое воздействие. По всей видимости, остол может также фосфорилировать (активировать) протеинкиназу-В и понижать концентрацию белков AS160 и GSK3 – ещё один возможный механизм повышения ГЛУТ4.
Жир
Аналогичным образом АМФК может активироваться и в адипоцитах, ввиду повышенной степени дифференциации адипоцитов у крыс после перорального введения 50мг/кг остола. Это считается противодиабетических свойством, так как глюкозу начинает поглощать большее количество клеток.
Взаимодействие с печенью
Остол может оказывать противодиабетическое воздействие на людей с жировой инфильтрацией печени ввиду своей способности замедлять её развитие. Пероральный приём 5-10мг/кг остола может понижать уровень жирных кислот и триглицеридов в печени на фоне своих противовоспалительных воздействий, что повышает чувствительность к инсулину у животных, страдающих ожирением.
Взаимодействие с ожирением
рАППα/γ
Остол является смешанным стимулятором активности рАПП альфа и гамма, что является одним из механизмов действия, которые борются с жировой инфильтрацией печени. Предполагалось, что этот же механизм оказывает и противодиабетическое воздействие,19) однако активация АМФК кажется более вероятным объяснением. Активация рАППα и рАППγ – это жиросжигающий механизм, который запускается на фоне приёма некоторых пищевых добавок, например – конъюгированной лионеловой кислоты и, что более эффективно – TTК. Таким образом, остол, потенциально, может оказаться агентом, способствующим сжиганию жира. Исследования на крысах по измерению массы тела существенных результатов не показали. Мышей кормили пищей, которая вызывала жировую инфильтрацию печени и, если обычно они набирали 9.5% веса, то понижение составило лишь 3.2-5.1% вне зависимости от дозировки препарата. Потенциально, может либо способствовать потере веса, либо препятствовать ожирению (соответственно – либо понижать вес, либо предотвращать его набор), однако ни одно из утверждений пока не исследовано
Воздействие на сексуальность
Эрекция
Жгун-корень Монньери – это растительный препарат, который часто назначают китайские медики против мужской импотенции. Он традиционно используется для повышения мужской эрекции (или её восстановления) наряду с эпимедиумом стреловидным (подвид Горянки) и рыжиком посевным.20) В лабораторных исследованиях пещеристого тела, биоактивный компонент остола (при определённой дозировке) смог вызвать мышечное расслабление. Вероятно, этот механизм действия происходит посредством ингибиции фосфодиэстеразы, так как остол (равно как и окись азота) стимулирует цГМФ, который, в свою очередь, и вызывает мышечное расслабление. Это свойство присуще всем кумаринам в составе жгун-корня Монньери, однако для эффективного воздействия императорину требуется наименьшая концентрация. Это также может касаться и функций мозга, так как остол способствует глутаминергической нейротрансмиссии (см. раздел Неврологии). Хотя исследования на людях не проводились, препарат традиционно используется в китайской народной медицине для повышения эрекции и, подобно виагре, эффективно воздействует как на ткани пениса, так и на мозг.
Взаимодействие с гормонами
Тестостерон
В одном из исследований, остол способствовал повышению уровня тестостерона, а также лютеинизировал гормон и ФСГ у самцов крыс в течение 20 дней после кастрации. Дальнейшие исследования не проводились.
Эстроген
В ходе изучения крыс после овариэктомии (исследовательская модель менопаузы), инъекции по 30мкг/кг 17β-эстрадиола (биологически активный эстроген) и пероральный приём 9мг/кг остола существенно снизили потерю костной массы. Тем не менее, в этом исследовании было отмечено, что остол не влияет на другие характеристики метаболизма эстрогена и не оказывает на него противоостеопорозного воздействия.[55] Остол никак не повлиял на процессы уменьшения тела матки и набора веса, которые способен замедлять 17β-эстрадиол.
Прогестерон
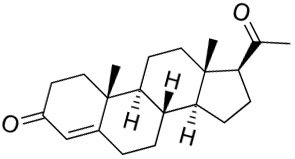 В ходе исследования в лабораторных условиях дудника китайского вместе со жгун-корнем Монньери было обнаружено, что вместе они повышают выработку прогестерона в жёлтом теле.
В ходе исследования в лабораторных условиях дудника китайского вместе со жгун-корнем Монньери было обнаружено, что вместе они повышают выработку прогестерона в жёлтом теле.
Воздействие на аллергию
Дыхательные пути
Кожа
Плоды жгун-корня традиционно употребляются в качестве противоаллергена. Взаимодействуя с различными травами (общий показатель n=33, эффективным он является уже при 6), жгун-корень способен нейтрализовать раздражение кожи, оказываясь наиболее эффективным препаратом для устранения зуда у мышей, вызванного веществом Р. Пероральный приём 50-500мг/кг этанолового экстракта жгун-корня Монньери нейтрализовал желание мышей расчёсывать раздражённые участки кожи, что позволяет предположить его противозудящее воздействие.21) Тот же эффект наблюдается и после приёма плодов жгун-корня. Биоактивными компонентами являются остол и родственные ему кумарины, такие как изопимпинеллин, притом остол (но не императорин) оказался эффективен сам по себе против соединения 48/80, однако веществу Р эффективно противодействовал только изопипинеллин. В сравнении с дифенгидрамином при 50 мг/кг, жгун-корень при 200мг/кг и 500мг/кг был менее эффективен в нейтрализации расчёсывания зудящей кожи, ввиду того, что он вызывал понижение на 33.1-34.7%, тогда как дифенгидрамин – на 89.3%. Изменение дозировки особой роли не играет, так как 50мг/кг оказали примерно такое же воздействие, что и 200, и 500мг/кг. Кумарины, по большей части – изопипинеллин, эффективно понижают раздражение кожи после перорального приёма в составе пищи или пищевых добавок. Пероральное введение 200-500мг/мг остола и кумаринов мышам также подавляют контактный дерматит, который связан с рассматриваемыми воспалительными процессами.
Воздействие на сердце и состояние крови
Ткани сердца
Остол, биоактивный компонент жгун-корня, может ингибировать вызванные эпинефрином или кофеином артериальные спазмы в зависимости от дозировки; в данном исследовании концентрация препарата варьировалась от 40 до 200мкм. Ввиду того, что он частично ингибируется метиленовым синим красителем и не реагирует на индометацин, можно предположить, что механизм действия остола, вызывающий расслабление, основан на блокации кальциевых каналов, а также на аккумуляции цГМФ.
:Tags
Читать еще: Бетаин (триметилглицин) , Гипопитуитаризм , Гликопиррония бромид , Пилоростеноз , Черный перец ,
Список использованной литературы:
Понравилась статья? Поделитесь ей в соцсетях:
Инструменты страницы
Боковая панель
Подпишитесь на новости
Если вы желаете быть в курсе новых материалов, которые публикуются на нашем сайте, подпишитесь на рассылку!
