Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Амфетамин
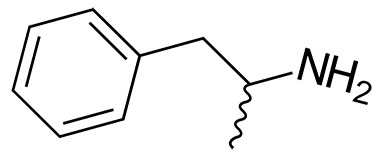 Амфетамин (сокращение от альфа-метилфенэтиламина) – это мощный стимулятор ЦНС, который используется в медицине для лечения синдрома дефицита внимания с гиперактивностью (СДВГ) и нарколепсии. Амфетамин был открыт в 1887 году. Вещество существует в виде двух энантиомеров: левоамфетамин и декстроамфетамин. Слово «амфетамин», в первую очередь, обозначает особенное химическое вещество, рецемическое свободное основание, содержащее в равных пропорциях два энантиомера, левоамфетамин и декстроамфетамин, в чистой аминной форме. Однако, этот термин часто используется для обозначения любой комбинации энантиомеров или любого из них в отдельности. Исторически, амфетамин использовали для лечения заложенности носа, депрессии и ожирения. Амфетамин также используется в качестве ноотропного средства и спортивного допинга, а также рекреационно в качестве афродизиака и средства для улучшения настроения. Во многих странах мира амфетамин доступен при наличии рецепта. Незаконное владение и распространение амфетамина запрещено, поскольку злоупотребление этим веществом влечет за собой серьезные риски для здоровья.
Первым фармацевтическим амфетамином был Бензедрин, ингалятор для лечения ряда заболеваний. В настоящее время фармацевтический амфетамин обычно прописывают в форме препарата Аддерол, декстроамфетамина или неактивной депо-формы лиздексамфетамина. Благодаря активации рецептора TAAR1, амфетамин усиливает активность биогенных аминов и возбуждающих нейротрансмиттеров в мозге, при этом наиболее выраженные эффекты связаны с катехоламинными нейротрансмиттерами норэпинефрином и дофамином. В терапевтических дозах, амфетамин вызывает эмоциональные и когнитивные эффекты, такие как эйфория, изменения либидо, нарушения сна и улучшение когнитивного контроля. Физические эффекты амфетамина включают снижение времени реакции, повышение устойчивости к утомлению и усиление силы мышц.
Очень большие дозы амфетамина могут вызвать нарушение когнитивной функции и спровоцировать быстрое разрушение мышечной ткани. При рекреационном использовании амфетамина, высок риск развития привыкания, чего, однако, не наблюдается при медицинском применении. Прием очень высоких доз может привести к развитию психоза (галлюцинации и паранойя), что редко наблюдается даже при длительном приеме терапевтических доз. Рекреационные дозы, как правило, в несколько раз превышают терапевтические. Такой прием связан с риском тяжелых побочных эффектов.
Амфетамин принадлежит к классу фенэтиламинов и является основным соединением в своем структурном классе замещенных амфетаминов, который включает такие соединения, как бупропион, катинон, MDMA (экстази) и метамфетамин. Являясь членом фенэтиламинового класса веществ, амфетамин также химически связан с естественными нейромодуляторами следовых аминов, а именно, фенэтиламином и N-метилфенетиламином, оба из которых производятся внутри тела человека. Фенэтиламин – это исходное соединение, из которого образуется амфетамин, в то время как N-метилфенетиламин является его структурным изомером, отличающимся только положением метильной группы.
Амфетамин (сокращение от альфа-метилфенэтиламина) – это мощный стимулятор ЦНС, который используется в медицине для лечения синдрома дефицита внимания с гиперактивностью (СДВГ) и нарколепсии. Амфетамин был открыт в 1887 году. Вещество существует в виде двух энантиомеров: левоамфетамин и декстроамфетамин. Слово «амфетамин», в первую очередь, обозначает особенное химическое вещество, рецемическое свободное основание, содержащее в равных пропорциях два энантиомера, левоамфетамин и декстроамфетамин, в чистой аминной форме. Однако, этот термин часто используется для обозначения любой комбинации энантиомеров или любого из них в отдельности. Исторически, амфетамин использовали для лечения заложенности носа, депрессии и ожирения. Амфетамин также используется в качестве ноотропного средства и спортивного допинга, а также рекреационно в качестве афродизиака и средства для улучшения настроения. Во многих странах мира амфетамин доступен при наличии рецепта. Незаконное владение и распространение амфетамина запрещено, поскольку злоупотребление этим веществом влечет за собой серьезные риски для здоровья.
Первым фармацевтическим амфетамином был Бензедрин, ингалятор для лечения ряда заболеваний. В настоящее время фармацевтический амфетамин обычно прописывают в форме препарата Аддерол, декстроамфетамина или неактивной депо-формы лиздексамфетамина. Благодаря активации рецептора TAAR1, амфетамин усиливает активность биогенных аминов и возбуждающих нейротрансмиттеров в мозге, при этом наиболее выраженные эффекты связаны с катехоламинными нейротрансмиттерами норэпинефрином и дофамином. В терапевтических дозах, амфетамин вызывает эмоциональные и когнитивные эффекты, такие как эйфория, изменения либидо, нарушения сна и улучшение когнитивного контроля. Физические эффекты амфетамина включают снижение времени реакции, повышение устойчивости к утомлению и усиление силы мышц.
Очень большие дозы амфетамина могут вызвать нарушение когнитивной функции и спровоцировать быстрое разрушение мышечной ткани. При рекреационном использовании амфетамина, высок риск развития привыкания, чего, однако, не наблюдается при медицинском применении. Прием очень высоких доз может привести к развитию психоза (галлюцинации и паранойя), что редко наблюдается даже при длительном приеме терапевтических доз. Рекреационные дозы, как правило, в несколько раз превышают терапевтические. Такой прием связан с риском тяжелых побочных эффектов.
Амфетамин принадлежит к классу фенэтиламинов и является основным соединением в своем структурном классе замещенных амфетаминов, который включает такие соединения, как бупропион, катинон, MDMA (экстази) и метамфетамин. Являясь членом фенэтиламинового класса веществ, амфетамин также химически связан с естественными нейромодуляторами следовых аминов, а именно, фенэтиламином и N-метилфенетиламином, оба из которых производятся внутри тела человека. Фенэтиламин – это исходное соединение, из которого образуется амфетамин, в то время как N-метилфенетиламин является его структурным изомером, отличающимся только положением метильной группы.
Использование
В медицине
Амфетамин применяется для лечения синдрома дефицита внимания с гиперактивностью (СДВГ) и нарколепсии (нарушение сна), и иногда выписывается вне утверждённых показаний для лечения депрессии, ожирения и заложенности носа.1) У некоторых видов животных, длительное использование амфетамина связано с аномальным развитием допаминовой системы или повреждением нервов,2) однако у людей, страдающих СДВГ, фармацевтические амфетамины, напротив, улучшают развитие мозга и рост нервной ткани. Анализы магнитно-резонансной томографии показали, что длительное применение амфетаминов снижает количество нарушений структуры и функций мозга, обычно наблюдаемых у пациентов с СДВГ, а также улучшает функционирование различных участков головного мозга, таких как правое хвостатое ядро базальной ганглии.3) Исследования клинического использования стимуляторов показали, что длительное использование амфетаминов для лечения СДВГ является безопасным и эффективным.4) Такие же выводы были сделаны после проведения двухлетних контролируемых испытаний.5) В одном обзоре было рассмотрено девятимесячное рандомизированное контролируемое испытание детей с СДВГ, которое продемонстрировало среднее увеличение показателя IQ на 4,5, а также долговременное улучшение внимания и уменьшение эпизодов разрушительного поведения и гиперактивности. Имеющиеся на настоящий момент модели СДВГ предполагают, что данное заболевание связано с функциональными нарушениями в нейротрансмиттерных системах в мозгу; а именно, с нарушением дофаминовой нейротрансмиссии в мезокортиколимбической проекции и нейротрансмиссии норэпинефрина в голубом пятне и префронтальной коре головного мозга.6) Психостимуляторы, такие как метилфенидат и амфетамин, усиливают активность нейротрансмиттеров в этих системах мозга, поэтому их применяют для лечения СДВГ. Приблизительно у 80% пациентов, использующих эти стимуляторы, наблюдаются улучшения в симптоматике СДВГ. Дети с СДВГ, применяющие стимулирующие лекарственные препараты, обычно более дружны со сверстниками и членами семьи, лучше учатся в школе, меньше отвлекаются и совершают меньше необдуманных поступков и имеют лучшую концентрацию внимания.7) В Кохрановском обзоре данных по лечению СДВГ у взрослых с использованием фармацевтических амфетаминов указывается, что, несмотря на то, что эти препараты улучшают кратковременную симптоматику, пациенты, применяющие их, чаще прекращают лечение из-за серьезных побочных эффектов, чем пациенты, применяющие не стимулирующие препараты. Обзор Кохрановского Сотрудничества по лечению детей с СДВГ с тиковыми расстройствами, такими как синдром Туретта, показал, что стимуляторы в целом не ухудшают тики, однако высокие дозы декстроамфетамина могут обострить тики у некоторых пациентов.8)
Улучшение показателей
Систематический обзор и мета-анализ 2015 года клинических испытаний высокого качества показали, что низкие терапевтические дозы амфетамина вызывают заметные улучшения умственных способностей, в том числе – в функционировании рабочей памяти, эпизодической памяти и ингибиторного контроля у здоровых взрослых;9) ноотропные эффекты амфетамина связаны с непрямой активацией дофаминового рецептора D1 и адренорецептора A2 в префронтальной коре. Терапевтические дозы амфетамина также улучшают эффективность работы коры головного мозга, что, в свою очередь, связано с улучшениями в показателях рабочей памяти у всех лиц.10) Амфетамин и другие стимуляторы, применяемые при СДВГ, также улучшают мотивацию при выполнении заданий и усиливают бдительность (активность ЦНС), что также способствует поведению, связанному с достижением цели. Стимуляторы, такие как амфетамин, могут улучшить производительность при выполнении сложных и скучных заданий и используются некоторыми студентами в качестве «допинга» при подготовке к экзаменам.11) Исследования, изучающие самостоятельное незаконное употребление стимуляторов, таких как амфетамин, студентами, показывают, что студенты используют их для улучшения своих результатов, а не в качестве рекреационных наркотиков. Однако, высокие дозы амфетамина, превышающие терапевтический диапазон, могут оказать негативное влияние на рабочую память и другие аспекты когнитивного контроля. Некоторые спортсмены используют амфетамин в качестве стимулятора психических функций и производительности, а именно, увеличения выносливости и концентрации; однако, антидопинговые агентства запрещают его использование на спортивных мероприятиях университетского, национального и международного уровней. У здоровых людей, амфетамин, при пероральном приеме в терапевтических дозах, увеличивает показатели физической силы, ускорение, выносливость и производительность, уменьшая при этом время реакции.12) Амфетамин улучшает выносливость, производительность и время реакции, в первую очередь, за счет ингибирования обратного захвата и утечки дофамина в ЦНС.13) В терапевтических дозах, побочные эффекты амфетамина не влияют на спортивные показатели;14) однако, при приеме доз, во много раз превышающих терапевтические, амфетамин может серьезно нарушить производительность за счет быстрого разрушения мышечной ткани и повышения температуры тела.
Противопоказания
В соответствии с Международной программой по безопасности химических веществ и FDA США, амфетамин противопоказан лицам с историей злоупотребления веществами, а также лицам, имеющим сердечно-сосудистые заболевания, страдающие тяжелыми тревожными расстройствами или беспокойством. Он также противопоказан при артериосклерозе, глаукоме, гипертироидизме или гипертензии. Амфетамин также не рекомендуется при наличии аллергии на другие стимуляторы или во время применения ингибиторов моноаминоксидазы (иМАО).15) Вышеназванные организации также рекомендуют лицам, страдающим от нервной анорексии, биполярного расстройства, депрессии, гипертензии, заболеваний печени или почек, мании, психоза, феномена Рейно, судорожных расстройств, заболеваний щитовидной железы, тиковых расстройств или синдрома Туретта, регулярно следить за симптомами имеющихся заболеваний при использовании амфетамина.16) Данные исследований на людях показывают, что терапевтическое использование амфетамина не связано с аномалиями развития плода или новорожденных (то есть, вещество не является тератогенным), однако злоупотребление амфетамином матерью может быть связано с некоторым риском для плода. Амфетамин может проникать в грудное молоко, поэтому Международная программа по безопасности химических веществ и FDA США рекомендуют матерям воздержаться от кормления грудью при употреблении амфетамина. Из-за наличия риска обратимых нарушений роста, FDA США рекомендует регулярно следить за весом и ростом детей и подростков, которым врач прописал амфетаминовые препараты.
Побочные эффекты
 Амфетамин имеет разнообразные побочные эффекты, и используемая доза является основным фактором, определяющим вероятность развития и тяжесть побочных эффектов. Амфетаминовые продукты, такие как Аддерол, Декседрин и их генерики, одобрены FDA США для длительного терапевтического использования. Рекреационное использование амфетаминов обычно связано с использованием более крупных доз и более серьезным риском развития побочных эффектов.
Амфетамин имеет разнообразные побочные эффекты, и используемая доза является основным фактором, определяющим вероятность развития и тяжесть побочных эффектов. Амфетаминовые продукты, такие как Аддерол, Декседрин и их генерики, одобрены FDA США для длительного терапевтического использования. Рекреационное использование амфетаминов обычно связано с использованием более крупных доз и более серьезным риском развития побочных эффектов.
Физические побочные эффекты
В нормальных терапевтических дозах, физические эффекты амфетамина варьируются в зависимости от возраста и особенностей человека. Сердечно-сосудистые побочные эффекты могут включать в себя гипертензию или гипотензию в результате парасимпатической сосудистой реакции, феномена Рейно (сильное снижение кровотока) и тахикардии (увеличение ЧСС).17) Сексуальные побочные эффекты у мужчин могут включать эректильную дисфункцию, частую эрекцию или более длительную эрекцию. Побочные эффекты, связанные с желудочно-кишечным трактом, могут включать боли в желудке, потерю аппетита, тошноту и потерю веса. Другие потенциальные побочные эффекты включают акне, нечёткое зрение, сухость во рту, скрежетание зубами, повышенное потоотделение, медикаментозный ринит (заложенность носа), снижение судорожного порога и тики (тип двигательных расстройств). Опасные физические побочные эффекты редко наблюдаются при приеме фармацевтических доз. Амфетамин стимулирует медуллярный дыхательный центр, вызывая ускорение и углубление дыхания. У здорового человека при приеме терапевтических доз этот эффект практически незаметен, в отличие от лиц, у которых дыхательная система повреждена. Амфетамин также может вызвать сжатие детрузора мочевого пузыря, мышцы, которая контролирует мочеиспускание, что может привести к сложностям при мочеиспускании. Этот эффект может играть положительную роль при недержании мочи и ночном энурезе. Афетамин может оказать непредсказуемое воздействие на желудочно-кишечный тракт. При повышенной желудочно-кишечной активности, амфетамин может снизить моторику желудочно-кишечного тракта (скорость прохождения пищи через пищеварительную систему); однако, в том случае, если гладкая мускулатура расслаблена, амфетамин может увеличить моторику. Амфетамин также оказывает незначительный анальгетический эффект и может усилить обезболивающее действие опиоидов. Исследования FDA от 2011 года показали, что у детей, молодых людей и взрослых не наблюдается связи между серьезными сердечно-сосудистыми заболеваниями (внезапная смерть, сердечный приступ или удар) и использованием амфетамина или других стимуляторов, применяемых при СДВГ.
Психологические побочные эффекты
Распространенные побочные эффекты при приеме терапевтических доз амфетамина включают чрезмерную возбудимость, тревожность, концентрацию, уменьшение усталости, изменения настроения (чередование повышенного настроения с депрессивными эпизодами), повышенную инициативность, бессонницу или бодрствование, самоуверенность и общительность. Менее распространенные побочные эффекты включают беспокойство, изменения либидо, идеи величия, раздражительность, циклические действия или обсессии и дисфорию; эти эффекты зависят от особенностей личности пользователя и его психологического состояния. У постоянных пользователей при длительном приеме высоких доз может наблюдаться амфетаминовый психоз (галлюцинации и паранойя). Очень редко такой психоз может развиться и при длительном приеме амфетамина в терапевтических дозах. Цитируя FDA США, «не имеется систематических данных», демонстрирующих, что стимуляторы могут способствовать проявлению агрессивности или враждебности.18) Также наблюдался такой интересный эффект, как предпочтение определенного места использования вещества у людей при приеме амфетамина в терапевтических дозах.
Передозировка
Передозировка амфетамином может привести к различным симптомам, однако она редко оказывается смертельной при вовремя оказанной помощи.19) Тяжесть симптомов передозировки увеличивается с увеличением дозы и снижается при развитии толерантности к амфетамину. Пользователи, развившие толерантность, могут принимать до 5 мг амфетамина в день, что в 100 раз превышает максимальную терапевтическую дозу. Ниже перечислены симптомы передозировки средней и сильной тяжести; при смертельном отравлении амфетамином обычно также наблюдаются конвульсии и кома. В 2013 году, от «расстройств, связанных с использованием амфетамина» (куда включается передозировка амфетамином, метамфетамином и другими веществами) погибло 3788 человек (3425–4145 смертей, 95% доверительный интервал). Амфетаминовая зависимость связана, в первую очередь, с патологической гиперактивацией мезолимбического пути, дофаминового пути, соединяющего вентральную область покрышки с прилежащим ядром.20) Лица, часто принимающие высокие дозы амфетамина в рекреационных целях, имеют повышенный риск развития амфетаминовой зависимости, поскольку постоянная передозировка значительно увеличивает уровень ΔFosB, «молекулярного переключателя» и «управляющего белка» при привыкании. При чрезмерной экспрессии ΔFosB в прилежащем ядре, наблюдается ухудшение аддиктивного поведения (то есть, поведения, связанного с постоянным поиском наркотика). Несмотря на отсутствие эффективных препаратов для лечения амфетаминовой зависимости, похоже на то, что регулярное выполнение аэробных физических упражнений снижает риск развития такой зависимости и является эффективным средством для её лечения;21) упражнения улучшают исход клинического лечения и могут использоваться в комбинации с когнитивно-поведенческой терапией (которая является наиболее эффективным способом лечения амфетаминовой зависимости на сегодняшний день).
Симптомы передозировки амфетамином
- Сердечно-сосудистая система: изменения ЧСС, повышение или понижение кровяного давления. При серьезной передозировке – кардиогенный шок (сердце не закачивает достаточное количество крови), кровоизлияние в мозг (инсульт), сердечная недостаточность, амфетаминовый психоз (галлюцинации и паранойя), компульсивные и циклический действия и поведение, серотониновый синдром (чрезмерная активность серотонергической системы), переактивация адренергической системы.
- Скелетно-мышечная система: боль в мышцах. При сильном отравлении – острый некроз скелетных мышц
- Дыхательная система: учащение дыхания, при сильной передозировке – отёк лёгких (аккумуляция жидкости в лёгких), лёгочная гипертензия, респираторный алкалоз (снижение уровня CO2 в крови)
- Мочевыделительная система: болезненные мочеиспускания, задержка мочеиспускания. При сильном отравлении – отсутствие производства мочи, почечная недостаточность.
- Прочие эффекты: повышение температуры тела, при тяжелом отравлении – повышение или снижение уровня калия в крови, гиперпирексия (сильное повышение температуры), метаболический ацидоз
Зависимость
 Развитие зависимости – это серьёзный риск при рекреационном использовании амфетамина в больших дозах. Маловероятно развитие зависимости при использовании амфетамина в терапевтических дозах. При злоупотреблении амфетамином быстро развивается толерантность, поэтому для достижения того же эффекта требуется приём более крупных доз.22)
Развитие зависимости – это серьёзный риск при рекреационном использовании амфетамина в больших дозах. Маловероятно развитие зависимости при использовании амфетамина в терапевтических дозах. При злоупотреблении амфетамином быстро развивается толерантность, поэтому для достижения того же эффекта требуется приём более крупных доз.22)
Биомолекулярные механизмы
Имеющиеся на сегодняшний день модели развития зависимости от хронического употребления наркотических веществ включают изменения в экспрессии генов в определенных участках мозга, а именно, в прилежащем ядре.23) Наиболее важными транскрипционными факторами, влияющими на эти изменения, являются ΔFosB, CREB и NFκB. ΔFosB играет решающую роль в развитии наркотической зависимости, поскольку его чрезмерная экспрессия в средних шипиковых нейронах типа D1 в прилежащем ядре является необходимым и достаточным условием для развития большей части поведенческих и нейронных адаптационных механизмов, наблюдаемых у наркозависимых. При достаточном переизбытке ΔFosB развивается зависимость, которая усиливается при дальнейшей экспрессии ΔFosB. ΔFosB вовлечен в развитие зависимости к алкоголю, каннабиноидам, кокаину, никотину, опиоидам, фенциклидину, замещённым амфетаминам и другим веществам. ΔJunD, транскрипционный фактор, и G9a, фермент гистон метилтрансферазы, непосредственно противостоят индукции ΔFosB в прилежащем ядре (то есть, они не дают увеличиваться его экспрессии). Достаточная экспрессия ΔJunD в прилежащем ядре с вирусными векторами может полностью блокировать многие поведенческие и нейронные изменения при наркомании (т.е., изменения, опосредуемые ΔFosB). ΔFosB также играет важную роль в регулировании поведенческого ответа на естественные стимулы, такие как вкусная пища, секс и физические упражнения.24) Поскольку экспрессия ΔFosB увеличивается как в ответ на естественные стимулы, так и при приеме наркотиков, постоянное получение таких вознаграждений может привести к подобному патологическому привыканию. Таким образом, ΔFosB является наиболее значительным фактором, вовлеченным в амфетаминовую зависимость и сексуальную зависимость, вызванную использованием амфетамина (компульсивное сексуальное расстройство, связанное с чрезмерным употреблением амфетамина и сексуальной активностью). Эти сексуальные зависимости связаны с синдромом дисрегуляции дофамина, который наблюдается у некоторых пациентов, принимающих допаминергические препараты.25) Эффекты амфетамина на генную регуляцию зависят от дозы и от маршрута. Большая часть исследований генной регуляции и развития зависимости была проведена с использованием животных и при внутривенном введении амфетамина в очень высоких дозах. В нескольких исследованиях с использованием дозы, эквивалентной терапевтической дозе (по весу), было показано, что, если эти изменения и наблюдались, они были относительно незначительными. Предположительно, медицинское применение амфетамина не оказывает значительного влияния на генную регуляцию.
Фармакологическое лечение
По состоянию на май 2014 года, не существует эффективной фармакотерапии для лечения амфетаминовой зависимости.26) Амфетаминовая зависимость опосредована увеличением активации дофаминовых рецепторов и колокализованных NMDA рецепторов в прилежащем ядре. Ионы магния ингибируют NMDA рецепторы, блокируя кальциевые каналы рецептора. В одном обзоре было сделано предположение, что, основываясь на данных тестирований на животных, патологическое (связанное с развитием зависимости) использование амфетамина значительно снижает уровни внутриклеточного магния в мозге. Приём добавок магния и флуоксетина снижает частоту самостоятельного использования амфетамина у людей, однако, ни один из препаратов в отдельности не является эффективной мерой лечения амфетаминовой зависимости.27)
Поведенческие технологии
Когнитивно-поведенческая терапия – это наиболее эффективный способ лечения амфетаминовой зависимости из известных на сегодняшний день. Помимо этого, исследования нейробиологических эффектов физических упражнений показывают, что ежедневное выполнение аэробных упражнений, особенно тренировки на выносливость (например, беговой марафон), предотвращает развитие наркотической зависимости и является эффективным средством вспомогательной терапии амфетаминовой зависимости. При выполнении упражнений наблюдается улучшение результатов лечения, особенно при зависимостях от психостимуляторов. В частности, аэробные упражнения снижают частоту самостоятельного применения психостимуляторов, уменьшают риск рецидива и увеличивают плотность дофаминовых D2 рецепторов (DRD2) в стриатуме, в противоположность патологическому использованию стимуляторов, при котором снижается плотность DRD2 в стриатуме.
Зависимость и абстиненция
По данным другого обзора Кохрановского Содружества по абстиненции у лиц, компульсивно использующих амфетамин и метамфетамин, «при резком прекращении использования амфетамина, многие постоянные пользователи сообщают об абстинентном синдроме в течение 24 часов после последней дозы». 28) В обзоре отмечается, что у хронических наркоманов, принимающих высокие дозы амфетамина, часто (в 87.6% случаев) наблюдаются симптомы абстиненции, которые сохраняются на протяжении 3-4 недель, при этом самая тяжелая фаза обычно наблюдается на первой неделе. Симптомы абстинентного синдрома при отмене амфетамина могут включать беспокойство, ломку, депрессию, усталость, увеличение аппетита, увеличение или снижение подвижности, отсутствие мотивации, бессонницу и осознанные сновидения. В обзоре указывается, что симптомы абстинентного синдрома связаны со степенью привыкания. Таким образом, был сделан вывод о том, что терапевтическое использование амфетамина связано с намного более мягкими симптомами. Производители амфетамина для терапевтического использования не указывают о возможности развития симптомов абстинентного синдрома после прекращения употребления амфетамина.
Токсичность и психоз
У грызунов и приматов, достаточно высокие дозы амфетамина вызывают дофаминергическую нейротоксичность (повреждение дофаминовых нейронов), которая характеризуется снижением транспортной и рецепторной функции. Нет данных, подтверждающих прямую нейротоксичность амфетамина у человека. Однако, большие дозы амфетамина могут спровоцировать непрямую нейротоксичность в результате увеличения окислительного стресса от активных форм кислорода и самоокисления дофамина.29) Серьезная передозировка может привести к стимуляторному психозу, который может включать разнообразные симптомы, такие как паранойя и галлюцинации. В обзоре Кохрановского Сотрудничества по лечению амфетаминового, декстроамфетаминового и метамфетаминового психоза указывается, что только около 5–15% пользователей не смогли полностью реабилитироваться. По данным того же обзора, по крайней мере, одно исследование показывает, что антипсихотические лекарственные средства эффективно борются с симптомами амфетаминового психоза. Психоз – очень редкое явление при терапевтическом использовании амфетамина.
Взаимодействия
Известно, что существует множество типов веществ, которые взаимодействуют с амфетамином, что приводит к изменению действия или метаболизма амфетамина, этого вещества, или обоих.30) Ингибиторы ферментов, метаболизирующих амфетамин (например, CYP2D6 и флавин-содержащая монооксигеназа 3) продлевают его период полувыведения, продлевая, таким образом, его действие. Амфетамин также взаимодействует с ингибиторами моноаминоксидазы, особенно с ингибиторами МАОА, поскольку ИМАО и амфетамин увеличивают плазменные уровни катехоламинов (норэпинефрина и дофамина); таким образом, одновременный прием этих веществ может быть опасен.31) Амфетамин модулирует активность большинства психоактивных препаратов. В частности, амфетамин может снижать эффекты седативных средств и депрессантов ЦНС и усиливать эффекты стимуляторов и антидепрессантов. Амфетамин также может снижать эффекты противогипертонических средств и антипсихотиков в результате воздействия на кровяное давление и дофамин соответственно. В общем, при употреблении амфетамина с едой не наблюдается значительных взаимодействий, однако pH содержимого желудочно-кишечного тракта и мочи влияет на абсорбцию и экскрецию амфетамина, соответственно. Кислоты снижают абсорбцию амфетамина и увеличивают его выведение с мочой, а щелочи – наоборот. Из-за воздействия, которое pH оказывает на абсорбцию, амфетамин также взаимодействует с веществами, снижающими кислотность желудка, такими как ингибиторы протонного насоса и антигистаминными H2 средствами, которые усиливают pH желудочно-кишечного тракта (снижая его кислотность).
Фармакология
Фармакодинамика
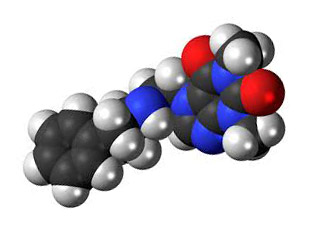 Амфетамин проникает в пресинаптический нейрон через нейронную мембрану или DAT. Оказавшись внутри, он связывается с TAAR1 или проникает в синаптические пузырьки через VMAT2.32) При проникновении амфетамина в синаптические пузырьки через VMAT2, в цитозоль высвобождается дофамин. При связывании амфетамина с TAAR1, снижается частота пульсации дофаминового рецептора через калиевые каналы и провоцируется сигнализация протеинкиназы А (PKA) и протеинкиназы С (PKC), что приводит к фосфорилированию DAT. Фосфорилирование PKA вытесняет DAT в пресинаптический нейрон (интернализация) и блокирует транспорт. DAT, фосфорилированный PKC, может либо действовать задним ходом, либо, как при фосфорилировании PKA, интернализоваться и прекратить транспорт. Амфетамин также увеличивает внутриклеточные уровни кальция, что происходит благодаря активации TAAR1, которая связана с фосфорилированием DAT через CAMK-зависимый путь, в свою очередь, вызывая эффлюкс дофамина.33)
Поведенческие эффекты амфетамина связаны с тем, что он меняет механизмы использования моноаминов в качестве нейронных сигналов в мозгу, в первую очередь, механизмы вознаграждения и исполнительные функции, зависящие от катехоломинных нейронов в головном мозге. Амфетамин, воздействуя на моноаминовые транспортеры, вызывает резкое увеличение концентрации дофамина и норадреналина, основных нейротрансмттеров, вовлеченных в процессы, связанные с вознаграждением и исполнительными функциями, в дозозависимой манере. Эффекты, связанные с усилением внимания и фокусированием на задаче, связаны с увеличением дофаминергической активности в мезолимбическом пути.
Амфетамин является мощным полным агонистом рецептора, связанного со следовыми аминами-1 (TAAR1), Gs-связанного и Gq-связанного G протеин-связанного рецептора (GPCR), обнаруженного в 2001 году, который является важной частью регулирования следовых аминов в головном мозге.34) Активация TAAR1 увеличивает производство cAMP через активацию аденилил циклазы и ингибирует функцию транспортера моноаминов. Моноаминовые авторецепторы (например, D2 короткий, пресинаптический α2 и пресинаптический 5-HT1A) оказывают противоположный TAAR1 эффект, а вместе эти рецепторы являются регуляторной системой для моноаминов. Что интересно, амфетамин и следовые амины связываются с TAAR1, но не связываются с авторецепторами моноаминов. Лучевые исследования продемонстрировали, что ингибирование обратного захвата моноаминов амфетамином или следовыми аминами является локализованым и зависит от присутствия колокализации TAAR1 в связанных моноаминовых нейронах. По состоянию на 2010 год, колокализация TAAR1 и дофаминового транспортера (DAT) была визуализирована у макак-резусов, однако колокализация TAAR1 с транспортерами норэпинефрина (NET) и серотонина (SERT) была связана лишь с экспрессией мессенджера РНК (mRNA).
Помимо нейронных моноаминовых транспортеров, амфетамин также ингибирует везикулярный моноаминовый транспортер-2 (VMAT2), SLC1A1, SLC22A3 и SLC22A5. SLC1A1 – это возбуждающий моноаминовый транспортер-3 (EAAT3), транспортер глутамата, локализованный в нейронах, SLC22A3 – это экстранейронный моноаминный транспортер, представленный в астроцитах, а SLC22A5 – это транспортер карнитина с высокой афинностью. Амфетамин вызывает мощную генную экспрессию транскрипта, регулируемого кокаином и амфетамином (CART),35) нейропептида, вовлеченного в процессы, связанные с поеданием пищи, стрессовыми реакциями и вознаграждением, который вызывает значительное усиление нейронного развития и выживаемости in vitro. Рецептор CART еще не был идентифицирован, однако имеются основания считать, что CART связывается с уникальным Gi/Go-связанным GPCR. В очень высоких дозах, амфетамин также ингибирует моноаминоксидазу, что приводит к снижению дофаминового и фенетиламинового обмена и, следовательно к увеличению концентрации синаптических моноаминов. У человека, единственным известным постсинаптическим рецептором, с которым связывается амфетамин, является рецептор 5-HT1A, где он действует в качестве агониста с микромолярной афинностью.36)
Полный профиль кратковременных эффектов амфетамина, в основном, осуществляется через увеличение клеточного сообщения (нейротрансмиссии) дофамина, серотонина, норэпинефрина, эпинефрина, гистамина, CART пептидов, ацетилхолина, эндогенных опиоидов и глутамата благодаря его взаимодействию с CART, 5-HT1A, EAAT3, TAAR1 и VMAT2.
Декстроамфетамин является более активным агонистом TAAR1, чем левоамфетамин. Следовательно, декстроамфетамин является более сильным стимулятором ЦНС, нежели левоамфетамин (разница в 3-4 раза), однако левоамфетамин проявляет немного более сильные сердечно-сосудистые и периферийные эффекты.
Амфетамин проникает в пресинаптический нейрон через нейронную мембрану или DAT. Оказавшись внутри, он связывается с TAAR1 или проникает в синаптические пузырьки через VMAT2.32) При проникновении амфетамина в синаптические пузырьки через VMAT2, в цитозоль высвобождается дофамин. При связывании амфетамина с TAAR1, снижается частота пульсации дофаминового рецептора через калиевые каналы и провоцируется сигнализация протеинкиназы А (PKA) и протеинкиназы С (PKC), что приводит к фосфорилированию DAT. Фосфорилирование PKA вытесняет DAT в пресинаптический нейрон (интернализация) и блокирует транспорт. DAT, фосфорилированный PKC, может либо действовать задним ходом, либо, как при фосфорилировании PKA, интернализоваться и прекратить транспорт. Амфетамин также увеличивает внутриклеточные уровни кальция, что происходит благодаря активации TAAR1, которая связана с фосфорилированием DAT через CAMK-зависимый путь, в свою очередь, вызывая эффлюкс дофамина.33)
Поведенческие эффекты амфетамина связаны с тем, что он меняет механизмы использования моноаминов в качестве нейронных сигналов в мозгу, в первую очередь, механизмы вознаграждения и исполнительные функции, зависящие от катехоломинных нейронов в головном мозге. Амфетамин, воздействуя на моноаминовые транспортеры, вызывает резкое увеличение концентрации дофамина и норадреналина, основных нейротрансмттеров, вовлеченных в процессы, связанные с вознаграждением и исполнительными функциями, в дозозависимой манере. Эффекты, связанные с усилением внимания и фокусированием на задаче, связаны с увеличением дофаминергической активности в мезолимбическом пути.
Амфетамин является мощным полным агонистом рецептора, связанного со следовыми аминами-1 (TAAR1), Gs-связанного и Gq-связанного G протеин-связанного рецептора (GPCR), обнаруженного в 2001 году, который является важной частью регулирования следовых аминов в головном мозге.34) Активация TAAR1 увеличивает производство cAMP через активацию аденилил циклазы и ингибирует функцию транспортера моноаминов. Моноаминовые авторецепторы (например, D2 короткий, пресинаптический α2 и пресинаптический 5-HT1A) оказывают противоположный TAAR1 эффект, а вместе эти рецепторы являются регуляторной системой для моноаминов. Что интересно, амфетамин и следовые амины связываются с TAAR1, но не связываются с авторецепторами моноаминов. Лучевые исследования продемонстрировали, что ингибирование обратного захвата моноаминов амфетамином или следовыми аминами является локализованым и зависит от присутствия колокализации TAAR1 в связанных моноаминовых нейронах. По состоянию на 2010 год, колокализация TAAR1 и дофаминового транспортера (DAT) была визуализирована у макак-резусов, однако колокализация TAAR1 с транспортерами норэпинефрина (NET) и серотонина (SERT) была связана лишь с экспрессией мессенджера РНК (mRNA).
Помимо нейронных моноаминовых транспортеров, амфетамин также ингибирует везикулярный моноаминовый транспортер-2 (VMAT2), SLC1A1, SLC22A3 и SLC22A5. SLC1A1 – это возбуждающий моноаминовый транспортер-3 (EAAT3), транспортер глутамата, локализованный в нейронах, SLC22A3 – это экстранейронный моноаминный транспортер, представленный в астроцитах, а SLC22A5 – это транспортер карнитина с высокой афинностью. Амфетамин вызывает мощную генную экспрессию транскрипта, регулируемого кокаином и амфетамином (CART),35) нейропептида, вовлеченного в процессы, связанные с поеданием пищи, стрессовыми реакциями и вознаграждением, который вызывает значительное усиление нейронного развития и выживаемости in vitro. Рецептор CART еще не был идентифицирован, однако имеются основания считать, что CART связывается с уникальным Gi/Go-связанным GPCR. В очень высоких дозах, амфетамин также ингибирует моноаминоксидазу, что приводит к снижению дофаминового и фенетиламинового обмена и, следовательно к увеличению концентрации синаптических моноаминов. У человека, единственным известным постсинаптическим рецептором, с которым связывается амфетамин, является рецептор 5-HT1A, где он действует в качестве агониста с микромолярной афинностью.36)
Полный профиль кратковременных эффектов амфетамина, в основном, осуществляется через увеличение клеточного сообщения (нейротрансмиссии) дофамина, серотонина, норэпинефрина, эпинефрина, гистамина, CART пептидов, ацетилхолина, эндогенных опиоидов и глутамата благодаря его взаимодействию с CART, 5-HT1A, EAAT3, TAAR1 и VMAT2.
Декстроамфетамин является более активным агонистом TAAR1, чем левоамфетамин. Следовательно, декстроамфетамин является более сильным стимулятором ЦНС, нежели левоамфетамин (разница в 3-4 раза), однако левоамфетамин проявляет немного более сильные сердечно-сосудистые и периферийные эффекты.
Дофамин
В определенных областях мозга, амфетамин увеличивает концентрацию дофамина в синаптической щели. Амфетамин проникает в пресинаптический нейрон либо при помощи DAT, либо путем непосредственной диффузии в нейронную мембрану. Вследствие захвата DAT, амфетамин является конкурентным ингибитором обратного захвата на этом транспортере. Войдя в пресинаптический нейрон, амфетамин активирует TAAR1, что вызывает фосфорилироване DAT через сигнализацию протеинкиназы A (PKA) и протеинкиназы C (PKC). Фосфорилирование любой протеинкиназой может привести к интернализации DAT (неконкурентное ингибирование обратного захвата), однако фосфорилирование, опосредованное только PKC, вызывает обратную транспортную функцию (эффлюкс дофамина).37) Амфетамин увеличивает внутриклеточные уровни кальция, что происходит в результате активации TAAR1 и связано с фосфорилированием DAT через Ca2+/кальмодулин-зависимую протеинкиназу (CAMK), в свою очередь приводя к эффлюксу дофамина.
Норадреналин
Амфетамин в дозозависимой манере увеличивает синаптические уровни норэпинефрина, прямого предшественника эпинефрина. На основании нейронной экспрессии мРНК TAAR1, считается, что амфетамин воздействует на норэпинефрин, аналогично его воздействию на дофамин.38) Другими словами, амфетамин вызывает TAAR1-опосредованный эффлюкс и неконкурентное ингибирование обратного захвата на фосфорилированном NET, конкурентное ингибирование обратного захвата NET и высвобождение норэпинефрина из VMAT2.
Серотонин
Амфетамин оказывает аналогичные, хотя и менее выраженные, эффекты на серотонин. Амфетамин воздействует на серотонин через VMAT2 и, как и в случае с норэпинефрином, фосфорилирует SERT через TAAR1. Как и дофамин, амфетамин обладает незначительной микромолярной афинностью на человеческом рецепторе 5-HT1A.
Другие нейротрансмиттеры и пептиды
Амфетамин не оказывает прямого эффекта на нейротрансмиссию ацетилхолина, однако некоторые исследования показали, что после использования амфетамина увеличивается высвобождение ацетилхолина. У лабораторных животных амфетамин увеличивает уровни ацетилхолина в определенных участках мозга. У человека подобный феномен наблюдается при активации грелин-опосредованной связи холинергического-дофаминергического вознаграждения в вентральной области покрышки. Кратковременный прием амфетамина у человека также увеличивает высвобождение эндогенных опиоидов в нескольких структурах мозга в системе вознаграждения.39) При употреблении амфетамина увеличиваются внеклеточные уровни глутамата, основного возбуждающего нейротрансмиттера головного мозга. Этот эффект был обнаружен в мезолимбическом пути, области мозга, вовлеченной в процессы, связанные с вознаграждением, при этом амфетамин влияет на нейротрансмиссию дофамина. Амфетамин также индуцирует эффлюкс гистамина из синаптических пузырьков в лаброцитах ЦНС и гистаминергических нейронов через VMAT2.
Фармакокинетика
Пероральная биодоступность амфетамина зависит от pH желудочно-кишечного тракта; он хорошо абсорбируется из кишки, при этом биодоступность декстроамфетамина составляет более 75%. Амфетамин является слабым основанием и имеет показатель pKa 9–10; таким образом, если pH является основным, большая часть препарата находится в жирорастворимой форме свободного основания, и больше может абсорбироваться через богатые жирами клеточные мембраны в эпителии кишки. В противном случае, кислотный pH означает, что препарат находится в основном в водорастворимой катионной (солевой) форме, и меньшая его часть абсорбируется. Приблизительно 15–40% амфетамина, циркулирующего в кровотоке, связывается с белками плазмы. Период полувыведения очень отличается у разных энантиомеров амфетамина и зависит от pH мочи. При нормальном pH мочи, периоды полувыведения декстроамфетамина и левоамфетамина составляют 9–11 и 11–14 часов соответственно. Диета с высоким содержанием кислот снижает период полувыведения энантиомеров до 8–11 часов; а пища с высоким содержанием щелочей, напротив, увеличит его до 16–31 часов.40) Варианты обоих изомеров немедленного и замедленного высвобождения достигают пиковой концентрации в плазме в течение 3 и 7 часов, соответственно. Амфетамин выводится из организма почками, при этом 30–40% вещества выводится в неизмененном виде при нормальном pH мочи. Если pH мочи является основным, амфетамин находится в форме свободного основания и меньшее количество вещества выводится и организма. Если pH мочи не нормальный, мочевое выведение амфетамина может варьироваться от 1% до 75%, в зависимости от щелочности или кислотности мочи соответственно. Амфетамин обычно выводится из организма в течение двух дней после последней пероральной дозы. Наблюдаемый пользователем период полувыведения и продолжение действия увеличиваются при постоянном применении и накоплении препарата в организме. Депо-форма амфетамина, лиздексамфетамин, не так чувствителен к pH, как амфетамин, при абсорбировании в желудочно-кишечном тракте; после абсорбции в кровотоке, он конвертируется ферментами, связанными с красными клетками крови в декстроамфетамин путем гидролиза.41) Период полувыведения лиздексамфетамина обычно составляет меньше часа. CYP2D6, дофамин β-гидроксилаза, флавин-содержащая монооксигеназа 3, битурат-КоА лигаза и глицин N-ацилтрансфераза – ферменты, метаболизирующие амфетамин или его метаболиты в организме человека. Существует много экскретируемых метаболических продуктов амфетамина, в том числе 4-гидроксиамфетамин, 4-гидроксинорэпинефрин, 4-гидроксифенилацетон, бензойная кислота, бензоилгликоколл, норэфедрин и фенилацетон. Активными симпатомиметиками среди этих метаболитов являются 4-гидроксиамфетамин, 4 гидроксинорэпинефрин42) и норэфедрин. Основные метаболические пути включают ароматическое пара-гидроксилирование, алифатическое альфа- и бета-гидроксилирование, N-окисление, N-деакилирование и дезаминирование.
Связанные эндогенные соединения
Амфетамин имеет структурное и функциональное сходство с эндогенными следовыми аминами, натуральными нейротрансмиттерными молекулами, которые производятся в мозге и теле человека. Наиболее близкими к амфетамину соединениями из этой группы являются фенетиламин, предшественник амфетамина, и N-метилфенетиламин, изомер амфетамина (т.е. вещество с идентичной молекулярной формулой).43) В организме человека фенетиламин производится непосредственно из L-фенилаланина при участии декарбоксилазы ароматических аминокислот, которая конвертирует L-ДОФА в дофамин. В свою очередь, N метилфенетиламин превращается из фенетиламина при участии фенилэтаноламин N-метилтрансферазы, фермента, который превращает норэпинефрин в эпинефрин. Как и амфетамин, фенетиламин и N метилфенетиламин регулируют нейротрансмиссию моноаминов через TAAR1; в отличие от амфетамина, оба этих вещества расщепляются при помощи моноаминоксидазы B и, таким образом, имеют более короткий период полувыведения, чем амфетамин.
Физические и химические характеристики
Амфетамин является метиловым гомологом фенетиламина, нейротрансмиттера, встречающегося у млекопитающих, имеющего химическую формулу C9H13N. Атом углерода, прилежащий к первичному амину, является стереогенным центром. Амфетамин состоит из рацемической смеси (1:1) двух энантиомеров. Эта рацемическая смесь может быть разделена на два оптических изомера: левоамфетамин и декстроамфетамин. Что касается физических характеристик, при комнатной температуре чистое свободное основание амфетамина является легкоиспаряющейся жидкостью без цвета и запаха с характерно сильным аминовым запахом и едким вкусом. Твёрдые соли амфетамина включают: амфетамин аспартат, гидрохлорид, фосфат, сахарат и сульфат, причем последний является наиболее распространенной солью амфетамина. Амфетамин является предшественником соединений своего структурного класса, в который входят его психоактивные производные. В органической химии, амфетамин является подходящим хиральным лигандом для стереоселективного синтеза 1,1’-би-2-нафтола.44)
Производные
 Производные амфетамина, которые часто обозначают просто как «амфетамины», или «замещённые амфетамины», представляют собой широкий класс химических веществ, содержащих амфетамин в качестве основы. В этот класс, наряду с другими группами, входят стимуляторы, такие как метамфетамин, серотонинергические эмпатогены, такие как MDMA, и проивозастойные средства, такие как эдедрин. Этот класс химических веществ иногда называт «амфетаминовым семейством веществ».45)
Производные амфетамина, которые часто обозначают просто как «амфетамины», или «замещённые амфетамины», представляют собой широкий класс химических веществ, содержащих амфетамин в качестве основы. В этот класс, наряду с другими группами, входят стимуляторы, такие как метамфетамин, серотонинергические эмпатогены, такие как MDMA, и проивозастойные средства, такие как эдедрин. Этот класс химических веществ иногда называт «амфетаминовым семейством веществ».45)
Обнаружение в жидкостях организма
Амфетамин может быть обнаружен в моче или крови при тестировании. Этот метод используется в спорте, при приеме на работу, при диагностике отравления и в криминалистике. Такие техники, как иммуноанализ (наиболее распространенный метод тестирования на обнаружение амфетамина в организме), могут давать перекрёстную реакцию с некоторыми симпатомиметиками.46) Для предотвращения ложноположительных результатов используются хроматографические методы, специфичные для амфетамина.[180] Техники хирального разделения могут использоваться для того, чтобы обнаружить источник препарата, а также медицинский амфетамин, депо-формы медицинского амфетамина (напр., селегинин), безрецептурные продукты (напр., американская версия Vicks VapoInhaler, содержащая левоамфетамин) или незаконно распространяемые замещённые амфетамины. Некоторые доступные по рецепту препараты производят амфетамин в качестве метаболита. К ним относятся: бенгфетамин, клобензорекс, фампрофазон, фенпропорекс, лиздексамфетамин, мезокарб, метамфетамин, фениламин и селегинин. Эти соединения могут показывать положительные результаты в тесте на наличие амфетамина в теле. Амфетамин обнаруживается в ходе стандартного теста на наркотики в течение приблизительно 24 часов, хотя высокие дозы могут быть обнаружимы и в течение 2-4 дней после использования.
История, общество и культура
Амфетамин был впервые синтезирован в 1887 году в Германии румынским химиком Лазером Еделяну, который назвал полученное соединение фенилизопропиламином;47) вплоть до 1927 года стимулирующий эффект вещества был неизвестен. В 1927 году Гордон Аллес, независимо от Еделяну, заново синтезировал амфетамин и сообщил о его симпатомиметических свойствах. До 1934 года амфетамин не применялся в фармакологии, до тех пор, пока фармацевтическая компания Smith, Kline and French не начала продажи амфетамина в качестве противозастойного ингалятора под торговой маркой Benzedrine (бензедрин). В ходе Второй Мировой Войны амфетамин и метамфетамин широко применялись солдатами армий союзных держав и солдатами гитлеровской армии.48) Когда стало известно о том, что амфетамин вызывает привыкание, в целом ряде стран началась кампания по введению мер контроля за продажей амфетамина. Например, в начале 1970х годов, амфетамин был включен в список II контролируемых веществ в США. Несмотря на жесткий контроль, амфетамин продолжает использоваться легально или нелегально людьми разных социальных уровней и профессий (авторы, музыканты, математики, спортсмены). Амфетамин все еще производится нелегально в подпольных лабораториях и продается на чёрном рынке, преимущественно в странах Европы. По состоянию на 2003 год, в странах Евросоюза амфетамин или метамфетамин употребляло 1,2 миллиона молодых людей.49) По данным 2012 года, в странах Евросоюза было конфисковано около 5,9 тонн нелегально произведенного амфетамина; «уличная цена» такого продукта составляла от 6 до 38 евро за грамм. За пределами Европы, амфетамин куда менее распространен на чёрном рынке, по сравнению с метамфетамином и MDMA.50)
Легальность амфетамина
После принятия Конвенции о психотропных веществах 1971 года, амфетамин был включен в список II контролируемых веществ, во всех (183) странах-членах ЕС. Следовательно, в большинстве стран мира амфетамин подлежит жесткому регулированию. В некоторых странах, например, в Южной Корее и Японии, использование замещенных амфетаминов запрещено даже в медицинских целях. 51) В других странах мира амфетамин разрешен только для медицинского использования.
Фармацевтические продукты
Единственной формой амфетамина, содержащей оба энантиомера и доступной для медицинского использования, является препарат Аддеролл (Adderall). Кроме того, в медицине применяются амфетаминовые препараты, содержащие один энантиомер (декстроамфетами) и депо-формы амфетамина (лиздексамфетамин). Лиздексамфетамин имеет структурные отличия от амфетамина и является неактивным до момента превращения в декстоамфетамин. Свободное основание рацемического амфетамина было ранее доступно в форме таких препаратов, как Бензедрин, Психедрин и Симпатедрин. Левоамфетамин был ранее доступен в виде препарата Cydril. Все доступные сегодня амфетаминовые препараты являются солями, поскольку свободное основание имеет достаточно высокую испаряемость.
ИЮПАК наименование: (RS)-1-фенилпропан-2-амин (RS)-1-фенил-2-аминопропан
Применение при беременности
США: категория C (риск не определен)
Легальность
- Австралия: контролируемое вещество (S8)
- Канада: Список I
- Новая Зеландия: Класс B
- Великобритания: Класс B
- США: Список II
- Евросоюз: Список психотропных веществ II
- ℞ (отпускается только по рецепту)
Способность вызывать зависимость
- Физическая: нет
- Психологическая: средняя
Способы применения
- Медицинское использование: перорально, вдыхание в нос
- Рекреационное использование: перорально, вдыхание в нос, вдувание, ректальное, внутривенное
Биодоступность
Ректальное 95–100%; пероральное 75–100%
Связывание с белками 15–40%
Метаболизм CYP2D6, DBH, FMO3, XM-лигаза и ACGNAT
Начало действия Немедленное Период полураспада
- D-амф:9–11 ч;
- L-амф:11–14 ч
Экскреция Почечная; pH-зависимый уровень: 1–75%
Синонимы α-метилфенэтиламин
Формула C9H13N
Молекулярная масса 135.20622 г/моль
:Tags
Читать еще: Велаксин (Венлафаксин) , Древогубец метельчатый , Фенхель , Циклофосфамид , Эссенциале форте Н ,










