Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Сезамин
 Сезамин – это лигнан, который получают из семян кунжута (Sesamum indicum или Кунжут индийский), и считается, что он ингибирует метаболизм витамина E, благодаря чему уровень γ-токоферола и γ-токотриенола в крови, в целом, повышается; перспективность сезамина заключается, по большому счету, в усилении действия пищевых добавок на основе витамина E.
Сезамин – это лигнан, который получают из семян кунжута (Sesamum indicum или Кунжут индийский), и считается, что он ингибирует метаболизм витамина E, благодаря чему уровень γ-токоферола и γ-токотриенола в крови, в целом, повышается; перспективность сезамина заключается, по большому счету, в усилении действия пищевых добавок на основе витамина E.
Основная информация
Сезамин – это самый известный лигнан, содержащийся в кунжутных семенах, одном из двух крупнейших источников лигнанов в человеческом рационе (второй источник – это лен, в частности, семена льна). Сезамин выпускают в виде пищевой добавки, которая обладает антиоксидантными и противовоспалительными свойствами (что касается пользы для здоровья) и, вероятно, является модулятором рецептора эстрогена и жиросжигателем (для спортсменов и людей, желающих похудеть). У сезамина есть несколько механизмов действия, и если рассматривать препарат в целом, то его можно охарактеризовать как модулятор жирового обмена. Он блокирует фермент дельта-5-десатуразы (Δ5-десатураза), который замедляет жировой обмен в организме; ингибирование этого фермента приводит к снижению уровня эйкозапентаеновой кислоты (ЭПК, одной из двух жирных кислот, богатых рыбьим жиром) и арахидоновой кислоты; данный механизм относится к пероральному приему сезамина. Другой основной механизм заключается в ингибировании процесса токоферол-ω-гидроксиляции, замедляющем усвоение витамина E; блокируя данный фермент, сезамин способствует увеличению запасов витамина E в организме, в частности в гамма-подгруппе (γ-токоферол и γ-токотриенол); данный механизм также относится к пероральному приему сезамина. Есть также некоторые другие потенциально перспективные механизмы действия (профилактика болезни Паркинсона и помощь в наборе костной массы), но большинство из них связаны с модулированием рецептора эстрогена, сжиганием жира в печени и активацией антиоксидантного ответного элемент (ARE) и не подтверждены у людей, в связи с чем ученые предполагают, что таких механизмов не существует на практике; для их функционирования необходимы слишком высокие дозировки сезамина, не совместимые с пероральным приемом, а в случае сжигания жира, такие механизмы характерны исключительно для крыс. В заключении можно добавить, что сезамин выполняет довольно интересную роль потенциального стимулятора метаболизма γ-токоферола и γ-токотриенола, предотвращая их распад; увеличение количества витамеров витамина E - это одно из важнейших свойств сезамина, которое широко применяется в терапии, и поскольку пищевые добавки с витамерами стоят очень дорого, сезамин мог бы быть дешевой альтернативой. Не путать с: семенами кунжута, кунжутным маслом
Сочетается с:
- витамином E (предотвращает его распад и повышает концентрацию γ-токоферола и γ-токотриенола в крови и тканях)
- витамином K (может усиливать задерживающую способность организма в отношении K1 и MK-4)
- рыбьим жиром (предотвращает перокисное окисление липидов и может повышать уровень ДНК в сыворотке)
Сезамин: инструкция по применению
Сезамин мало тестировался на людях, но очевидно, что 100-150мг сезамина достаточно для пополнения существующих запасов сезамина в организме до того уровня, когда он сможет удерживать витамин E в клетках; такое косвенное антиоксидантное действие и является главной причиной приема сезамина в качестве пищевой добавки. Если в качестве основного источника сезамина рассматривать кунжутные семена, в экспериментах с участием людей 50-75г семян было достаточно для восполнения дневной нормы сезамина, тогда как опыты с крысами показали, что им требуется в 100 раз больше кунжутных семян, чем чистого сезамина (100-150мг сезамина – эквивалент 10-15г кунжутных семян).
Источники и структура
Источники
Сезамин – это молекула, известная как лигнан, и поскольку она доминирует во многих пищевых источниках, ее назвали в честь первого открытого учеными источника (масла кунжутных семечек или масла кунжута индийского) и его производной, сезамолина, в 1951 году.1) У кунжута индийского (семян), помимо сезамина, есть еще и другие лигнаны, такие как сезаминол, сезамолин и сезамол, а также множество гликозидов и катаболитов этих лигнанов; в кунжутных семенах представлены 16 отдельных лигнинов2) , из которых сезамину посвящено наибольшее количество исследований, поскольку он, ввиду своих свойств и структуры, является самым важным лигнином в кунжутном масле. Кунжутные семена – это один из немногих источников диетических лигнанов (которые там содержатся в достаточном количестве), поскольку в большинстве продуктов содержание этих ценных молекул составляет меньше 2мг/100г, а в кунжуте их значительно больше (предполагаемое среднее значение – 373мг/100г3)), также как и в семенах льна (335мг/100г);[8] ни один привычный продукт и близко не стоял с этими двумя источниками, за исключением (с натяжкой) нута (35мг/100г) и зеленого горошка (8мг/100г), тогда как в семенах льна, помимо сезамина,4) содержится диглюкозид секоизоларицирезинола (основной лигнановый компонент семян льна). Само по себе, кунжутное масло на 1-2% состоит из «нежирных» компонентов, содержащих лигнаны кунжута.5) Сезамин – это типичный лигнан, который выделяют из масла кунжутных семечек; это далеко не единственный лигнан в составе масла, но именно ему посвящено огромное количество научных исследований, что связано с наиболее высокой концентрацией (по сравнению с другими лигнанами). С тех пор сезамин получают из различных продуктов и лекарственных трав, включая:
- Масло семян кунжута6) и кунжутные семена (Sesamum indicum);7) общее содержание сезамина в последних составляет 373мг/100г, что выше, чем в льняных семенах (на 165%)8), при этом в льняном масле содержится 190-720мг/100г сезамина, в семенах - 67-804мг/100г 9), далее следуют листья растения с микроскопической концентрацией сезамина (0.26мг/100г)
- Различные виды полыни, включая абсент10)
- Различные виды анациклюса, включая анациклюс пиретриновый11)
- Различные виды аристолохии (кирказона), включая к. ладьевидный14)
- Различные виды копытеня, включая к. гетеротроповидный15)
- Различные виды камелии, включая к. масличную (33,88мг/100г масла семян)
- Различные виды хризантемы, включая х. цинерариелистную (10мг/100г сухих плодов)
- Различные виды Кариодафнопсиса, включая к. бараний (220мг/100г плодов)
- Семена павилики (112-200мг/100г сухой коры)
- Различные виды эвкалипта, включая э. шариковый
- Различные виды гингко, включая гингко билоба (листья)16)
- Различные виды зантоксилума, включая з. американский (Северная колючая груша),19) з. крылатый, з. паракантальный,20)хинолин-7-один алкалоиды зантоксилума паракантального (семейство Рутовые)|изд.=2013|авторы=Samita FN, Sandjo LP, Ndiege IO, Hassanali A, Lwande W|журнал=Beilstein J Org Chem] и з. цельнолистный (1,57мг/100г сухих плодов)
- Различные виды глоссостемона, включая г. бругуиерский (араб. ‘Moghat’)
- Различные виды форзиции, включая ф. свисающую21)
- Различные виды магнолии, включая м. коко,[38] м. кобус (4.16мг/10г высушенной коры) and м. обнаженная22)
- Различные виды прутняка, включая ниргунди (0,024мг/100г мыссы сухих семян)
- Различные виды виролы, включая в. суринамскую (70мг/100г семян и околоплодника), в. венозная (8,5% в околоплоднике первичного экстракта), в. мультиневральная (5мг/100г семян) и в. извилистая (737.5мг/100г семян)23)
Несмотря на вое «кунжутное» название, сезамин широко распространен в природе и содержится в самых разных растениях, не будучи «привязанным» к какому-то конкретному семейству или роду. И все же кунжутные семена – это основной источник сезамина, если не считать одно ядовитое растение, а именно, виролу венозную.
Структура
Сезамин – это лигнан (в отличие от пинорезинола, матаирезинола и сирингарезинола), который, сам по себе, не образует соединений, вместо чего, он изначально трансформируется в метаболиты катехола. Несмотря на отсутствие связей, сезамин, как известно, существует в двух формах: сезамин и эписезамин (его наиболее известный эпимер24)), а также как азаринин (наименее известный эпимер25)). Метаболиты пирокатехола образуются, когда группы метеленедиоксифенила (пятиугольники с двумя кислородными структурами) превращаются в группы 3,4-дигидроксифенола (группа катехинов, которая визуально похожа на две OH- группы шестиугольника); метаболитом данной реакции является сезамин монокатехол или сезамин декатехол (depending on в зависимости от того, сколько групп – одна или две – превращаются в катехолы). Сезамин представляет собой лигнановую структуру, которая в ходе метаболизма принимает форму двух побочных продуктов лигнана (энтеродиол и энтеролактон), обладающих некоторыми биологическими свойствами сезамина (и пищевых добавок на его основе). Вышеописанные молекулы имеют некоторые другие названия. Сезамин монокатехол иногда называют SC-1, а когда смешивается с метиловым спиртом (посредством ингибитора катехол-О-метилтрансферазы) – «производная сезамин монокатехола», помимо обычного названия данного вещества («пиперитол»). А поскольку пиперитол является довольно известной молекулой, сезамин монокатехол (буквально «пиперитол», до прикрепления к нему метиловой группы) порой называют деметилированный пиперитол. Пиперитол образуется при смешивании сезамин монокатехола с метиловым спиртом, причем, если только одна сторона сезамин декатехола метилируется, то образовавшуюся молекулу называют 3'-O-деметилпинорезинол; если же оби стороны метилируются, то полученный лигнан – это не что иное, как пинорезинол (содержащийся в пище исходный лигнан). Метаболиты сезамина функционируют совместно с метаболитами других лигнанов, поэтому иногда их названия идентичны, отчего возникает недопонимание.
Фармакология
Кровяная сыворотка
Когда крысам перорально давали сезамин (240-280мг/кг – 2% ежедневного рациона), он был впоследствии обнаружен в их сыворотке, наряду с монокатехолом сезамина и декатехолом сезамина, при этом концентрация всех трех веществ составляла 200нг/мл, оставаясь неизменной даже при включении в рацион крыс 1% витамина E.26) У людей, употребляющих в пищу кунжутные семена (50г семян = 183мг сезамина), усвоение сезамина происходит при максимальной концентрации Cmax 105+/-11.7нМ в течение максимум (Tmax ) одного часа, при этом период полу-усвоения составляет 15минут, а период полувыведения из организма – 2,08+/-0,58 часов; в целом, площадь под кривой «концентрация-время» (AUC) равняется 362+/-92,0нМ/ч/л. Одно из исследований, результаты которого не были обнародованы, показало, что Tmax сезамина составляет 4,7+/-0,2 часов (доза не указана), чуть дольше усваиваются эписезамин и сезамолин.27) У крыс и людей сезамин лучше всего усваивается при пероральном приеме, а в стандартных дозах нано-молярная концентрация препарата в крови варьируется в диапазоне от низкого до умеренного.
Метаболизм
В ходе метаболизма, сезамин, при участии ферментов P450 (CYP2C928), принимает форму сезамин монокатехола (SC-1), который впоследствии метаболизируется (с помощью того же CYP2C9) в сезамин дикатехол (SC-2); Катехолы сезамина либо подвергаются глюкоронидации (через ферменты уридиндифосфата), после чего выводятся из организма вместе с мочой, или смешиваются с метиловым спиртом (при помощи фермента катехол-О-метилтрансферазы), приобретая форму монометиловых структур (SC-1 превращается в SC-1m, известный как пиперитол, а SC-2 в SC-2m); как SC-1, так и SC-2 могут активировать Nrf2/ARE, тогда как сезамин и его метилированные метаболиты не могут29), из чего следует, что вмешательство на уровне фермента катехол-О-метилтрансферазы (COMT) позволяет метаболитам сезамина сохранить свои антиоксидантные свойства. Сезамин монокатехол (SC-1) и сезамин дикатехол (SC-2) обнаруживаются в человеческой моче после перорального приема сезамина (508μM/180мг сезамина и 192μM/71мг сезаминола), при этом 22,2-38,6% принятого сезамина приходится на долю SC-1. Эписезамин проходит тот же метаболический путь, что и сам сезамин. Изначально сезамин метаболизируется (при помощи CYP2C9-фермента) в монокатехол сезамина, после чего тот же фермент помогает ему трансформироваться в дикатехол сезамина. Впоследствии эти производные катехола либо «обрастают» глюкоронидами и выводятся из организма вместе с мочой, либо, при помощи COMT, претерпевают дальнейшие трансформации, в конечном итоге принимая форму метилированных производных сезамина. Сезамин иногда выбирает альтернативный метаболический путь, не связанный с образованием монокатехола. В этом случае, сезамин усваивается микрофлорой кишечника, после чего принимает форму энтеролактона и энтеродиола (CYP2C9 тут ни при чем), основных побочных продуктов деятельности кишечной микрофлоры (при переваривании диетических лигнанов, известных как энтеролигнаны.30) Говорят, что у крыс (как минимум) превращение сезамина в энтеролигнан происходит очень медленно (1,1%), при этом образуется гораздо меньше лигнанов, чем в семенах льна (секоизоларицирезинол - 57,2%)[13] однако конверсия была довольно однородной (у крыс), либо с существенным перевесом в сторону энтеродиола, что было установлено в ходе опытов над мышами, которым давали сезамин (0,1% дневного рациона), после чего сывороточная концентрация энтеролактона составила 6,5-8нM, а энтеродиола - 388-569нM.31) Превращение сезамина в энтеролигнаны происходит при пероральном приеме, однако сезамин не является основным источником синтеза этих лигнанов, здесь пальма первенства принадлежит семенам льна (в том же количестве) и (у крыс) тахини.32) Как и большинство лигнанов, сезамин переваривается кишечником, образуя энтеролигнаны (энтеродиол и энтеролактон), при этом их нано-молярная концентрация в сыворотке довольно мала.
Реакции с ферментами
Сезамин (в зависимости от концентрации) ингибирует деятельность CYP3A4-фермента (на 15,6-55,8% в концентрации 10-40µM), воздействуя на ко-регуляторов прегнан-Х-рецептора (PXR), предотвращает индукцию CYP3A4; при совместном инкубировании с известным стимулятором данного рецептора, сезамин замедляет его (CYP3A4) активацию на 21,3-77,3% (по сравнению с контрольным препаратом).33) Известно, что сезамин блокирует CYP3A4-фермент, препятствуя его активации, в ответ на действие препаратов-активаторов данного фермента. Сезамин (10-100µM) ингибирует деятельность P-глюко-протеина, о чем свидетельствует накопление родамина-123 в клетках LS-180V, которое ускоряется в 2,2 раза при приеме самой высокой (в данном эксперименте) дозы сезамина (то же характерно и для 300µM пиперина), но спустя 48 часов инкуббации, сезамин теряет свои свойства.34) Сезамин повышает сывороточный уровень иРНК мульти-лекарственных белков сопротивления MDR1 и MDR3 (уровень MDR2 меняется незначительно). Сезамин является ингибитором P-гликопротеина и, в то же время, активатором мульти-лекарственного белка сопротивления, с неопределенным действием в последнем случае, что становится не таким важным после продолжительного инкубационного периода сезамина.
Молекулярные цели
Ферменты десатуразы
Δ5-десатураза – это фермент-катализатор конверсии эйкозатетраеновой кислоты в эйкозапентаеновую (или рыбий жир), что характерно для омега-3 жирных кислот, причем Δ5-десатураза выступает в роли медиатора превращения ди-гомо-γ-линоленовой кислоты в арахидоновую кислоту (омега-6 жирные кислоты). Таким образом, скорость реакции замедляется, а блокировка данного фермента приводит к понижению сывороточной концентрации экзопентаеновой (и впоследствии ДГА) и арахидоновой кислот, вызывая тем самым относительное повышение уровня как ди-гомо-γ-линоленовой, так и эйкозатетраеновой кислот. Сезамин – это неконкурентный ингибитор Δ5-десатуразы (Ki=155µM), который практически не влияет ни на деятельность ферментов Δ6, Δ9 или Δ12-десатуразы35) , ни на транскрипцию какого-либо фермента;36) и хотя сезамин считается эффективным в данном отношении, куркумин все же более эффективен37), при этом обе молекулы чаще ингибируют синтез омега-6, чем синтез омега-3. Такое «избирательное» ингибирование не распространяется на крыс, которым, в ходе эксперимента, давали сезамин, из расчета 0,5% дневного рациона (в результате чего концентрация препарата в печени составляла 1,32µг/г, а в сыворотке – 0,17µг/мл) и для здоровых женщин с начавшейся менопаузой, которые ежедневно съедали по 50г кунжутных семечек, что привело к снижению сывороточной концентрации как эйкозапентаеновой (на 12%), так и арахидоновой (на 8%) кислот.38) Сезамин, очевидно, обладает способностью блокировать фермент Δ5-десатуразы, в результате чего снижается уровень концентрации эйкозапентаеновой и арахидоновой кислот в крови. Говорят, что сезамин является мощным ингибитором Δ5-десатуразы, и, тем не менее, куркумин его превосходит, поскольку для качественного ингибирования необходимы слишком большие концентрации сезамина, которых обычно не бывает в организме (если только у человека, и то неточно).
Токоферол-ω-гидроксилаза
Фермент цитохром P450 3A4 (CYP3A) тоже принимает участие в метаболизме токоферолов с их последующим превращением в метаболиты карбоксихрома39), которые, как видно из опытов, важны для усвоения витамина E40), при этом сезамин (1µM) ограничивает метаболизм токоферола, медиатором которого является CYP3A (сезамин ингибирует 90% метаболизма в течение 48 часов), в изолированных HepG2 -клетках; его эффективность в данном случае сопоставима с действием 1µM кетоконазола, в других реакциях сезамин не теряет своих свойств, однако его требуется больше (2µM)41), что, вероятно, связано с цитохромом типа CYP3A, который инициирует ω-гидроксиляцию токоферола.42) Говорят, что в некоторых случаях сезамин выборочно защищает витамеры витамина Е гамма-группы (γ-токоферол и γ-токотриенол), поскольку ранее описанный метаболизм у токоферола протекает более вяло, и, как показывают опыты с крысами по измерению уровня витамеров витамина Е в плазме, чаще всего увеличивается концентрация γ-токоферола и γ-токотриенола, а не α-токоферола.43) Сезамин ингибирует определенные CYP3A-ферменты, которые участвуют в метаболизме витамина E, при котором данный фермент сначала ω-гидроксилирует витамин E (необходимый шаг), после чего оставшаяся часть витамина Е подвергается жировому окислению. Чтобы этому воспрепятствовать, сезамин повышает уровень витамина Е как в плазме, так и в органах. На фоне ингибирования метаболизма витамина Е, сезамин (из расчета 0,2% дневного рациона), как известно, повышает концентрацию этого витамина в крови, если употреблять его в качестве пищевой добавки при стандартном рационе питания44) , а если при этом еще принимать витамин Е (α-токоферол, δ-токоферол и γ-токоферол), то он также начинает накапливаться в сыворотке и в тканях.45) Природные свойства витамина Е, как, например, снижение уровня холестерина в крови, при приеме сезамина усиливаются, а его концентрация в крови растет. Данный механизм жизненно важен для усиления действия диетических или пищевых источников витамина Е, и вся та польза, которую организм извлекает из приема данного витамина, под действием сезамина, преумножается в разы.
Рецепторы, активируемые пролифератом-перокисом (PPARs)
Когда крысам на протяжении 15 дней давали сезамин, из расчета 0,5% дневного рациона (вследствие чего концентрация в клетках печени поднялась до 1,32µг/г, а в сыворотке – до 0,17µг/мл46)), то по прошествии этого периода, у них в 2 раза увеличилась митохондриальная активность печени и аж в 10 раз – окисление жирных кислот в пероксисомах (геномный механизм); такая реакция типична исключительно для крыс и не возникает ни у мышей, ни у хомяков, и наиболее ярко выражена при приеме сезамолина47) и эписезамина, чем самого сезамина. Вышеописанные изменения в процессе липидного окисления являются, как полагают ученые, отражением активации PPARα-рецепторов[78][47] , которые инициируют окисление жировых кислот в печени при активации.48) Они также образуют синергию с диетической эйкозапентановой кислой, но крайне редко с арахидоновой кислотой. Сезамин обладает потенциальной способностью активировать PPARα-рецепторы в печени, однако практическая значимость данного свойства у людей остается под вопросом, ввиду того, что данный механизм у каждого вида протекает по-разному.
Ядерный фактор «каппа-би»
Ученые обнаружили у сезамина способность ингибировать активацию ядерного фактора «каппа-би» (в зависимости от дозы и времени), при помощи различных воспалительных агентов, влияющих на конститутивный и индуктивный ядерный фактор «каппа-би» (IC50 = 40,1-60,2μM, в зависимости от типа клетки).49) Кроме того, сезамин предотвращает распад IκBα –ингибитора (под действием TNF-α-рецептора), совместно с которым впоследствии препятствуют активации IKB-киназы и ядерного фактора «каппа-би», за активацию которого отвечает IKB- киназа. Установлено, что сезамин блокирует ядерный фактор «каппа-би» в раковых клетках, и считается, что данный механизм лежит в основе «химиотерапевтического» эффекта сезамина, связанного с усилением действия противораковых препаратов.
Транскрипционные факторы Nrf2/ARE
Пока сезамин и эписезамин бездействуют, метаболиты SC-1 и EC-1 (продукты распада P450) синтезируют сигналы транскрипционных факторов Nrf2/ARE, тогда как метаболиты SC-1m, EC-1m и EC-2 (продукты распада COMT) , остаются неактивными.50) SC-1 (изучаемая молекула; 1-10µM) способствовала повышению активности Nrf2/ARE (в самой высокой концентрации в 6 раз усиливается активность γ-GCSc и NQO-1). Как полагают ученые, что ингибитор p38 MAPK так или иначе участвует в данной реакции, скорее в роли посредника, но N-ацетилцисцеин препятствует усилению факторов Nrf2/ARE, при приеме сезамина (что предполагает наличие эффектов гормезиса при участии Keap1), а блокировка Nrf2 не дает сезамину защищать клетки H2O2. Сезамин способен активировать антиоксидантный ответный элемент (ARE) через Nrf2, что связано с реакцией гормезиса. Этот принцип лежит в основе антиоксидантных свойств сезамина, хотя прямое антиоксидантное действие и способность индуцировать дисмутазу супероксида подчиняются другим механизмам.
Супероксид дисмутаза
Супероксид дисмутаза (SOD) - это фермент-антиоксидант, который изолирует и блокирует супероксидный радикал (O2-), а сезамин (в концентрации 1пм= 0,001нм) способен усиливать действие данного фермента в 3 раза 51), и это его свойство лежит в основе защиты нейронных клеток PC12 (1пм). Для данной реакции необходимы гораздо более низкие концентрации сезамина, чем для индукции Nrf2/ARE (где самая низкая активная концентрация, 1µM, в 1,000,000 раз выше, чем 1пм), поэтому речь идет о двух разных механизмах. Механизм действия сезамина (в отношении его эффективности в крайне низкой концентрации 1 пикомоль) до сих пор до конца не изучен, но ясно одно: он не связан с другими механизмами сезамина.
Долголетие
Дрозофила
 Сезамин составляет 0,2% дневного рациона плодовой мушки, что способствует увеличению максимальной продолжительности ее жизни приблизительно на 12%, и если 0,1% сезамина влияли на данный показатель лишь незначительно (на 5%), данное свойство сезамина не имеет статистической ценности. Это связано с повышением уровня ферментов дисмутазы супероксида SOD1 и SOD2 и их иРНК, тогда как у некоторых других ферментов (каталазы и Rpn11) увеличилась лишь концентрация иРНК, но не белков.52)
Авторы данного исследования подозревают, что сезамин не влияет на активацию Rpn11 (фермента, который способствует увеличению продолжительности жизни 53)), за это отвечает Mth (или «ген долголетия» 54)). Любопытно, что полный спектр свойств сезамина (активация Rpn11 и ферментов-антиоксидантов без участия Mth) также можно наблюдать в экстракте голубики 55) и в полифенолах, содержащихся в яблоках.56)
Сезамину однажды приписали чудесный «эффект долголетия», что так или иначе связано с повышением концентрации ферментов-антиоксидантов в крови и тканях, а механизмы сезамина в данной реакции схожи с действием других антиоксидантов.
Сезамин составляет 0,2% дневного рациона плодовой мушки, что способствует увеличению максимальной продолжительности ее жизни приблизительно на 12%, и если 0,1% сезамина влияли на данный показатель лишь незначительно (на 5%), данное свойство сезамина не имеет статистической ценности. Это связано с повышением уровня ферментов дисмутазы супероксида SOD1 и SOD2 и их иРНК, тогда как у некоторых других ферментов (каталазы и Rpn11) увеличилась лишь концентрация иРНК, но не белков.52)
Авторы данного исследования подозревают, что сезамин не влияет на активацию Rpn11 (фермента, который способствует увеличению продолжительности жизни 53)), за это отвечает Mth (или «ген долголетия» 54)). Любопытно, что полный спектр свойств сезамина (активация Rpn11 и ферментов-антиоксидантов без участия Mth) также можно наблюдать в экстракте голубики 55) и в полифенолах, содержащихся в яблоках.56)
Сезамину однажды приписали чудесный «эффект долголетия», что так или иначе связано с повышением концентрации ферментов-антиоксидантов в крови и тканях, а механизмы сезамина в данной реакции схожи с действием других антиоксидантов.
Неврология
Глютаминергическая нейротрансмиссия
Сезамин (500-2000нм, в зависимости от концентрации) способен защищать клетки PC12 от некроза (под действием каината), а клетки линии BV-2 более резистентны к его действию (для предотвращения их гибели нужно 10-50µM сезамина); данное свойство сезамина связано со снижением уровня РФК в клетках и пероксидацией липидов.57) Когда крысам в течение трех дней давали 15-30мг/кг экстракта сезамина (90% сезамина и 10% сезамолина), то в более высокой из этих двух доз сезамин полностью защищал клетки от каинатового некроза (смертность клеток снизилась с 22% до нуля). Сезамин (в очень низкой концентрации) защищает клетки от каинатовой экзайтотоксичности, что связано с его антиоксидантными свойствами внутри этих нейронных клеток. Данный процесс был отмечен в ходе эксперимента с крысами, которым давали сезамин перорально. В более высоких концентрациях (1-50µM) сезамин подавляет активацию p38 и ERK1/2 (митоген-активируемые протеин киназы или MAПK), вызванную деятельностью каинатов, а в концентрации 50µM свводит эту разницу на нет; на с-Jun-N-терминальную киназу сезамин не влияет. Сезамин также может блокировать каинатную активацию MAПK(киназы, которая балансирует уровень нейро-токсичности каината), но для этого необходимы более высокие концентрации.
Допаминергическая нейротрансмиссия
Область микроглии образована нейронными опорными клетками (нейроглиальными клетками), принимающими воспалительные сигналы (при активации) и секретные цитокины, которые, выполняя, на физиологическом уровне, жизненно важную функцию, могут вызывать нейродегенерацию, которая только усугубляется с течением времени. Активные микроглиальные клетки, как известно, накапливаются в организме при болезни Паркинсона58), и поэтому их деактивация крайне важна в терапии. В ответ на деятельность MPP+, сезамин мешает нейроглиальным клеткам реагировать на воспаления (судя по выделению IL-6, IL-1β и TNF-α -рецептора), при этом его эффективность сопоставима (или чуть ниже) с 0,1µM (100нM) кверцетина, что связано с подавлением синтеза O2- (супероксида) и, как следствие, со снижением цитотоксичности с 20% до 1,9% и прекращением распада ДНК. Такая эффективность сезамина характерна и для других областей, где в концентрации 1пм он защищает допаминергические PC12 –нейроны от разрушения вследствие окисления, вызванного деятельностью MPP+ (сезамин «спасает» 60% нейронов, если сравнивать с контрольными показателями); данное свойство сезамина связано с включением пероксиддисмутазы (SOD) и со снижением концентрации окислительного фермента каталазы (что свидетельствует о меньшей выраженности процессов окисления в клетках). Сезамин (в крайне низкой концентрации) эффективно защищает клетки от основного допаминергического токсина. Причина этого до сих пор не установлена, вероятно, защитное действие сезамина распространяется только на клетки тестируемой линии (PC12). Сезамин не влияет на концентрацию активного переносчика допамина (DAT), ни сам по себе, ни в ответ на действие MPP+ -токсина (несмотря на способность этого токсина понижать уровень DAT в клетках59)), однако его защитные свойства сохраняются. Итак, сезамин никак не влияет на уровень DAT в клетках. В изолированных клетках PC12 –линии сезамин (в концентрации 20-75µM, но никак не 150-200μM) ускоряет внутриклеточный синтез допамина, (который замедляется при индукциии фермента тирозин гидроксилазы60)) на 106,3–128,2% (50µM), действуя совместно с L-дигидроксифенилаланином. Действие сезамина не затрагивает фермент ДАЛА (катализатор превращения L-ДОФА в допамин). Циклическая cAMP-зависимая протеин киназа (PKA)61) оказывает благотворное воздействие на тирозин гидроксилазу, при этом ее «мишенью» является сезамин, поскольку он способствует повышению внутриклеточной концентрации циклического аденозинмонофосфата, в зависимости от времени действия и концентрации: от 136,5% (10 минут, 20µM) до 321,6% (60 минут, 100µM). Кроме того, сезамин (50μM) способен снижать уровень цитотоксичности в клетках (вызванной действием L-ДОФA), не задействуя при этом дисмутазу супероксида; данная реакция обусловлена тем, что сезамин смягчает негативное действие L-ДОФА на внешне-регулируемую киназу (ERK)1/2. Вне живых организмов, сезамин стимулирует синтез допамина (как минимум), увеличивая ограничение скорости и защищая клетки от допаминового некроза. Для данной реакции необходимы более высокие концентрации сезамина, чем для других его реакций.
Нейро-воспаление
Сезамин (100µM) препятствует активации микроглии (клеток BV-2), вызванной ЛПС, о чем свидетельствует изменение концентрации окиси азота на 20% по отношению к контролю,62) тогда как сезаминол менее эффективен в этом отношении, но все же активен (20-100µM). По данным исследований, сезамин мешает активации p38 MAPK, вызванной ЛПС (смягчая воспалительное действие ЛПС), и, тем не менее, в целях защиты клеток активирует Nrf2/ARE, которые, как известно, деактивируют p38 MAPK;63) разумным объяснением этому является тот факт, что название ‘p38 MAPK' относится как к p38, так и к p42/p44 (сезамин является селективным ингибитором последнего64)), и, тем не менее, данная реакция еще недостаточно изучена. Сезамин уменьшает нейро-воспаление (в повышенных концентрациях), что так или иначе связано с образованием сигналов MAPK. Хотя точный механизм этой реакции до сих пор неизвестен.
Нейрогенез
Монокатехолы сезамина и эписезамина (10µM) инициируют дифференциацию нейронов, активируя внешне-регулируемую киназу1/2 (ERK1/2) (деактиватора TrkA-рецептора), не влияя при этом на сам рецептор, а данная концентрация (10µM) в 62-66% случаев настолько же эффективна, как и 30нг/мл NGF; агонисты данного рецептора, включая NGF в низких концентрациях, образуя синергию между собой и монокатехолами сезамина (5-10µM), становятся на 45-68% активнее.65) Сам по себе, сезамин, как и его дикатехол вместе с производными COMT, в этой концентрации неэффективны или мало эффективны, и считается, что основную роль в этом выполняет ERK1/2, поскольку Akt не активна, а ингибирование ERK1/2 блокирует действие сезамина. Сигналы сезамина, поступающие на TrkA-рецептор, под действием NGF усиливаются, что, как полагают ученые, связано с блокировкой ERK1/2.
Гипоксия и инсульт
Если давать сезамин (20мг/кг) песчанкам, то объем ишемического инфаркта уменьшается (модель инсульта) на 56%, тогда как в комбинации с сезаминолом (90% сезамина и 10% сезаминола) - на 49%. У экспериментальных крыс с гемморагическим инсультом, после инъекции 30нм сезамина в сосуды головного мозга, происходит селективное ингибирование p44/42 (сигнального пути MAPK, тесно связанного с p38), и данный механизм лежит в основе защитных свойств сезамина.66) Как мы видим, сезамин (при пероральном приеме) обладает нейропротективным действием, при этом стандартная человеческая доза составляет 2,5мг/кг.
Здоровье сердечнососудистой системы
Усвоение сезамина
У крыс сезамин (0,5% дневного рациона), влияя на мицеллообразование, препятствует кишечному усвоению холестерина, однако не влияет на усвоение жирных кислот и не вступает ни в какие реакции с желчной кислотой; сезамин не ингибирует жирные кислоты.67) Этим, возможно, и объясняется гипохолестеринемическое действие сезамина (при приеме человеком). Известно, что сезамин мешает усвоению холестерина в кишечнике крыс (в умеренных дозах).
Ткани сердечной мышцы
Оценивая временные характеристики скорости оседания эритроцитов (что необходимо для вычисления степени антиоксидантных эффектов сезамина в живых организмах, посредством инъекции TEMPOL68)), можно сделать вывод, что прием 250мг/кг сезамина (смеси сезамина и эписезамина в равных пропорциях) и 10мг/кг α-токоферола не влияет на восстановительную способность нижней полой вены, и это свидетельствует о том, что спустя 24 часа после перорального приема сезамина, выраженность антиоксидантных свойств остается прежней.
Холестерин
В ЛПНП-рецепторах дефективных мышей (рецептор НЛП-/-) сезамин (0,1% дневного рациона) не снижает уровень холестерина в сыворотке, как сам по себе, так и при одновременном приеме 0,7% станоловых эфиров (которые эффективны, но не в комбинации с сезамином). Пилотный эксперимент, в ходе которого люди с повышенным уровнем холестерина на протяжении 6 недель ежедневно съедали 40г жареных кунжутных семян (без контроля плацебо), показал несостоятельность сезамина в плане ослабления ЛПНП-C и снижения общего уровня холестерина в сыворотке, однако концентрация ЛПВП-C снизилась на 5%, по сравнению с изначальными показателями.
Триглицериды
Сезамин (из расчета 0,1% дневного рациона) не влияет на концентрацию триглицеридов в НЛП-/–рецепторах дефективных мышей, то же можно сказать и об особой экспериментальной диете. Когда люди с повышенным холестерином на протяжении 6 недель ежедневно съедали 40г жареных кунжутных семян (в ходе пилотного эксперимента без контроля плацебо), концентрация триглицеридов в плазме так и не снизилась.
Атеросклероз
Говоря об эндотелиальной дисфункции, вызванной окислением ЛПНП (оЛПНП), то прием сезамина препятствует окислительному действию оЛПНП (косвенным образом защищая фермент дисмутазы супероксида), что, по мнению ученых, обусловлено деактивацией ядерного фактора «каппа-би»; это своеобразная ответная реакция на воспаление.69) Диетический сезамин (63,7+/-0,4мг/кг) как у диких, так и у мышей с аполипопротеином типа Е-/- (предрасположенных к развитию атеросклероза) способствует (лишь незначительно - на 40%) уменьшению очага атеросклеротического поражения артерий и грудного отдела, спустя 26 недель после начала эксперимента (тогда как кверцетин и теафлавин оказались неэффективными в этом отношении), при этом эндотелиальная NO-синтаза была менее активна, чем обе, ранее упомянутые, молекулы.70)
Артериальное давление и кровообращение
Считается, что сезамин разгоняет кровообращение, на фоне синтеза радикалов супероксида71), обусловленным снижением концентрации NADPH-оксидазы (белков p22(phox) и p47(phox)) у крыс-гипертоников;72) ингибирование NADPH мешает синтезу супероксида в клетках эндотелия, поддерживая необходимый уровень активности эндотелиальной NO-синтазы и относительно ускоряя синтез окиси азота, поскольку, в обычных условиях, супероксид, как правило, превращает окись азота в радикал пероксинитрата. Будучи антиоксидантом, сезамин поддерживает и усиливает свойства окиси азота в эндотелии. Когда мышам –гипертоникам давали сезамин (0,1-1% дневного рациона), у них нормализовались процессы окисления, вызванного деятельностью ацетата деоксикортикостерона (DOCA; хотя цистолическое артериальное давление понизилось лишь на 29-55%), чего нельзя сказать о контрольной концентрации кислородных радикалов, которая практически не изменилась; а когда крысам-гипертоникам на протяжении 16 недель давали 40-160мг/кг сезамина, артериальное давление у них пришло в норму. Эксперименты с животными подтверждают предположение ученых о том, что пероральный прием сезамина разгоняет кровообращение при гипертонии. В ходе обследования (двойной слепой метод) женщин среднего возраста с легкой формой гипертонии, которым в течение 4 недель давали 60мг сезамина, у них резко понизилось цистолическое артериальное давление (с 137,6+/-2,2 до 134,1+/-1,7мм/мг; 2.6%мм ртутного столба) и диастолическое артериальное давление (с 87,7+/-1,3 до 85,8+/-1,0мм ртутного столба; то есть давление снизилось на 2,2%). В ходе других исследований также было отмечено благотворное воздействие сезамина на кровообращение здоровых людей с замедленным кровотоком (при одновременном приеме лимонника китайского), а прием кунжутного масла (35г) способствовал повышению артериального давления у гипертоников. Незначительное (но статистически важное) понижение артериального давления наблюдается при пероральном приеме сезамина (в низких дозировках) людьми, причем таким же действием обладает и кунжутное масло.
Реакции с жировой массой
Механизмы
Сезамин (из расчета 2% дневного рациона, прибл. 200мг/кг) подавляет выработку «жирных» генов в печени, спустя 15 дней после начала приема, причем действие его усиливается, распространяясь на все иРНК, если Ваш рацион включает арахидоновую кислоту, чего нельзя сказать о кукурузе и о масле дигидролипоевой кислоты (DHLA). Подобные изменения произошли также в иРНК генов, вовлеченных в процесс окисления жирных кислот, в частности, пероксисомального окисления.73) Свойства сезамина проявляются посредством активного окисления жирных кислот в печени через пероксисомы, при этом сезамин выступает в роли вещеста-агониста PPARα –рецептора. Говоря об изомерах, сезамин, эписезамин или сезамолин в расчете 0,2% дневного рациона могут менять экспрессию генов-регуляторов различных жирных кислот в 1,5- 2 раза, по сравнению с контрольным рационом питания. Также значительно увеличилось число ферментов, участвующих в процессе окисления жирных килот (n=22): на 10-280% с сезамином, на 60-1200% с эписезамином и на 50-1100% с сезамолином (по отношению к контрольному рациону).[47] Подобные изменения произошли генах биогенеза (n=3), чего нельзя сказать о генах липогенеза или липидных транспортировочных генах и их подавлении. В ходе данного исследования ученые пришли к выводу, что эписезамин и сезамолин могут увеличивать массу печени (на 22-27%), снижая при этом массу эпидидимальной белой подкожно-жировой клетчатки (на 19-20%), тогда как сезамин не влияет ни на один из этих параметров. Вне живых организмов, сезамин менее эффективен, чем эписезамин74) и сезамолин, если говорить об индукции генной экспрессии. Сезамин и родственные ему кунжутные лигнаны оказывают влияние на ответные реакции различных геномов, поэтому ученые полагают, что сезамин способен сжигать жир в организме.
Обследования
50г кунжутных семян, если сравнивать с контрольным рисовым порошком одинаковой массы или же с их собственными исходными данными (при контроле калорийности рациона), никак не повлияли на массу тела женщин с начавшейся менопаузой, которые их ели ежедневно на протяжении 4 недель. Таким образом, мы приходим к выводу, что на сегодняшний день ученым не хватает научных фактов, подтверждающих способность сезамина эффективно сжигать жир.
Скелет и метаболизм костной ткани
Остеобласты
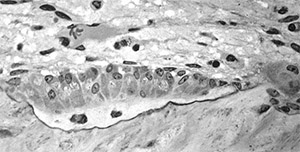 Сезамин увеличивает экспрессию COL1 (в 7 раз), ALP (в 15 раз), OCN и BMP-2 (в 20 раз), Runx2, а также активирует OGN и деактивирует RANKL в остеобластах (линии hFOB1,19) при концентрации 10μг/мл, наиболее существенный и статистически важный эффект проявляется при 1μг/мл.75) Эти изменения говорят о дифференциации остеобластов, и, как раньше считалось, связаны с активацией внешне-регулируемой киназы и образованием сигналов p38 (не факт, что последнее играет роль), поскольку обе MAPK-киназы вызывают рост остеобластов.76)
Сезамин, как минимум в клеточных культурах, способствует росту остеобластов, что, как считают ученые, благотворно сказывается на массе костной ткани.
Сезамин увеличивает экспрессию COL1 (в 7 раз), ALP (в 15 раз), OCN и BMP-2 (в 20 раз), Runx2, а также активирует OGN и деактивирует RANKL в остеобластах (линии hFOB1,19) при концентрации 10μг/мл, наиболее существенный и статистически важный эффект проявляется при 1μг/мл.75) Эти изменения говорят о дифференциации остеобластов, и, как раньше считалось, связаны с активацией внешне-регулируемой киназы и образованием сигналов p38 (не факт, что последнее играет роль), поскольку обе MAPK-киназы вызывают рост остеобластов.76)
Сезамин, как минимум в клеточных культурах, способствует росту остеобластов, что, как считают ученые, благотворно сказывается на массе костной ткани.
Воспаление и иммунология
Макрофаги
Попадание 12,5-50μM сезамина в моноциты линии THP-1 препятствует хемотаксису, вызванному деятельностью N-формил-метионил-фениланина (fMLF в роли хемоаттрактанта, который формирует ответное воспаление при участии FP-рецептора77)), в зависимости от времени действия и концентрации, при этом 50μM достаточно для нормализации хемотаксиса.78) Такая реакция наблюдается после инъекции 12мг/кг сезамина (мышам), у которых процесс хемотаксиса прекратился, что связано с ингибированием сигналов внешне-регулируемой киназы1/2 и активацией ядерного фактора «каппа-би» в моноцитах. В более высоких концентрациях сезамин обладает противовоспалительным действием по отношению к хемотаксису, обеспечивая тканевую фильтрацию иммунных клеток.
Механизмы
Эписезамин предотвращает «шеддинг» эндотелиального рецептора протеина-С (EPCR), вызванный образованием воспалительных сигналов молекул (TNF-α, IL-1β и PMA), происходящем, как считают ученые, на фоне ингибирования фактора некроза опухолей (ФНО).79)
Реакции с окислением
Механизмы
По данным химического анализа дифенилпикрилгидразила (ДФПГ), метаболиты сезамина (5µM), включая монокатехол (11,4%), дикатехол (70.5%), пиперитол (1,2%) и 3'-O-деметилпиперитол (43,2%), обладают прямым антиоксидантным действием, тогда как, сам по себе, сезамин в данном случае, как правило, неэффективен. По данным химического анализа ДФПГ, метаболиты сезамина, а не он сам, способны напрямую захватывать свободные радикалы (вне живых организмов). CYP3A также принимает участие в метаболизме токоферолов с последующим их расщеплением на метеболиты карбоксихрома, что, по подтвержденным данным, имеет отношение к усвоению витамина Е у людей, а 1µM сезамина замедляет метаболизм токоферола, медиатором которого является CYP3A (ингибирует 90% за 48 часов) в изолированных HepG2-клетках; эффективность сезамина в данном случае сопоставима с действием 1µM кетоконазола, сохраняется в других реакциях (2µM) и, вероятн, связана с деятельностью цитохрома типа CYP3А, который инициирует ω-гидроксиляцию токоферола. Как отмечают ученые, сезамин (30мг/кг) повышает уровень витамеров витамина Е в крови на 50-55,8%, по сравнению с изначальным. У крыс, которых кормили исключительно γ-токоферолом и сезамином (из расчета 0,2% дневного рациона), на 20% усиливается накопление γ-токоферола в органах (такой же эффект у кунжутных семечек) и на 20% сокращается мочевыделение80) , тогда как 0,2% сезамина в других реакциях увеличивают уровень α и γ-токоферола в плазме (сезамол в данном случае эффективнее)81) и, будучи в синергии с другими веществами, подавляет пероксидацию липидов, вызванную диетой с преобладанием докохогексановой кислоты (источник – рыбий жир).82) Кунжутные семена не ингибируют процесс попадания витамина E в желчные кислоты.83) Препятствуя деградации витамеров витамина E (что было выявлено в ходе опытов над экспериментальными животными, когда им давали сезамин перорально), сезамин продлевает их действие в организме и проявляет антиоксидантные свойства, на фоне подобных свойств витамина Е.
Супероксид
Супероксид напрямую выводится из организма метаболитами сезамина (5µM), включая монокатехол (55,5%), дикатехол (73,7%), пиперитол (2,5%) и 3'-O-демитилпиперитол (53,6%). Моно- и дикатехолы (сезамина и эписезамина) не столь активны, как моно- и дикатехолы катехина, однако метаболитов эллаговой кислоты.84) Сезамин напрямую блокирует радикалы супероксида, и действие его можно назвать умеренным, поскольку по своей эффективности он находится где-то между двумя вышеупомянутыми молекулами. Сезамин (1пм) может увеличивать экспрессию SOD в нейронах PC12 приблизительно в 3 раза (по сравнению с контролем), защищая при этом от разрушительного действия токсинов. У крыс, подверженных каинатным судорожным припадкам, падение уровня SOD до 55% (по отношению к исходным показателям) продолжается, достигая в итоге 81%, при пероральном приеме 30мг/кг экстракта сезамина (90% сезамина и 10% сезамолина); дозировка 15мг/кг оказалась. Если говорить об индукции фермента дисмутазы супероксида вне живых организмов, то сезамин крайне эффективен в данном случае.
Гидроксильные радикалы
Гидроксильные радикалы напрямую выводятся из организма метаболитами сезамина (5µM), включая монокатехол (5,4%), дикатехол (59,2%), пиперитол (5,7%) и 3'-O-деметилпиперитол (11,9%).[45]Эффективность монокатехола эписезамина сопоставима с действием катехина, а дикатехолы сезамина и эписезамина можно поставить в один ряд с эллаговой кислотой Сезамин эффективно выводит из организма свободные гидроксильные радикалы (он также эффективен, как эллаговая кислота).
Перикись водорода
В клетках PC12, подверженных действию H2O2, активные метаболиты сезамина (2-10μM) борятся с цитотоксичностью, возникающей на фоне активации Nrf2/ARE.
Перекисное окисление липидов (липопероксидация)
Пероксиды липидов (по данным химического анализа побочных продуктов липопероксидации) напрямую выводятся из организма метаболитами сезамина (5µM), включая монокатехол (37,9%), дикатехол (71,3%), пиперитол (6,7%) и 3'-O-деметилпиперитол (42,0%). Несмотря на то, что метаболиты сезамина вступают в метаболические реакции с витамином E, они способны напрямую блокировать пероксиды липидов. У крыс, предрасположенных к каинатовым припадкам, сезамин (30мг/кг) снижает уровень липидной пероксидации (ген с дифференцировкой меланомы в сыворотке) со 145% (контрольных) до 117%, что связано с повышением плазменной концентрации витамина E до 50% и 55,8%, по отношению к исходным показателям (препараты контроля и каинатной группы, соответственно). 15мг/кг сезамина оказались в данном случае неэффективными, и если, сам по себе, сезамин способен снижать уровень липопероксидации у крыс85), то, действуя в синергии с витамином Е, он становится еще более эффективным. Сезамин эффективно ингибирует перекисное окисление липидов, что связано с его способностью увеличивать запасы витамина E в живых организмах.
Повреждение ДНК
Когда мышам, подверженным токсичному действию никеля, на протяжении 20 дней, наряду с никелем, давали диетический сезамин (60-120мг/кг), то в их печени замедлился рост ферментов, ответственных за вредоносное окисление, степень которого снизилась, уменьшая тем самым окислительное повреждение ДНК мышей (по данным анализа 8-OH-диоксигуанозина). Действие сезамина на фоне без-никелевой диеты не отличалось от действия контрольного препарата.86) Кроме того, антиоксидантные свойства сезамина проявляются на геномном уровне, усеньшая степень окислительного повреждения ДНК. Однако у животных, не подверженных действию окислительных токсинов, степень повреждения ДНК, с приемом сезамина, не меняется.
Реакции с гормонами
Эстроген
Что касается рецепторов эстрогена в клетках PC12, сезамин в одной из своих активных концентраций (1пм) не влияет на уровень содержания белка ни в ERα , ни в ERβ-рецепторах. Как известно, действие сезамина не распространяется на сам рецептор эстрогена (на его количество в клетках) Попадание 500-4,000нM (0,5-4µM) сезамина в клетки Исикавы не вызвало эстрогенового эффекта и не повлияло на образование сигналов эстрогена в 1нм эстрадиола. В более высоких концентрациях (10µM) сезамин, попадая в раковые клетки T47D (рак груди), обладает слабовыраженным действием эстрогена и, поскольку в данном случае сезамин выступает в качестве добавки к эстрадиолу (1пм), он подавляет сигналы эстрогена (в концентрации нм); то же самое можно сказать о сезамоле и энтеролактоне, поскольку, как известно, энтеролактон и энтеродиол являются эстрогенами (хотя последний не мешает сигналам 1нм эстрадиола87)). Несмотря на достаточно высокие концентрации (10µM), если мышам с повышенным уровнем эстрогена в крови давать сезамин (1% дневного рациона), то размер эстрогено-зависимой опухоли у них уменьшается, а это говорит о том, что сезамин является антагонистом эстрогена.88) Что касается рецептора эстрогена, ученые сомневаются, что сезамин и отдельные его метаболиты настолько же избирательны, как модуляторы этих рецепторов, однако ни то, ни другое на примере живых организмов не доказано. Эксперимент с участием женщин с начавшейся менопаузой, которые на протяжении 4 недель ежедневно съедали по 50г кунжутных семян, не выявил какого-либо воздействия сезамина на содержание эстрона и эстрадиола (двух составляющих эстрогена) в моче, тогда как уровень сульфатирования ДГЭА в сыворотке снизился на 22%. Незначительно (P=0.065) повысился уровень ГСПГ (15%); эти эффекты не связаны не столько с сезамином, как таковым, сколько с другими лигнанами, содержащимися в кунжуте. Прием семян кунжута не влияет на уровень эстрогена в крове женщин с начавшейся менопаузой.
Реакции с системами органов
Печень
По данным химического анализа скорости оседания эритроцитов (способ измерения степени выраженности антиоксидантных свойств в живых организмах посредством инъекции TEMPOL89)), совместный прием 250мг/кг сезамина (смеси сезамина и эписезамина в равных пропорциях) и 10мг/кг витамина E способствует повышению восстановительной способности печени (показателя антиоксидантнного эффекта) на 10-15% (по сравнению с контролем), которая спустя один день приходит в свое обычное состояние. Несмотря на то, что сезамин не способствует накоплению γ-токотриенола в печени (поскольку сам в ней не накапливается), он незначительно повышает концентрацию α-токоферола.90)
Поджелудочная железа
Попадая в иммортализованные β-клетки поджелудочной железы (NIT-1), подверженные токсичному действию стрептозоцина, сезамин, в зависимости от концентрации (100-400µг/мл), проявляет в этих клетках защитные антиоксидантные свойства (нормализует уровень перокисного окисления липидов и ферментов-антиоксидантов). Сезамин (в высоких концентрациях), вероятно, защищает β-клетки поджелудочной железы от токсичного повреждения стрептозоцином.
Почки
По данным химического анализа скорости оседания эритроцитов, одновременный прием 250мг/кг сезамина и 10мг/кг α-токоферола никак не повлиял на восстановительную способность почечных тканей (спустя 1 день после перорального приема обоих препаратов).
Метаболизм раковых клеток
Иммунные реакции
Вне живых организмов, сезамин препятствует быстрому росту раковых клеток различных линий: лейкозных клеток KBM-5(42,7мкм), K562(IC50=48,3мкм/л), миеломных клеток U266 (IC50=51,7мкм/л), раковых клеток простаты DU145 (IC50=60,2мкм/л), толстой кишки HCT116(IC50=57,2мкм/л), поджелудочной железы MiaPaCa-2 (IC50=58,3мкм/л), клеток легочной аденокарциомы H1299 (IC50=40,1мкм/л) и клеток рака груди BreastMDA-MB-231(IC50=51,1мкм/л). Как отмечают ученые, усиление фактора роста опухолей-а приводит к апоптозу клеточных линий KBM-5 и U266 (другие не исследовали), который ускоряется в 4,7-7,2 раз, и это связано с тем, что сезамин препятствует индукции фактора роста опухолей-а (вызываемой деятельностью Bcl-2 и сурвивина), которая способствует сохранению и развитию раковых клеток в организме. Сезамин предотвращает вызываемую фактором роста опухолей экспрессию пролиферационных (циклина Д1, ЦОГ-2) и инвазивных (фактора межклеточной адгезии-1, матриксной металло-протеин киназы-9, фактора роста сосудистого эндотелия) генных продуктов, что связано с предотвращением сезамином (100мкм/л) транслокации ядерного фактора «каппа-би». В ходе всех экспериментов с сезамином, в клетках человеческого эндотелия была выявлена пониженная экспрессия фактора межклеточной адгезии-1.91) Таким образом, ученые пришли к выводу, что сезамин усиливает эффект от химиотерапии, вне живых организмов, и мешает фактору роста опухолей-а культивировать раковые клетки.
Эстетическая медицина
Кожа
Если сравнивать два рациона питания мышей, один из которых включает 50мг/кг α-токоферола, а другой – 229мг/кг витамина E (содержащего 50мг/кг α-токоферола и 37,4% γ-токотриенола), то через 6 недель после начала эксперимента и за неделю до УФВ-повреждения кожного покрова, мыши из второй группы оказались более защищеннными (в связи с накоплением в клетках кожи γ-токотриенола. При последующем включении в рацион второй группы мышей 0,2% сезамина, накопление γ-токотриенола усилилось, также как и защитные свойства обоих веществ (вследствие синергии). Как мы видим, сезамин стимулирует накопление γ-токотриенола в клетках кожи, благодаря чему его защитное действие на кожу усиливается.
Реакции «биоген-биоген»
Витамин E
На фоне одного из своих основных механизмов действия (ингибирования токоферол-ω-гидроксилазы), сезамин увеличивает запасы витамина Е в организме, как сам по себе, так и при совместном приеме с витамином Е; поэтому сезамин, очевидно, усиливает полезные свойства витамина Е, который также способствует повышению эффективности первого. Наглядными примерами такого синергизма являются: блокировка перокисного окисления липидов, противораковые свойства γ-токотриенола92) и защитное действие токотриенола в борьбе с вредным УФВ-излучением.Одно из исследований (как минимум), направленное на изучение реакций между γ-токоферолом и сезамином у людей, показало, что концентрация d2-γ-CEHC (почечного метаболита γ-tocopherol93)) в моче снизился как у женщин, так и у мужчин (в большей степени, чем у женщин; концентрация почечного метаболита у них снизилась вдвое, спустя 72 часа после того, как они съели кунжутные маффины, содержащие 93,8мг сезамина и 42мг сезамолина). У женщин, как известно, γ-токоферол выводится из организма быстрее, поскольку концентрация липидов у них в крови не настолько высока, как у мужчин (у которых концентрация γ-токоферола в плазме выше, чем у женщин) 94) , и хотя у ученых неоднозначное мнение на счет причины разной скорости выведения почечного метаболит из организма у людей разного пола, это может быть связано с разным уровнем γ-токоферола в плазме. Одним словом, сезамин усиливает свойства всех витамеров витамина E, просто потому, что способствует активному накоплению витамина Е в клетках, где этот витамин (в больших количествах) оказывает благотворное воздействие на наш организм.
Витамин K
Витамин K - это жирорастворимый хиноно-содержащий витамин, который входит в состав K1-витамера (филлохинона) и любых K2-витамеров (менахинонов); он выводится из организма подобно витамину E, поэтому считается, что сезамин способствует накоплению витамина К в клетках. У крыс, пероральный прием сезамина (0,2% дневного рациона) увеличивает концентрацию филлохинона в печени, что можно сказать и о кунжутных семенах (1-10% рациона; различия между разными дозами несущественные); уровень менахинона-4 (МХ-4) в ходе данной реакции не изменился, но при приеме кунжутных семян из расчета 20% рациона, количество его (МХ-4) в тканях (почек, сердца, легких, кишечника и мозга), наряду с филлохиноном, увеличилось. По предварительным данным, при приеме сезамина накопительная способность витамина К в организме также увеличивается.
Витамин C
Учеными отмечается, что сезамин стимулирует синтез витамина C у крыс,95) чего нельзя сказать о людях, поскольку у них отсутствует врожденная способность организма синтезировать витамин С. И хотя сезамин увеличивает запасы витамина С в организме крыс, его действие в данном случае не распространяется на человека; хотя существует некая косвенная взаимосвязь синтеза витамина С с витамином Е , но данный вид синергизма относится скорее не к сезамину, а к самому витамину Е.
Рыбий жир
Как известно, прием сезамина (0,5% рациона) способствует жировому окислению клеток печени и, при совместном приеме с диетическим рыбьим жиром (сезамин - 0,2%, рыбий жир – 1,5-3% рациона крыс) жировое окисление печени синергически усиливается, достигая уровня, характерного для приема рыбьего жира самого по себе (8-10% рациона) 96), а при добавлении рыбьего жира к сезамину, эффективность последнего удваивается. Такой синергизм прослеживается даже в тех реакциях, где сезамин выступает в роли антагониста эйкозопентаеновой кислоты (влияя на ее концентрацию) в печени, что, как считают ученые, связано с ингибированием Δ5-десатуразы. Один из механизмов сезамина связан с активацией PPARα –рецептора (при приеме сезамина наблюдаются побочные эффекты данной реакции), а при включении в рацион рыбьего жира (помимо сезамина) эти эффекты усиливаются.
Альфа-липоевая кислота
У крыс, совместный прием сезамина (2% дневного рациона) и альфа-липоевой кислоты (2,5% рациона) на протяжении 22 дней вызывает понижение сывороточной концентрации триглицеридов (дополнительный синергический эффект),97) несмотря на практически одинаковую генную экспрессию.98) Таким образом, не стоило смешивать между собой эти вещества (что касается уровня триглицеридов в сыворотке), хотя данная комбинация препятствует липогенезу, но при этом аминокислота аланина частично блокирует действие сезамина (которое выражается в стимуляции окисления жирных кислот). По данным одного исследования, сезамин проявляет дополнительные свойства, а именно, препятствует синтезу триглицеридов и выступает в роли антагониста при синтезе жирных кислот.
Лимонник китайский
 Один из биоактивных компонентов лимонника китайского (шизандры), известный как шизандрин-B, стал предметом исследования, при совместном приеме с сезамином (43мг/кг или 215мг/кг); как выяснилось, данная комбинация защищает клетки печени от токсического повреждения, вызванного деятельностью тетрахлорметана, настолько же эффективно, как и 7,5мг/кг силимарина (содержащегося в чертополохе морском.99)
Эксперимент (по изучению вязкости крови), в ходе которого 10 человек с кровообращением ниже среднего на протяжении двух недель одновременно принимали по две таблетки шизандры китайской (65мг экстракта), сезамина (2,5мг) и небольшое количество витамина E (3,75мкг), показал, что по истечении первой недели кровообращение у испытуемых ускорилось на 9% , а в конце второй недели - на 9,7%, по сравнению с исходными показателями.
Шизандра и сезамин стали предметом исследования с двойным слепым методом, участниками которого были люди с критическим уровнем печеночных ферментов; испытуемые принимали двойные дозы обоих препаратов, совместно с комбинированной терапией, в результате чего у них понизился уровень аланин трансферазы и аспарагин трансферазы в крови, а уровень билирубина остался прежним; а спустя 5 месяцев улучшились антиоксидантные параметры.
Ученые изучали свойства лимонника китайского в комбинации с сезамином, однако самому синергизму было посвящено недостаточное количество исследований.
Один из биоактивных компонентов лимонника китайского (шизандры), известный как шизандрин-B, стал предметом исследования, при совместном приеме с сезамином (43мг/кг или 215мг/кг); как выяснилось, данная комбинация защищает клетки печени от токсического повреждения, вызванного деятельностью тетрахлорметана, настолько же эффективно, как и 7,5мг/кг силимарина (содержащегося в чертополохе морском.99)
Эксперимент (по изучению вязкости крови), в ходе которого 10 человек с кровообращением ниже среднего на протяжении двух недель одновременно принимали по две таблетки шизандры китайской (65мг экстракта), сезамина (2,5мг) и небольшое количество витамина E (3,75мкг), показал, что по истечении первой недели кровообращение у испытуемых ускорилось на 9% , а в конце второй недели - на 9,7%, по сравнению с исходными показателями.
Шизандра и сезамин стали предметом исследования с двойным слепым методом, участниками которого были люди с критическим уровнем печеночных ферментов; испытуемые принимали двойные дозы обоих препаратов, совместно с комбинированной терапией, в результате чего у них понизился уровень аланин трансферазы и аспарагин трансферазы в крови, а уровень билирубина остался прежним; а спустя 5 месяцев улучшились антиоксидантные параметры.
Ученые изучали свойства лимонника китайского в комбинации с сезамином, однако самому синергизму было посвящено недостаточное количество исследований.
Конъюгированная линолевая кислота
Конъюгированная линолевая кислота (КЛК) - это смесь жирных кислот, которую расхваливают за эффективность в борьбе с лишним весом (тот же механизм, что у сезамина). В ходе эксперимента с двумя группами крыс, одной из которых на протяжении 8 недель давали 1% КЛК, а другой, наряду с КЛК, давали 0,2% сезамина (с примесью эписезамина), не было выявлено никаких кумулятивных или синергических эффектов этих препаратов.100) То же относится и к предыдущему эксперименту с крысами (те же дозировки КЛК и сезамина), хотя в ходе обоих исследований наметилась тенденция статистической важности кумулятивного действия сезамина и КЛК.
:Tags
Читать еще: Абилифай (Арипипразол) , Болденон (Эквипойз) , Бримонидин , Дигидротестостерон , Иглица колючая (Иглица понтийская) ,










