Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Синефрин

Синефрин, или, более конкретно, p-синефрин, является алкалоидом, который встречается в природе в составе некоторых растений и животных, а также содержится в одобренной лекарственной продукции в форме его m-замещенного аналога, известного как неосинефрин. P-синефрин (или ранее Sympatol и oxedrine) и m-синефрин известны своими долгодействующими адренергическими эффектами, по сравнению с норадреналином. Это вещество присутствует в очень низких концентрациях в составе распространенных пищевых продуктов, таких как апельсиновый сок и другие цитрусовые. В традиционной китайской медицине (ТКМ), также известной как Чжи Ши, используются незрелые и высушенные целые апельсины из вида померанцев. Экстракт этого растения, или очищенный синефрин, также выпускается на рынок в США, иногда в сочетании с кофеином, в качестве диетической добавки для потери веса. В то время как традиционные препараты использовались на протяжении тысячелетий в качестве компонента формул ТКМ, сам синефрин не является утвержденным препаратом. В качестве фармацевтического препарата, m-синефрин до сих пор используется в качестве симпатомиметика (например, за свои гипертонические и сосудосуживающие свойства), в основном в виде инъекций, применяемых в чрезвычайных ситуациях, таких как шок, и редко принимается перорально для лечения бронхиальных проблем, связанных с астмой и сенной лихорадкой. Важно различать исследования синефрина как единой химической единицы (и даже здесь следует иметь в виду, что синефрин может существовать в виде одного из двух стереоизомеров, D- и L-синефрина, отличающихся друг от друга химически и фармакологически), синефрина, смешанного с другими лекарственными средствами и / или растительными экстрактами в виде «добавки», а также синефрина, который присутствует в качестве только одного из химических компонентов в натуральной смеси фитохимикатов, например, в кожуре плодов или горьких цитрусовых. Не следует полагать, что смеси, содержащие синефрин в качестве только одного из их химических компонентов (независимо от того, имеют они синтетическое или естественное происхождение), производят точно такие же биологические эффекты, как синефрин. Внешне синефрин представляет собой бесцветное кристаллическое твердое вещество, растворимое в воде. Его молекулярная структура основана на структуре фенэтиламина, и связана с многими другими препаратами, и с основными нейромедиаторами адреналином и норадреналином.
Фармакологическая группа: алкалоиды
ИЮПАК название: 4 - [1-гидрокси-2-(метиламино)этил] фенол
Другие названия: р-синефрин
Молекулярная формула: C9H13NO2
Молярная масса: 167,21 г / моль
Внешний вид: бесцветное твердое вещество
Температура плавления: 162-164 ° C (R-(-)-энантиомер); 184-185 ° C (рацемат)
Растворимость: растворим в воде
Общая информация
Молекула Синефрина подобна эфедрину, но менее мощная. Обычно Синефрин называют 'померанцем' (горький апельсин). Синефрин – это менее мощное средство для похудания в сравнении с эфедрином. Он может оказывать незначительное воздействие на системы кровообращения и пищеварения. Другие названия: померанец (горький апельсин), p-синефрин, Citrus Aurantium. Не путать с эфедрином. На заметку:
- P-синефрин является стимулирующим средством
- На данный момент известно, что p-синефрин не влияет на показатели теста CEDIA на состав амфетамина в моче
- Синефрин разрешён Всемирным Антидопинговым Агентством, в отличие от его метаболита октопамина; добавки синефрина не оказывают влияния на повышение содержания октопамина в моче
Является одним из средств для сжигания жировых тканей. Хорошо комбинируется с:
- Нарингенином и, возможно, с гесперидином
Синефрин: инструкция по применению
Рекомендуемая дозировка 10-20 мг, принимать три раза в день. Также часто используются дозировки в 50 мг, однако их не принимают 3 раза в день.
Источники и структура
Источники синефрина
P-синефрин (p-гидрокси-α-{метиламинометил} бензиловый спирт) является составной частью протоалкалоидов и имеет характеристики аминов. Может производиться эндогенно в человеческом теле и в больших количествах содержится в померанце (горьком апельсине). Померанец (кислый апельсин) не является обычным фруктом. Употребляется, возможно, лишь в Иране из-за его горького и кислого вкуса (обычный апельсин - citrus sinensis - сладкий апельсин). P-синефрин также содержится в:
- Апельсине кислом (8848.8 мг/кг сухого веса; 96% от общего количества протоалкалоидов)
- Экстракте обычного апельсина кислого (71.5 г/кг или 7.1% сухого веса; 92.2% от общего количества протоалкалоидов)
Распространенность в природе
Синефрин, хотя и известен в качестве синтетического органического соединения, впервые был выделен в качестве натурального продукта из листьев различных цитрусовых деревьев, и в начале 1960-х годов Стюарт и его сотрудники отметили его присутствие в составе различных цитрусовых соков. В 1970 году Уитон и Стюарт опубликовали обзор распределения синефрина среди высших растений. Впоследствии синефрин был обнаружен видах в Evodia и Zanthoxylum, растений из семейства Рутовые. Следовые количества (0,003%) синефрина были также обнаружены в составе высушенных листьев Pogostemon cablin (пачуля, Lamiaceae). Вещество также содержится в некоторых видах кактусов из родов Coryphantha и Dolichothele. Это соединение, однако, встречается преимущественно в ряде видов цитрусовых, в том числе «горьких» и «сладких» сортах.
Цитрусовые
Экстракты незрелых плодов из азиатских сортов померанца (широко известного как «горькие» апельсины) из Китая, как сообщалось, содержат синефрин на уровне примерно 0,1-0,3%, или ~ 1-3 мг/г. Анализ высушенных померанцев, выращенных в Италии, показал концентрацию синефрина ~ 1 мг / г, при этом в кожуре содержалось в три раза больше вещества, чем в мякоти. Сладкие апельсины сортов Tarocco, Naveline и разные виды Naveline, приобретенные на итальянском рынке, содержат синефрин в объеме ~ 13-34 мкг / г (что соответствует 13-34 мг / кг) (с примерно равной концентрацией в соке и мякоти). На основании этих результатов, было подсчитано, что в одном «среднем» апельсине Tarocco содержится ~ 6 мг синефрина. Анализ 32 выжимок различных апельсинов в основном в США и Великобритании с включением образцов из Франции, Италии, Испании и Ливана, показал, что уровни синефрина в выжимке из горьких апельсинов составляли 0,05 - 0,0009 мг/г, а в выжимке из сладких апельсинов – 0,05 - 0,006 мг / г. Синефрин также содержится в мармеладе, изготовленном из цитрусовых уншиу (мандарин Сатсума) из Японии, в концентрации ~ 0,12 мг/г (или 2,4 мг/20 г порцию). Большинство апельсиновых мармеладов в США производится с использованием «сладких» апельсинов (С. sinensis), а «горькие» апельсины, или померанцы (С. aurantium) используются для изготовления более традиционных горьких мармеладов в Великобритании. В образце коммерческого японского сока C. unshiu содержится ~ 0,36 мг / г синефрина (или примерно 360 мг/л), в то время как в соках, полученных из различных видов мандарина Сацума, выращенных в Калифорнии, уровни синефрина варьировались от 55 до 160 мг / л. Соки из «сладких» бразильских апельсинов содержат ~ 10-22 мг / л синефрина; коммерческие апельсиновые безалкогольные напитки, купленные на бразильском рынке, содержат в среднем ~ 1 мг / л синефрина. Коммерческие итальянские апельсиновые соки содержат ~ 13-32 мг / л синефрина. В ходе анализа более 50 соков цитрусовых, изготовленных коммерчески или выжатых вручную из свежих фруктов, полученных на рынке США, было показано, что уровни синефрина в них составляли от ~ 4 - 60 мг / л; синефрин не был обнаружен в соках из грейпфрута, лайма или лимона. Анализ уровней синефрина в соках различных цитрусовых, выжатых из свежих очищенных фруктов, показал следующие результаты: сладкий апельсин Marrs (C. sinensis Tan.): ~ 85 мг / л; мандарин Нова (C. reticulata Tan.): ~ 78 мг / л ; клементин (C. clementina Tan.): ~ 115 мг / л; лимон Мейер (C. limon Tan.) ~ 3 мг / кг; ягли (C. reticulata × C. paradisi) ~ 47 мг / кг. Синефрина не было обнаружено в следующих сортах: грейпфрут Красный Рио (C. paradisi Macf.); паммело с красной мякотью (C. grandis Tan.); или Wekiwa Tangelo (C. reticulata × C. paradisi).
Содержание синефрина в организме человека и других животных
В моче здорового человека содержатся низкие уровни синефрина. Синефрин также содержится в других тканях млекопитающих. Чтобы уменьшить вероятность того, что синефрин в моче имеет диетическое происхождение, испытуемые воздерживались от потребления любых цитрусовых в течение 48 часов до предоставления образцов мочи. Недавнее исследование содержания синефрина в тромбоцитах крови человека показало повышенный уровень синефрина в тромбоцитах пациентов, страдающих мигренью (0,72 нг/108 тромбоцитов, по сравнению с 0,33 нг/108 тромбоцитов в контрольной группе). Ранее та же группа исследователей сообщила том, что нормальные уровни синефрина в плазме крови человека равны 0.90-13.69 нг / мл.
Биосинтез
Биосинтез синефрина в цитрусовых, предположительно, следует пути: тирозин → тирамин → N-метилтирамин → синефрин, с участием ферментов тирозиндекарбоксилазы в первом шаге, тирамин N-метилтрансферазы во втором, и N-метил-тирамин-β-гидроксилазы в третьем. Этот путь отличается от наблюдаемого у животных, включающего октопамин: тирамин → октопамин → синефрин, где конверсия тирамина в октопамин опосредуется допамин-β-гидроксилазой и превращение октопамина в синефрин – фенилэтаноламин N-метилтрансферазой.
Наличие в пищевых / диетических добавках
Некоторые пищевые добавки для снижения веса или энергетики содержат в своем составе синефрин. Как правило, синефрин присутствует в качестве естественного компонента померанца («горького апельсина»), связанного в матрице растений, но также может встречаться синефрин синтетического происхождения, или очищенный фитохимическим путем (т.е. извлеченный из растительного источника и очищенный до достижения химической однородности). Диапазон концентрации синефрина в пяти различных добавках, приобретенных в США, составлял около 5 -14 мг / г.
Структура
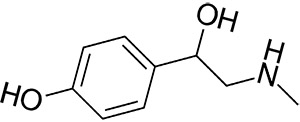 Термин «синефрин», как правило, противопоставляется парасинефрину или p-синефрину, а также двум другим вариантам, особенно метасинефрину (m-синефрину) и ортосинефрину (o-синефрину); считается, что они имеют подобные свойства, хотя p-синефрин – особая разновидность, содержащаяся в апельсине кислом, применяемой в китайской народной медицине (наряду с молекулой октопамина).
Термин «синефрин», как правило, противопоставляется парасинефрину или p-синефрину, а также двум другим вариантам, особенно метасинефрину (m-синефрину) и ортосинефрину (o-синефрину); считается, что они имеют подобные свойства, хотя p-синефрин – особая разновидность, содержащаяся в апельсине кислом, применяемой в китайской народной медицине (наряду с молекулой октопамина).
Стереоизомеры
Поскольку синефрин существует в виде одного из двух энантиомеров, которые не производят идентичных биологических эффектов, некоторые исследователи изучили стереоизомерный состав синефрина из природных источников. Хотя очевидно, что синефрин содержится в тех видах цитрусовых, которые изучались в основном как L-изомеры, низкие уровни d-синефрина были обнаружены в соке и мармеладе, произведенном из C. unshiu, и низкий уровень синефрина (0,002%) был зарегистрирован в составе свежих плодов С. aurantium. Существуют сведения о том, что некоторая часть d-синефрина может быть образована путем рацемизации L-синефрина в результате переработки свежих фруктов, хотя это вопрос до конца не выяснен. Тем не менее, вне зависимости от видов цитрусовых, Раньери и Маклафлин сообщили о выделении рацемического (т.е. смеси равных количеств D- и L-стереоизомеров) синефрина из кактуса рода Dolichothele, в условиях, которые не могли бы вызвать значительной рацемизации.
Фармацевтическое использование синефрина
В качестве синтетического препарата, синефрин впервые появился в Европе в конце 1920-х годов, под названием Sympatol. Одна из первых статей, описывающих его фармакологические и токсикологические свойства, была написана человеком по фамилии Lasch, который получил вещество от венской компании Syngala. К 1930 году Sympatol считался продукцией компании Boehringer, в то время как один из первых патентов США, описывающих его получение и использование, был передан компании Frederick Stearns&Co в 1933 году. Несмотря на сроки этого патента, клинические и фармакологические исследования синефрина от Frederick Fre Stearns&Co проводились в США в 1930 году. В 1931 году Гартунг сообщил, что в 1930 году Совет по Фармации и Химии Американской Медицинской Ассоциации принял синефрин для включения в список «новых и неофициальных средств» в качестве средства для лечения «приступов сенной лихорадки, астмы, кашля, спазмов астмы и коклюша» перорального или парентерального введения. В 1934 году, однако, синефрин был исключен из списка Совета, и его повторная реклама в качестве нового препарата от компании Stearns десять лет спустя вызвала резкую критику от редакции журнала Американской Медицинской Ассоциации. В третьем издании (1965 г.) «Фармакологии медицины» Дрилла было заявлено, с оговорками, что синефрин был «разрекламирован в качестве антигистаминного средства, которое может использоваться в лечении простуды», под торговым наименованием «Synephrin Tartrate», с указанием, что требуемая доза составляет 100 мг внутримышечно или подкожно. В опубликованном в 1966 году «Учебнике органической медицинской и фармацевтической химии» синефрин (в виде его рацемического тартрата) был описан в качестве симпатомиметического вещества, «менее эффективного, чем адреналин», которое использовалось для лечения хронической гипертонии, коллапса и других состояний, приводящих к гипотонии. В более поздней версии учебника (1972 г.) синефрин описывался в качестве лекарственного средства, продаваемого в Европе, применяемого в ситуациях, связанных с шоком, например, хирургический или бактериальный шок и спинальная анестезия, связанная с шоком. Рекомендуемая доза, принимаемая в этом случае, составляла 25-50 мг внутривенно, внутримышечно или подкожно. В более поздних изданиях «Фармакологии медицины» Дрилла нет упоминаний о синефрине. Нет также никаких ссылок на синефрин ни в «Настольном справочнике врача» 2012 года, ни в текущей «Оранжевой книге» FDA. Один из текущих источников описывает синефрин как сосудосуживающее средство, применяемое при гипотензии, перорально или инъекционно, в дозах 20-100 мг. Один из вебсайтов медицинской компании описывает окседрин как препарат для лечения гипотензивных состояний, применяемый перорально в дозах 100-150 мг три раза в день, и в качестве «конъюнктивного противоотечного средства», применяемого местно в виде 0,5%-ного раствора.
Названия
Существует некая путаница относительно биологических эффектов синефрина из-за сходства его названия с m-синефрином, мета-синефрином и неосинефрином, которые относятся к связанному препарату и натуральному амину, более известному как фенилэфрин. Хотя между синефрином и фенилэфрином существуют химические и фармакологические сходства, тем не менее, это разные вещества. Путаница усугубляется тем, что синефрин отпускался на рынок в качестве лекарственного средства под многочисленными торговыми наименованиями, в том числе Sympatol, Sympathol, Synthenate и Oxedrine, в то время как фенилэфрин также называется m-Sympatol. Синефрин, которому посвящена эта статья, иногда называют p-синефрин, чтобы отличать его от позиционных изомеров, m-синефрина и о-синефрина. Путаница различий между р- и m-синефрином присутствует даже в первичной исследовательской литературе.
Химия
Свойства
С точки зрения молекулярной структуры, синефрин имеет основу фенилэтиламина, с фенольной гидроксильной группой, спиртовой гидрокси-группой и N-метилированной аминогруппой. Кроме того, синефрин может быть описан как фенилэтаноламин с N-метил- и p-гидрокси заместителем. Аминогруппа передает молекуле основные свойства, а фенольная ОН-группа является слабокислой. Значение pKas для протонированного синефрина равно 9,55 (фенольный Н) и 9,79 (H аммония). Общими солями рацемического синефрина являются его гидрохлорид, C9H13NO2.HCl, t пл. 150-152°, оксалат (C9H13NO2) 2.C2H2O4, t пл. 221-222 ° С и тартрат (Sympatol), (C9H13NO2) 2.C4H6O6, t пл. 188-190 ° С. Наличие гидрокси-группы на бензильном участке C молекулы синефрина создает хиральный центр, таким образом, соединение существует в виде двух энантиомеров, D- и L-синефрина, или в виде рацемической смеси, D, L-синефрина. Правовращающий D-изомер соответствует S-конфигурации, а левовращающий l-изомер – R-конфигурации. Рацемический синефрин разлагается с использованием аммоний 3-бром-камфора-8-сульфоната. Эти энантиомеры не характеризуются как их свободные основания, однако превращаются в гидрохлоридные соли, со следующими свойствами: S- (+)- C9H13NO2.HCl : т. пл 178 ° С; [ α ] = 42,0 ° , с 0,1 (H2O ) ; R- (-)- C9H13NO2.HCl : т. пл 176 ° С; [ α ] = -39,0 ° , с 0,2 (H2O) (-)-синефрин, в виде свободного основания, выделенный из цитрусового источника, имеет т.пл. 162-164 ° C (с разложением).
Структурные Отношения
В литературе описывается структурное родство синефрина с эфедрином или с фенилэфрином, и часто подразумевается, что предполагаемые сходства в структуре должны приводить к сходству фармакологических свойств. Тем не менее, с химической точки зрения, синефрин также связан с большим количеством других лекарственных средств, структура которых основана на структуре фенэтиламина, и, несмотря на сходство некоторых свойств, имеется масса отличий, что делает нецелесообразным какие-либо сравнения и обобщения. Таким образом, благодаря замене N-метильной группы в синефрине на атом водорода создается октопамин; благодаря замене β-гидрокси группы в синефрине на атом Н создается N-метилтирамин; замена фенольной 4-ОН группы на -H дает галостацин. При смещении фенольной 4-ОН группы синефрина на мета- или 3-положение в бензольном кольце, соединения, создается соединение, известное как фенилэфрин (или m-синефрин, или «Нео-синефрин»); если же группа смещается в орто- или 2-позицию на кольце, создается о-синефрин. Добавление другой фенольной -OH группы на 3 позицию бензольного кольца производит нейротрансмиттер эпинефрин; добавление метильной группы на α-положение боковой цепи синефрина дает оксилофрин (или «метилсинефрин») (хотя следует отметить, что для этого вещества возможны четыре стереоизомера и две рацемические модификации). Расширение заместителя синефрин N-метила при помощи одной метиленовой группы до N-этила создает гипотензивный экспериментальный препарат «Стерлинг # 573»/«Aethyl -Sympatol». Приведенные выше структурные связи влекут за собой изменение в одном положении в молекуле синефрина, и возможны многочисленные другие подобные изменения, многие из которых были изучены. Однако, структура эфедрина отличается от структуры синефрина в двух различных положениях: эфедрин не имеет заместителя на фенильном кольце, где синефрин имеет группу 4-ОН, и эфедрин имеет метильную группу в положении α- к N на боковой цепи, где синефрин имеет только атом H. Кроме того, «синефрин» существует в виде одного из двух энантиомеров, а «эфедрин» существует в виде одного из четырех различных энантиомеров; кроме того, существуют рацемические смеси этих энантиомеров. Основные отличия изомеров синефрина от, например, эфедрина, составляют гидрокси-замещения на бензольном кольце. Синефрины являются прямыми симпатомиметическими препаратами, в то время как эфедрины могут быть как прямыми, так и косвенными симпатомиметиками. Одной из главных причин этих дифференциальных эффектов, очевидно, является увеличение полярности гидрокси-замещенных фенилэтиловых аминов, что снижает их способность проникать через гематоэнцефалический барьер, как было показано на примерах тирамина и аналогов амфетамина.
Фармакология
 Классические фармакологические исследования на животных и изолированных тканях животных показали, что основные действия парентерально вводимого синефрина включают повышение кровяного давления, расширение зрачков и сжатие периферических кровеносных сосудов.
В настоящее время существует достаточно доказательств того, что синефрин производит большую часть биологических эффектов, действуя как агонист (то есть стимулятор) а-адренорецепторов, с отчетливым предпочтением α1 над α2 подтипом. Однако, активность синефрина на этих рецепторах является относительно низкой (т.е. для их активации требуются относительно большие концентрации препарата). Эффективность синефрина на адренергических рецепторах β-класса (независимо от подтипа) значительно ниже, чем на α-рецепторах. Существует ряд доказательств того, что синефрин также имеет слабую активность на 5-НТ рецепторах, и что он взаимодействует с TAAR1.
Как и практически у всех других простых фенилэтаноламинов (β-гидрокси-фенэтиламины),R-(-) - или L-, энантиомер синефрина является более мощным, чем S-(+)- или d-энантиомер, в большинстве, но не во всех, анализах. Тем не менее, большинство исследований было проведено с использованием рацемической смеси двух энантиомеров.
Классические фармакологические исследования на животных и изолированных тканях животных показали, что основные действия парентерально вводимого синефрина включают повышение кровяного давления, расширение зрачков и сжатие периферических кровеносных сосудов.
В настоящее время существует достаточно доказательств того, что синефрин производит большую часть биологических эффектов, действуя как агонист (то есть стимулятор) а-адренорецепторов, с отчетливым предпочтением α1 над α2 подтипом. Однако, активность синефрина на этих рецепторах является относительно низкой (т.е. для их активации требуются относительно большие концентрации препарата). Эффективность синефрина на адренергических рецепторах β-класса (независимо от подтипа) значительно ниже, чем на α-рецепторах. Существует ряд доказательств того, что синефрин также имеет слабую активность на 5-НТ рецепторах, и что он взаимодействует с TAAR1.
Как и практически у всех других простых фенилэтаноламинов (β-гидрокси-фенэтиламины),R-(-) - или L-, энантиомер синефрина является более мощным, чем S-(+)- или d-энантиомер, в большинстве, но не во всех, анализах. Тем не менее, большинство исследований было проведено с использованием рацемической смеси двух энантиомеров.
Фармакологические исследования
Фармакологические исследования синефрина начались еще в конце 1920-х годов, когда было обнаружено, что при инъекционном введении синефрин вызывает повышение кровяного давления, сужение периферических кровеносных сосудов, расширение зрачков, стимуляцию матки и расслабление кишечника у экспериментальных животных. Авторами этой ранней работы являются Тэйнтер и Сайденфелд, которые были первыми исследователями, осуществившими систематическое сравнение различных эффектов двух энантиомеров синефрина, D- и L-синефрина, а также рацемата, d- и l-синефрина, в различных анализах на животных. В опытах на анестезированных кошках, Тэйнтер и Сайденфелд подтвердили ранние доклады повышения артериального давления при применении внутривенных доз синефрина, показав, что средними прессорными дозами для изомеров были: l-синефрин: 0,5 мг / кг; d, l-синефрин: 1,0 мг / кг; и d-синефрин: 2-20 мг / кг. Эти эффекты длились 2-3 минуты, достигая максимума через ~ 30 секунд после введения. Таким образом, l-синефрин был более мощным энантиомером, обладая около 1/60 х потенции стандартного L- адреналина в этом же тесте. В более позднем исследовании Лэндса и Гранта было показано, что доза ~ 0,6 мг / кг рацемического синефрина, при внутривенном введении собакам под наркозом, производит повышение артериального давления на 34 мм РТ, длящееся 5-10 минут, и предполагается, что эта компрессорная активность составляет около 1/ 300 х активности адреналина. В опытах на кошках и собак, Тэйнтер и Сайденфелд отметили, что ни d-, ни l-синефрин не вызывают никаких изменений в тоне бронхов in situ, даже при «максимальных» дозах. Кроме того, отмечаемое сужение бронхов после инъекций гистамина не обращалось при приеме l-синефрина или d, l- синефрина. В опытах с изолированной сонной артерией овец, d-, l- и d, l-синефрин проявляли некоторое сосудосуживающее действие. l-синефрин был самым мощным веществом, производящим сильные сокращения артерии при концентрациях 1:10000. d-синефрин обладал приблизительно ½ потенциала l-изомера, однако d, l-синефрин (который, как можно было бы ожидать, имеет 1/2 потенции l-синефрина, даже при полной неактивности d-изомера) не вызывал значительных и нерегулярных сокращений, пока его концентрация не достигала 1:2500, что предполагает наличие ингибирующего взаимодействия между двумя энантиомерами. Качественно аналогичные результаты были получены в препарате из уха кролика: 25 мг l-синефрина вызывали значительное (50%) сужение сосудов, в то время как та же концентрация d-синефрина не вызывала, по существу, никакого ответа. В противоположность этому, d, l-синефрин не производил никакого сужения при приеме дозы до 25 мг, а в дозе 25-50 мг вызывал релаксацию кровеносных сосудов, что вновь дает основание предполагать, что l-изомер может ингибировать действие d-изомера. Эксперименты на участках двенадцатиперстной кишки кролика показали, что l-синефрин вызывает небольшое снижение сокращений при концентрациях 1:17000, но что эффекты d- и d, l-форм были гораздо слабее. Рацемический синефрин, при внутримышечном приеме или при приеме путем инстилляции значительно снижает воспаление, вызванное закапыванием горчичного масла в глаза кроликов. Подкожное введение рацемического синефрина в кроликов вызывало большое повышение уровня сахара в крови. В опытах на анестезированных кошках, Papp и Szekeres обнаружили, что синефрин (стереохимия не указана) увеличивает пороги фибрилляции предсердий и желудочков, что указывает на антиаритмические свойства вещества. Доказательства того, что синефрин может производить некоторые центральные эффекты, имеются в исследованиях Сонга и коллег, изучавших эффекты синефрина в мышиных моделях антидепрессантной активности. Эти исследователи отметили, что пероральные дозы 0,3 - 10 мг / кг рацемического синефрина, были эффективны в сокращении продолжительности неподвижности, но не вызывали никаких изменений в спонтанной двигательной активности в отдельных тестах. Эта неподвижность может быть нейтрализована при предварительном введении празозина. Последующие эксперименты с использованием отдельных энантиомеров синефрина показали, что, хотя d-изомер значительно сокращает продолжительность неподвижности в тесте подвешивания за хвост, при пероральной дозе 3 мг / кг, l-изомер не оказывает влияния при приеме в той же дозе. У мышей, предварительно обработанных резерпином, пероральная доза 0,3 мг / кг d-синефрина значительно обращала гипотермию, в то время как для проявлении эффективности l-синефрина требовалась доза 1 мг / кг. Эксперименты с кусочками коры головного мозга, взятых из мозга крысы, показали, что d-синефрин ингибирует поглощение [3H]- норадреналина с IC50 = 5,8 мкМ; l-синефрин был менее мощным (IC50 = 13,5 мкм). d-синефрин также конкурентно ингибирует связывание низоксетина с кусочками коры головного мозга крыс, с Ki = 4,5 мкм; l-синефрин был менее мощным (Ki = 8,2 мкМ). В экспериментах по выпуску [3H]-норадреналина из кусочков коры головного мозга крыс, однако, l- изомер синефрина был более мощным усилителем выпуска (EC50 = 8,2 мкМ), чем d-изомер (EC50 = 12,3 мкМ). Этот усиленный выпуск l-синефрина блокировался низоксетином. Burgen и Iversen, рассматривая действия широкого диапазона препаратов на основе фенэтиламина на поглощение [14C]-норадреналина в изолированном сердце крысы, отметили, что рацемический синефрин [n] был относительно слабым ингибитором (IC50 = 0,12 мкМ) поглощения. Другое рецептор-ориентированное исследование показало, что синефрин (стереохимия не указана) был более сильнодействующим агонистом α1 -рецепторов аорты морской свинки (pD2 = 4,81), по сравнению с α2-рецепторами в подвздошной кишке (pD2 = 4,48), с соотношением относительной аффинности α2/α1 = 0,10. Указывая на селективность синефрина для α1-рецепторов, его активность в этом рецепторном подклассе все еще является относительно низкой, по сравнению с фенилэфрином (pD2 на α1 = 6,32). Браун и его коллеги исследовали влияние отдельных энантиомеров синефрина на α1 рецепторы в аорте крысы, и на α2 рецепторы в подкожной вене кролика. При подготовке аорты, l-синефрин давал pD2 = 5,38 (потенция относительно норадреналина = 1/1000), а d-синефрин имел pD2 = 3,50 (потенциал относительно норадреналина = 1/50000). Для сравнения, l-фенилэфрин имел pD2 = 7,50 (потенция относительно норадреналина ≃ 1/6). Никакого антагонизма норадреналина не наблюдалось при концентрации l-синефрина до 10-6 М. В подкожном анализе кроликов, pD2 l-синефрина была равна 4,36 (потенция по отношению к норадреналину ≃ 1/1700), а d-синефрина < 3,00; в сравнении, l-фенилэфрин имел pD2 = 5,45 (потенция по отношению к норадреналину ≃ 1/140). Никакого антагонизма норадреналина при концентрациях l-синефрина до 10-5 М не наблюдалось. Изучение действия синефрина (стереохимия не указана) на полоски аорты морской свинки и на поле-стимулированную подвздошную кишку морской свинки показали, что синефрин имеет потенцию агониста -logKa = 3,75 в анализе аорты. Для сравнения, адреналин имел активность -logKa = 5,70. Синефрин не оказывал никакого существенного влияния на подвздошную кишку при концентрациях до примерно 2х10-4М, что указывает на селективность в отношении рецептора α1, но относительно низкую активность. В экспериментах по связыванию с центральными адренорецепторами, с использованием коры головного мозга крыс, l-синефрин имел pIC50 = 3,35 и d-синефрин – pIC50 = 2,42 в конкуренции с [3H]- празозином (α1 стандартный лиганд); с [3H]- йохимбином (стандартный α2 лиганд), l-синефрин демонстрировал pIC50 = 5,01, а d-синефрин pIC50 = 4,17. Эксперименты, проведенные Хибино и сотрудниками, также показали, что синефрин (стереохимия не указана) производил дозозависимое сужение изолированных полос аорты крысы, в диапазоне концентраций 10-5-3х10-6 М. Это сужение конкурентно антагонизируется празозином (стандартный антагонист α1) и кетансерином [о], при этом празозин является более сильным антагонистом (pA2 = 9,38, против pA2 = 8,23 для кетансерина). Сужение синефрина также антагонизируется BRL-15, 572, но не SB-216, 641 или пропранололом. В исследованиях на предсердии и трахее морской свинки, Джоран и сотрудники также обнаружили, что синефрин незначительно действует на β1 и β2 рецепторы, будучи приблизительно в 40000 раз менее активен, чем норадреналин. Эксперименты с культивируемыми белыми жировыми клетками из нескольких видов животных, в том числе человека, показали, что рацемический синефрин производит липолитические эффекты, но лишь при высоких концентрациях (0,1-1 мм). Потенция синефрина у этих видов, выражаемая через pD2, был следующей: крыса: 4.38; хомяк: 5.32; морская свинка: 4.31; человек: 4,94. Для сравнения, в белых жировых клетках человека pD2 изопреналина = 8,29, а pD2 норадреналина = 6.80. Липолитический эффект 1 мМ / л синефрина в белый жировых клетках крыс антагонизировалось различными β-антагонистами со следующими значениями ингибирующей концентрации (IC50): бупранолол [P]: 0,11 мкм; CGP-20, 712A (β1 антагонист): 6,09 мкм; ICI -118, 551 (β2 антагонист): 3,58 мкм; SR- 5923A (β3 антагонист): 17 мкм. Было рассмотрено связывание рацемического синефрина с клонированными адренергическими рецепторами человека: Ма и его коллеги обнаружили, что синефрин связывается с α1A, 2а и α2C с низким сродством (PKI = 4,11 для α1A; 4.44 для 2а; 4.61 для α2C). Синефрин действовал как частичный агонист α1A рецепторов, но как антагонист 2а и α2C подтипов. Рацемический синефрин действует как агонист TAAR1, хотя его активность на человеческом TAAR1 является относительно низкой (EC50 = 23700 нм; Emax = 81,2%).
Фармакокинетика
Пиковые концентрация синефрина в плазме наблюдаются через 1-2 часа, и период полувыведения (Т1 / 2) составляет ~ 2 часа.
Метаболизм
Исследования метаболизма синефрина при помощи моноаминоксидаз, полученных из митохондрий головного мозга крыс, показали, что синефрин является субстратом для дезаминирования МАО-А и МАО-В, с Km = 250 мкМ и Vmax = 32,6 нм / мг белка/30 минут; были обнаружены некоторые доказательства для предпочтительного дезаминирования МАО-А. Синефрин, как известно, является эндогенным продуктом метаболизма октопамина, особенно его N-метилированная производная; его синтез был обнаружен в мозге крысы, и он был обнаружен в человеческой моче, независимо от добавок или приема пищи. Синефрин – эндогенно произведенный конечный продукт метаболизма тирамина, поскольку тирамин в процессе метаболизма превращается в октопамин (другая подобная аминокислота), который далее окисляется в синефрин. Синефрин - основа для ферментов моноаминной оксидазы (MAO) (Km на 250мкм и Vmax 32.6нм/мг протеина/30 мин), метаболизируется больше МАО-А, чем MAO-B (подобно его родительской молекуле октопамину). Окисление октопамина в синефрине, а также окисление самого синефрина, происходит через ферменты MAO и главным образом MAO-A.
Выведение из организма
Употребление в пищу добавок синефрина до 150 мг, без указаний на время приема, увеличивает уровень октопамина согласно с LOQ тестом, проведенного в течении 24 часов после единократного приема; это существенно, поскольку октопамин запрещен Всемирной антидопинговой организацией, хотя синефрин – разрешен, и сам октопамин может быть обнаружен после приема в пищу добавок октопамина.
Действие синефрина на человека
С момента выведения синефрина на рынок в качестве синтетического препарата, около 1930 года, был проведен ряд исследований действия синефрина на человека, большая часть которых касалась его воздействия на сердечнососудистую систему. В статье Стоктона и сотрудников описываются эффекты рацемического синефрина на человека, с особым вниманием на различия, возникающие из-за различных путей введения. Таким образом, в исследованиях было показано, что внутримышечные инъекции (средняя эффективная доза = 200 мг) препарата вызывают повышение систолического кровяного давления и частоты пульса, не влияя на диастолическое давление. Увеличение кровяного давления достигало максимума (~ 25 мм рт.ст.) в течение 5 минут после инъекции, а затем постепенно возвращалось к норме в течение 1 часа. При приеме препарата в дозах больше 200 мг наблюдались побочные эффекты, такие как учащенное сердцебиение, головная боль, потливость и чувство тревожности. При внутривенном введении дозы в 25-50 мг производили средний максимальный рост кровяного давления от 29 мм рт через 2 минуты, и возвращались к исходным в течение 30 минут. Дыхание во время этих экспериментов никак не изменялось. Подкожное введение синефрина в дозах ≤ 200 мг не оказывало никакого влияния на кровяное давление или частоту пульса. Пероральные дозы 500-1500 мг препарата не оказывали влияния на кровяное давление или дыхание, но пульс увеличивался на ~ 12%, а более высокие дозы вызывали тошноту и рвоту. Внутримышечное применение 75 - 500 мг синефрина не облегчает острых приступов астмы, что противоречит более ранним заявлениям производителя. Тем не менее, местное применение 1-3%-ных растворов препарата на слизистую оболочку носа пациентов с синуситом производило благоприятное сужение без местного раздражения. Более позднее исследование показало, что применение синефрина путем непрерывной внутривенной инфузии, в дозе 4 мг / мин, значительно увеличивает среднее артериальное и систолическое давление, не затрагивая диастолического давления и частоты сердечных сокращений. Имеется целый ряд исследований, посвященных эффектам пищевых добавок и травяных лекарств, содержащих синефрин в качестве одного из многих различных химических ингредиентов.
Неврология
Головная боль и мигрень
Синефрин эндогенно производится как продукт метаболизма тирамина, поскольку он должен быть декарбоксилирован в растениях из тирамина, чтобы преобразоваться в синефрин (выпустить углекислый газ). Синефрин, а также другие подобные амины (тирамин, октопамин) могут быть обнаружены в плазме в количестве намного большем, чем у людей с кластерными головными болями и мигренями. Уровень синефрина определенно выше у людей с мигренью с аурой (0.72 +/-0.44нг/ 108 тромбоцитов), чем при мигрени без ауры (0.37 +/-0.29нг/ 108 тромбоцитов), что подобно контрольной группе здоровых людей (0.33 +/-0.25нг/ 108 пластинки). Метаболизм подобных аминов (на основе тирамина) нарушается при мигрени, и из-за этого концентрации синефрина могут быть выше, чем у людей без мигрени или тех, у которых наблюдается мигрень, но без ауры.
Здоровье сердечно-сосудистой системы
Кровяное давление
Единократно принятая доза 50 мг p-синефрина у здоровых людей в состоянии покоя в течение 75 минут значительно не влияет ни на кровяное давление, ни сердечный ритм.
Ожирение и жировые отложения
Скорость метаболизма
Единократно принятая доза 50 мг p-синефрина, принятая здоровыми особями в состоянии покоя в последующие 75 минут, увеличила процесс метаболизма на 65 ккал, но без какого-либо влияния на кровяное давление или когнитивную способность.
Механизмы
P-синефрин – это симпатомиметический компонент, подобный эфедрину. Он способен повышать скорость метаболизма через увеличение расщепление жиров и интенсивности метаболизма. Эти эффекты в большинстве случаев независимы от диеты и могут пассивно увеличивать интенсивность метаболизма, обеспечивая процесс потери веса за длительный период времени. Синефрин также проявляет характеристики альфа-адренергического антагониста. Воздействует как на A1, так и на A2 рецепторы, хотя с различной силой. В случаях как альфа, так и в бета-агонизма, эффекты обеих форм синефрина намного меньше, чем у норадреналина.
Исследования на людях
Было отмечено увеличение термического эффекта еды, но одно исследование показало, что данный эффект наблюдается только у женщин.
Взаимодействия питательных веществ
Флавоноиды цитрусовых (Нарингенин и Гесперидин)
50 мг p-синефрина могут увеличивать скорость метаболизма на 65 ккал больше, чем плацебо (который показал уменьшение на 30 ккал; измерения, проведенные в голодном состоянии в течение 75 минут), и добавка в виде 600 мг нарингенина увеличивает эту скорость метаболизма на 129 ккал и при употреблении 100 мг гесперидина вышеупомянутые компоненты могут снова увеличить скорость метаболизма до 183 ккал; потребление более высокого полного уровня геспердина (1000 мг) с вышеупомянутыми дозами p-синефрина и нарингенина привело к меньшему увеличению скорости метаболизма на 79 ккал.
Кофеин
Как и эфедрин, p-синефрин также показывает совместное действие с кофеином и более выражен у наивных потребителей кофеина (не развивших толерантности).
Токсикология
Общая информация
P-синефрин не повышает кровяное давление. Сам померанец (исходное растение) может вызывать увеличение систолического и диастолического кровяного давления. В то время, как общая запатентованная смесь p-синефрина, известная как Xenadrine EFX (содержащая лишь 5.5 мг синефрина), увеличивает кровяное давление, другая запатентованная смесь, Advantra-Z (которая содержит значительно более высокую дозу синефрина в количестве 46.9 мг, наряду с активными биофлавонидами, такими как наринген и гесперидин) не оказывает влияния на кровяное давление. Обе смеси увеличивают сердечный ритм в сравнении с исходными показателями (16.7 и 11.7 ударов в минуту соответственно). В целом, использование p-синефрина достаточно безопасно и не связано с большинством неблагоприятных побочных эффектов.
Допинг-контроль
P-синефрин не показывает ложноположительных результатов допинг-контроля (при тестировании амфетаминов CEDIA) после приема в пищу 54 мг p-синефрина через потребление 900 мг экстракта апельсина горького.
Острая токсичность рацемического синефрина у различных животных (измеряемая в терминах «максимально переносимая доза») после подкожного введения, была следующей: мышь: 300 мг / кг; крыса: 400 мг / кг ; морская свинка : 400 мг / кг. «Смертельные дозы», применяемые подкожно, равнялись: мышь: 400 мг / кг; крыса: 500 мг / кг ; морская свинка: 500 мг / кг. В другом исследовании этого соединения, применяемого внутривенно у мышей, LD50 = 270 мг / кг. «Субхроническая токсичность» синефрина была признана низкой у мышей, после введения пероральной дозы 30 и 300 мг / кг в течение 28 дней, в недавнем исследовании, использующем современную методологию. Как правило,лечение не приводит к значительным изменениям в биохимических или гематологических показателях, или в относительной массе органов, но отмечались некоторые изменения в концентрациях глутатиона и в активности глутатионпероксидазы.
Безопасность / Эффективность / Полемика
Информация о безопасности и эффективности синефрина, по большому счету, не утверждена. Тем не менее, существует значительное противоречие о безопасности и / или эффективности синефрин-содержащих препаратов , которые часто путают с синефрином в отдельности, иногда с m-синефрином, и в медицинской литературе и в Интернете имеется много информации о таких препаратах.
Воздействие синефрина на беспозвоночных
 У насекомых синефрин действует как очень сильный агонист на многих октопаминовых рецепторах беспозвоночных, действуя даже более мощно, чем октопамин, на нервно-мышечную систему саранчи (Schistocerca americana gregaria). Синефрин (рацемический) также является более мощным, чем октопамин (рацемический) в потенциировании светового излучения у светлячка (виды Photinus). Синефрин проявляет одинаково высокую потенцию в стимулировании активности аденилатциклазы и в уменьшении времени свертывания в гематоцитах омара (Homarus americanus). Рацемический синефрин вызывает увеличение цАМФ в брюшном эпидермисе кровососущих жуков Rhodnius prolixus. Рачинский сообщил, что синефрин обладает равной октопамину активностью в стимулировании выпуска ювенильного гормона у пчел (Apis Mellifera), но Вудринг и Хоффманн обнаружили, что синефрин не воздействует на синтез ювенильного гормон III у сверчка Gryllus bimaculatus.
У насекомых синефрин действует как очень сильный агонист на многих октопаминовых рецепторах беспозвоночных, действуя даже более мощно, чем октопамин, на нервно-мышечную систему саранчи (Schistocerca americana gregaria). Синефрин (рацемический) также является более мощным, чем октопамин (рацемический) в потенциировании светового излучения у светлячка (виды Photinus). Синефрин проявляет одинаково высокую потенцию в стимулировании активности аденилатциклазы и в уменьшении времени свертывания в гематоцитах омара (Homarus americanus). Рацемический синефрин вызывает увеличение цАМФ в брюшном эпидермисе кровососущих жуков Rhodnius prolixus. Рачинский сообщил, что синефрин обладает равной октопамину активностью в стимулировании выпуска ювенильного гормона у пчел (Apis Mellifera), но Вудринг и Хоффманн обнаружили, что синефрин не воздействует на синтез ювенильного гормон III у сверчка Gryllus bimaculatus.
Доступность
Синефрин используется как препарат для сжигания жира. Входит в состав множества спортивных добавок. Считается заменителем эфедрина.
:Tags
Читать еще: Ацекор (Ацебутолол) , Занамивир , Кишечная непроходимость , Остеомаляция , Цераксон (Цитиколин) ,










