Инструменты пользователя
Инструменты сайта
- Life support
- Афродизиаки
- Липолитические (жиросжигающие) средства
- Ноотропные средства
- Нейропротекторы
- Снотворные средства
- Спортивная медицина
- Гормоны и гормональные препараты
- Анаболические/андрогенные стероиды
- Пептиды
- Селективные модуляторы андрогенных рецепторов (SARM/САРМ)
- Аминокислоты
- Витамины
- Растения
- Алкалоиды
- Лечение
- Что лечим
- Анальгетические средства
- Антибиотики
- Антигистаминные препараты
- Антидепрессанты
- Антикоагулянты
- Антисептические средства
- Диуретики
- Небензодиазепины (Z-препараты)
- Нейролептики
- Препараты, применяемые при химиотерапии
- Нестероидные противовоспалительные препараты
- Противогрибковые средства
- Противокашлевые препараты
- Противоопухолевые препараты
- Противорвотные средства
- Противосудорожные средства
- Все страницы
Содержание
Ревматоидный артрит
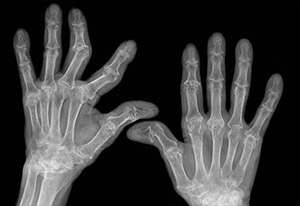 Ревматоидный артрит (РА) представляет собой хроническое, системное воспалительное заболевание, которое преимущественно воздействует на суставы.[1] Оно может привести к деформированным и болезненным суставам, что может вызвать утрату функционирования. Заболевание также может проявлять признаки и симптомы в отношении органов помимо суставов.
Причина РА полностью не установлена. Процесс охватывает воспаление и фиброз мембраны вокруг суставов. Также оказывает действие на лежащую под ней кость и хрящ.[1] РА может вызывать диффузное воспаление в легких, мембраны вокруг сердца, мембран легкого и белков глаз. Также может создавать узловые поражения, наиболее часто встречающиеся на коже. Представляет собой клинический диагноз, который ставится большей частью на основе симптомов и физического обследования. Рентгенограмма, лабораторные анализы и анализ синовиальной жидкости могут подтвердить диагноз или исключить другие заболевания с похожими симптомами.[2]
Лечение включает как лекарственные препараты, так и нефармакологические меры – цель заключается в контроле за воспалением суставов и предотвращении повреждения сустава и недееспособности. Нефармакологическое лечение включает физическую терапию, шины и ордотонтические скобы, трудовую терапию и изменения рациона, но это не останавливает прогрессирование повреждения сустава. Болеутоляющие средства и противовоспалительные препараты, включая стероиды, подавляют симптомы, но не останавливают прогрессирование заболевания. Модифицирующие заболевание противоревматические препараты (DMARD) могут замедлить или остановить прогрессирование болезни.[2] Биологические DMARD, такие как анти-ФНО агенты, эффективны, но обычно избегаются людьми с активным заболеванием или гиперчувствительностью к данным агентам.[3] Они снижают количество болезненных или опухших суставов, а также облегчают боль и недееспособность, связанные с заболеванием, но имеется недостаточно данных относительно побочных действий.[4] Альтернативная медицина не поддерживается фактами.[5][6][7]
РА страдает приблизительно 0,5 и 1% взрослых в развитых странах, при этом у от 5 до 50 на 100000 людей каждый год впервые диагностируется заболевание.[8] Развитие заболевания чаще всего наблюдается в среднем возрасте, но ему подвержены люди любого возраста.[9] В 2013 г. оно вызвало 38000 летальных исходов по сравнению с 28000 смертей в 1990 г.[10] Название заболевания основывается на понятии «ревматизм», заболевании, которое характеризуется болью в суставах и получено от греческого слова ῥεύμα-ревма (им.), ῥεύματος-ревматос (род.) («поток, течение»). Суффикс -оид («напоминающий») получил перевод как воспаление суставов, которое напоминает ревматизм. Первое официальное описание РА было сделано в 1800 г. доктором Августином Джакобом Ландре-Бове (1772–1840) в Париже.[11]
Ревматоидный артрит (РА) представляет собой хроническое, системное воспалительное заболевание, которое преимущественно воздействует на суставы.[1] Оно может привести к деформированным и болезненным суставам, что может вызвать утрату функционирования. Заболевание также может проявлять признаки и симптомы в отношении органов помимо суставов.
Причина РА полностью не установлена. Процесс охватывает воспаление и фиброз мембраны вокруг суставов. Также оказывает действие на лежащую под ней кость и хрящ.[1] РА может вызывать диффузное воспаление в легких, мембраны вокруг сердца, мембран легкого и белков глаз. Также может создавать узловые поражения, наиболее часто встречающиеся на коже. Представляет собой клинический диагноз, который ставится большей частью на основе симптомов и физического обследования. Рентгенограмма, лабораторные анализы и анализ синовиальной жидкости могут подтвердить диагноз или исключить другие заболевания с похожими симптомами.[2]
Лечение включает как лекарственные препараты, так и нефармакологические меры – цель заключается в контроле за воспалением суставов и предотвращении повреждения сустава и недееспособности. Нефармакологическое лечение включает физическую терапию, шины и ордотонтические скобы, трудовую терапию и изменения рациона, но это не останавливает прогрессирование повреждения сустава. Болеутоляющие средства и противовоспалительные препараты, включая стероиды, подавляют симптомы, но не останавливают прогрессирование заболевания. Модифицирующие заболевание противоревматические препараты (DMARD) могут замедлить или остановить прогрессирование болезни.[2] Биологические DMARD, такие как анти-ФНО агенты, эффективны, но обычно избегаются людьми с активным заболеванием или гиперчувствительностью к данным агентам.[3] Они снижают количество болезненных или опухших суставов, а также облегчают боль и недееспособность, связанные с заболеванием, но имеется недостаточно данных относительно побочных действий.[4] Альтернативная медицина не поддерживается фактами.[5][6][7]
РА страдает приблизительно 0,5 и 1% взрослых в развитых странах, при этом у от 5 до 50 на 100000 людей каждый год впервые диагностируется заболевание.[8] Развитие заболевания чаще всего наблюдается в среднем возрасте, но ему подвержены люди любого возраста.[9] В 2013 г. оно вызвало 38000 летальных исходов по сравнению с 28000 смертей в 1990 г.[10] Название заболевания основывается на понятии «ревматизм», заболевании, которое характеризуется болью в суставах и получено от греческого слова ῥεύμα-ревма (им.), ῥεύματος-ревматос (род.) («поток, течение»). Суффикс -оид («напоминающий») получил перевод как воспаление суставов, которое напоминает ревматизм. Первое официальное описание РА было сделано в 1800 г. доктором Августином Джакобом Ландре-Бове (1772–1840) в Париже.[11]
Признаки и симптомы
РА преимущественно воздействует на суставы, тем не менее, также он оказывает влияние на другие органы у более чем 15–25% субъектов.[12]
Суставы
Артрит суставов включает воспаление синовиальной мембраны. Суставы становятся припухшими, болезненными и теплыми, а скованность ограничивает их движение. Со временем воздействию подвергаются множественные суставы (это носит название полиартрит). Наиболее часто заболеванию подвержены небольшие суставы рук, ступней и шейного отдела позвоночника, но также могут быть вовлечены более крупные суставы, такие как плечо и колено.[13]:1089 Синовит может привести к скованности ткани с утратой подвижности и эрозии поверхности сустава, вызывая деформирование и утрату функции.[2] РА обычно проявляется посредством признаков воспаления, при этом подверженные воздействию суставы становятся припухшими, теплыми, болезненными и скованными, в частности, утром при пробуждении или вследствие длительного бездействия. Повышенная скованность утром часто является преобладающей особенностью заболевания и, как правило, длится более часа. Плавные движения могут облегчать симптомы на ранних стадиях заболевания. Признаки помогают отличить ревматоидный артрит от невоспалительных проблем суставов, часто упоминающихся как остеоартрит или «артрит вследствие износа». При артрите с невоспалительными причинами признаки воспаления и утренняя скованность менее выражены, при этом скованность обычно длится меньше часа, а движения вызывают боль по причине механического артрита.[14] Боль, вызываемая ревматоидным артритом, вызывается в месте воспаления и классифицируется как ноцицептивная в противоположность невропатической.[15] Суставы часто подвергаются действию в достаточно симметричной манере, хотя это неспецифично, а первоначальное проявление может быть ассиметричным.[13]:1089 Так как патология прогрессирует, воспалительная активность приводит к скованности сухожилия и эрозии и разрушению поверхности сустава, что нарушает амплитуду движения и ведет к деформированию. Пальцы могут подвергаться практически любому деформированию в зависимости от того, какой сустав поле подвержен заболеванию. Специфические деформации, которые также возникают при остеоартрите, включают локтевое отведение кисти, контрактуру Вайнштейна, деформацию пальцев в виде шеи лебедя и «Z-образный палец.» «Z-образный палец» или «Z-образная деформация» заключаются в перерастяжении межфалангового сустава, пассивном сгибании и подвывихе пястно-фалангового сустава и принятии пальцем формы буквы «Z».[13]:1089 Может наблюдаться деформация, известная как молотообразный палец. В худшем случае заболевание носит название мутилирующий артрит в связи с калечащей природой деформаций.[1]
Кожа
Ревматоидный узелок, который в некоторых случаях бывает кожным, представляет наиболее характерную для РА особенность. Это тип воспалительной реакции, известной у патоморфологов как «некротизирующая гранулема». Изначальный патологический процесс в образовании узелка не известен, но может по существу быть аналогичным синовиту, поскольку обоим присущи сходные структурные особенности. В узелке имеется центральная зона фибриноидного некроза, которая может растрескиваться и соотносится с фибрин-обогащенным некротическим материалом, обнаруженным внутри и вокруг затронутого синовиального пространства. Некроз покрывается слоем окружающих макрофагов и фибробластов, относящихся к интимальному слою синовиальной мембраны и скопления клеток вокруг соединительной ткани, содержащей кластеры лимфоцитов и клеток плазмы, относящиеся к субинтимальному слою синовита. Типичный ревматоидный узелок может составлять от нескольких миллиметров до нескольких сантиметров в диаметре и обычно обнаруживается над костными выступами, такими как локоть, пятка, суставы пальцев, или в других зонах, которые выдерживают многократный механический стресс. Узелки связываются с положительным титром RF (ревматоидный фактор) и тяжелым эрозивным артритом. В редких случаях, узелки могут возникать на внутренних органах или различных тканях организма. При РА наблюдаются тяжелые формы васкулита. Доброкачественная форма возникает как микроинфаркты около ногтевого ложа. Более тяжелые формы включают сетчатое ливедо, которое представляет собой сеть (ретикулум) эритематозного багрянистого изменения цвета кожи, вызванного наличием облитерирующей кожной капилляропатии. Другие, скорее редкие, связанные с кожей симптомы, включают гангренозную пиодермию, синдром Свита, реакции на препараты, узелковую эритему, панникулит на выступающих частях, атрофию кожи пальцев, ладонную эритему, диффузное истончение (кожа, напоминающая рисовую бумагу) и слабость кожи (часто ухудшается при использовании кортикостероидов).
Легкие
Фиброз легких представляет собой определенную реакцию на ревматоидное заболевание. Он также является редким, но хорошо распознаваемым последствием терапии (например, лечения метотрексатом и лефлюномидом). Синдром Каплана описывает легочные узелки у субъектов с РА и дополнительным воздействием угольной пыли. Плевральные выпоты также связываются с РА. Другим осложнением РА является ревматоидная болезнь легких. Рассчитано, что примерно у четверти американцев с РА развивается ревматоидная болезнь легких.[16]
Почки
Может возникнуть почечный амилоидоз как последствие хронического воспаления.[17] РА может непосредственно воздействовать на гломерулу почки посредством васкулопатии или мезангиального инфильтрата, но это менее хорошо зарегистрировано документально (хотя это не удивительно, учитывая обусловленную иммунным комплексом гиперчувствительность, которая вызывает патогенное отложение иммунных комплексов в органах, где кровь фильтруется под высоким давлением в целях образования других жидкостей, таких как моча и синовиальная жидкость[18]). Лечение пеницилламином и тетрахлорозолото-кислым натрием вызывает мембранозную нефропатию.
Сердце и кровеносные сосуды
Люди с РА более предрасположены к атеросклерозу, также значительно повышен риск инфаркта миокарда (сердечный приступ) и инсульта.[19][20] другие возможные осложнения включают: перикардит, эндокардит, левожелудочковая недостаточность, вальвутит и фиброз.[21] Многие люди с РА не демонстрируют такой же боли в груди, которую чувствуют другие с ангиной или инфарктом миокарда. Чтобы снизить сердечно-сосудистый риск, важно поддерживать оптимальный контроль воспаления, вызванного РА (которое может иметь отношение к сердечно-сосудистому риску), и надлежащим образом применять физическую нагрузку и лекарственные препараты, чтобы снизить другие сердечно-сосудистые факторы риска, такие как уровень липидов в крови и кровяное давление. Врачи, лечащие пациентов с РА, должны учитывать сердечно-сосудистый риск при выписывании противовоспалительных лекарственных препаратов, также может потребоваться постоянное применение низких доз аспирина, если желудочно-кишечное действие переносимо.[21]
Другие
Глаза
Глаза подвержены прямому воздействию посредством эписклерита, который при тяжелой степени может, в очень редких случаях, прогрессировать до проникающей склеромаляции. Более часто встречается косвенное воздействие в форме сухого кератоконъюнктивита, который представляет собой сухость глаз и во рту, вызванную инфильтрацией лимфоцитов слезной и слюнной желез. В тяжелой степени сухость роговой оболочки может привести к кератиту и потере зрения. Важно профилактическое лечение тяжелой сухости посредством таких мер как блокирование носослезного протока.
Печень
Выработка цитокинов в суставных и/или гепатических (печеночных) купферовских клетках ведет к повышенной активности гепатоцитов с повышенной выработкой острофазных белков, таких как C-реактивный белок, а также повышенному высвобождению таких ферментов как алкалин фосфатаза в кровь. При синдроме Фелти активация купферовских клеток настолько значительна, что повышение активности гепатоцитов связывается с узловой гиперплазией печени, которая может быть значительно увеличенной. Хотя купферовские клетки находятся внутри печеночной паренхимы, они отделены от гепатоцитов. Как результат, наблюдаются мелкие или немикроскопические признаки гепатита (обусловленное иммунитетом разрушение гепатоцитов). Вовлечение печени в РА преимущественно бессимптомное.
Кровь
Анемия однозначно является наиболее широко распространенным патологическим нарушением клеток крови, которое может быть вызвано различными механизмами. Хроническое воспаление, вызванное РА, ведет к повышению уровня гепцидина, что вызывает анемию хронических заболеваний, когда железо плохо абсорбируется, а также блокируется в макрофагах. РА также вызывает тяжелую аутоиммунную гемолитическую анемию.[22] Красные клетки нормального размера и цвета (нормоцитарная и нормохромная анемия). Низкое количество белых кровяных клеток обычно наблюдается только у людей с синдромом Фелти и с увеличенной печенью и селезенкой. Механизм нейтропении является сложным. Высокий уровень тромбоцитов наблюдается в том случае, когда воспаление не контролируется.
Неврологические
Может возникнуть периферийная невропатия и множественный мононеврит. Наиболее распространенная проблема заключается в туннельном синдроме запястья, вызванном сжатием срединного нерва в результате отека вокруг запястья. Может наблюдаться атлантоаксиальный подвывих вследствие эрозии зубовидного отростка и/или поперечных связок в месте соединения шейного отдела позвоночника и челюсти. Такая эрозия (>3 мм) может вызывать проскальзывание позвонков друг через друга и сжатие спинного мозга. Сначала наблюдается неповоротливость, но без надлежащего ухода она может прогрессировать до квадриплегии.
Системные симптомы
Системные симптомы включают утомляемость, слабое проявление лихорадки, дискомфорт, утреннюю скованность, потерю аппетита и потерю веса как основные системные проявления, наблюдаемые у людей с РА.
Кости
Вокруг воспаленных суставов при РА возникает локальный остеопороз. Как утверждается, он отчасти связан с воспалительными цитокинами. Более общий остеопороз предположительно связывается с неподвижностью, системным действием цитокинов, локальным высвобождением цитокинов в костный мозг и кортикостероидной терапией.
Рак
При РА повышается встречаемость лимфомы, хотя это наблюдается редко.[23][24]
Причины
РА представляет собой хроническое аутоиммунное заболевание, причины которого до сих пор неполностью установлены. Это системное (действует на весь организм) заболевание, главным образом воздействующее на синовиальные ткани. Отсутствуют свидетельства, что физическое или эмоциональное воздействие или стресс могут быть инициирующим фактором для заболевания. Многие отрицательные результаты свидетельствуют, что либо инициирующий фактор варьируется, либо что он может быть в действительности случайным событием, свойственным иммунной реакции.[25] Половина факторов риска РА предположительно генетическая.[8] Он имеет сильную связь с наследственным типом ткани комплекс тканевой совместимости (MHC), антигеном HLA-DRB1 (точнее сказать, общими эпитопами аллелей, включая *0401 и *0404) и генами PTPN22 и PADI4—следовательно, семейная история представляет собой важный фактор риска.[26][27] Наследование гена PTPN22 удваивает предрасположенность человека к РА. PADI4 был определен как основной фактор риска для людей азиатского происхождения, но не для людей европейского происхождения.[28] Распространенность у родственников первой степени составляет 2–3%, а генетическая конкордантность заболевания у однояйцовых близнецов составляет примерно 15–20%.[29][30] Курение является наиболее значительным негенетическим фактором риска,[8] при этом РА в три раза чаще встречается у курильщиков, чем у некурящих, в частности, у мужчин, заядлых курильщиков и тех, кто положителен на ревматоидный фактор.[31] Умеренное употребление алкоголя может обладать защитным действием.[32] Эпидемиологические исследования подтвердили потенциальную связь между РА и двумя герпесвирусными инфекциями: вирусом Эпштейна-Барра (EBV) и вирусом герпеса человека типа 6 (HHV-6).[33] Субъекты с РА более вероятно демонстрируют атипичную иммунную реакцию на EBV и имеют высокий уровень анти-EBV антител.[34] Дефицит витамина D чаще встречается у людей с ревматоидным артритом, чем у общей совокупности населения.[35][36] Тем не менее, является ли дефицит витамина D причиной или последствием заболевания, остается неясным.[37] 1α,25-дигидроксивитамин D3 (1,25D), активный метаболит витамина D, косвенно оказывает влияние на костный метаболизм посредством контроля гомеостаза кальция и фосфата. Взаимодействие между 1,25D и рецептором витамина D (VDR) влияет на выработку RANKL и замедляет остеокластогенез.[38] Некоторые исследования выявили снижение риска РА за счет приема витамина D, в то время как другие нет.[36]
Патофизиология
 К патофизиологии болезни причастны как генетические факторы, так и факторы окружающей среды. Курение является основным риском окружающей среды в отношении ревматоидного артрита.[8] 50% факторов риска развития РА приписывается генетическим факторам.[8] Никакие инфекционные агенты закономерно не связаны с РА, при этом отсутствуют доказательства агрегации болезни, которые свидетельствовали бы о ее инфекционной этиологии.[39] HLA-DR4 является основным вовлеченным генетическим фактором – но его сравнительная значимость варьируется среди этнически групп.[39][40] Связанные аллотипы MHC класса II и T клеточный-связанный белок PTPN22 также демонстрируют связь во многих исследованиях .[40]
РА преимущественно начинается как состояние устойчивой клеточной активации, вызывая аутоиммунитет и иммунные комплексы в суставах и других органах, где он проявляется. Начальным местом проявления заболевания является синовиальная мембрана, где опухание и конгестия ведут к инфильтрации иммунными клетками. Различные фазы прогрессирования ревматоидного артрита включают:[1]
К патофизиологии болезни причастны как генетические факторы, так и факторы окружающей среды. Курение является основным риском окружающей среды в отношении ревматоидного артрита.[8] 50% факторов риска развития РА приписывается генетическим факторам.[8] Никакие инфекционные агенты закономерно не связаны с РА, при этом отсутствуют доказательства агрегации болезни, которые свидетельствовали бы о ее инфекционной этиологии.[39] HLA-DR4 является основным вовлеченным генетическим фактором – но его сравнительная значимость варьируется среди этнически групп.[39][40] Связанные аллотипы MHC класса II и T клеточный-связанный белок PTPN22 также демонстрируют связь во многих исследованиях .[40]
РА преимущественно начинается как состояние устойчивой клеточной активации, вызывая аутоиммунитет и иммунные комплексы в суставах и других органах, где он проявляется. Начальным местом проявления заболевания является синовиальная мембрана, где опухание и конгестия ведут к инфильтрации иммунными клетками. Различные фазы прогрессирования ревматоидного артрита включают:[1]
- Вступительную фазу, связанную с неспецифическим воспалением.
- Фазу амплификации, связанную с активацией T-клеток
- Хроническую воспалительную фазу с повреждением ткани, связанную с цитокинами ИЛ–1, ФНО-альфа и ИЛ–6.
Факторы, дающие возможность атипичной иммунной реакции, как только запущены, становятся устойчивыми и хроническими, а также все более ясно объяснимыми. Генетическая связь с HLA-DR4, а также только что открытая связь с геном PTPN22 и с двумя дополнительными генами[40] имеют отношение к измененным параметрам в регуляции адаптивной иммунной реакции. Из недавних исследований также становится ясно, что данные генетические факторы могут взаимодействовать с наиболее ясно изученным фактором риска окружающей среды в отношении РА под названием курение табака.[31][41] Другие факторы окружающей среды также модулируют риск приобретения РА, а гормональные факторы человека могут объяснять некоторые особенности заболевания, такие как более высокая встречаемость у женщин, довольно частое развитие после рождения ребенка, а также (незначительное) модулирование риска заболевания гормональными препаратами. Точная информация, как измененные регуляторные параметры дают возможность запуска специфической аутоиммунной реакции, остается неясной. Тем не менее, одна из возможностей заключается в том, что механизмы отрицательной обратной связи, которые обычно поддерживают самопереносимость, обгоняются аберрантными механизмами положительной обратной связи в отношении определенных антигенов, таких как иммуноглобулин G Fc (связанный ревматоидным фактором) и цитруллинированный фибриноген (связанный ACPA) (смотри вступление к статье аутоиммунитет). Споры в отношении сравнительных ролей иммунных комплексов и продуктов T-клеток в воспалении при РА длятся на протяжении 30 лет. Существует незначительное сомнение, что B- и T-клетки играют существенную роль в заболевании. Тем не менее, имеется надежное оказательство, что ни одна из клеток не является необходимой в месте воспаления. Это способствует иммунным комплексам (с использованием антител, синтезированных в других местах) в качестве инициаторов, даже если не единичным исполнителям воспаления. Наличие антител к иммуноглобулину GFc, известных как ревматоидные факторы (RF), а также антител к цитруллинированным пептидам (ACPA) представляет собой неотъемлемую часть течения РА. Как только атипичная иммунная реакция установилась (что может занять несколько лет до проявления симптомов), клетки плазмы, полученные из B лимфоцитов, вырабатывают ревматоидные факторы и ACPA иммуноглобулинов класса G и M в больших количествах. Они не откладываются таким же образом, как при системной волчанке. Скорее они активируют макрофаги посредством Fc рецептора и связывания комплемента, что играет важную роль в интенсивной воспалительной реакции, наблюдаемой при РА.[42] Это способствует воспалению синовиальной мембраны, которое включает отек, расширение кровеносных сосудов и инфильтрацию активированными T-клетками (в основном, CD4 в узелковых агрегатах и CD8 в диффузных инфильтратах). Синовиальные макрофаги и дендритные клетки в дальнейшем функционируют как антигенпредставляющие клетки за счет выраженности молекул MHC класса II, что ведет к устойчивой локальной иммунной реакции в тканях. Заболевание прогрессирует совместно с образованием грануляционной ткани по краям синовиальной выстилки (паннус) с избыточным ангиогенезом и выработкой ферментов, вызывающих повреждение ткани. Современные фармакологические методы лечения РА нацелены на данные медиаторы. Как только установилась воспалительная реакция, синовиальная мембрана утолщается, хрящ и лежащая под ним кость начинают разрушаться, возникает очевидное разрушение сустава. ФНО (альфа) играет важнейшую роль в патогенезе РА. Имеется несколько теорий относительно того, как высвобождение ФНО происходит в процессе болезни. Если высвобождение ФНО стимулируется продуктами B-клеток в форме RF или ACPA -содержащих иммунных комплексов, посредством активации Fc рецепторов иммуноглобулина, тогда оно может рассматриваться как форма гиперчувствительности типа III.[43][44] Если высвобождение ФНО стимулируется продуктами T-клеток, такими как интерлейкин-17, он может рассматриваться как близкий к гиперчувствительности типа IV, хотя данная терминология может быть в некоторой степени устаревшей и бесполезной.[45] Хотя ФНО является доминирующим фактором, другие цитокины (химические медиаторы), скорее всего, также причастны к воспалению РА. Блокирование ФНО не оказывает полезного действия на всех людей или все ткани (заболевания легких и узелки могут ухудшиться). Блокирование ИЛ-1, ИЛ-15 и ИЛ-6 также обладает полезным действием, может быть важен ИЛ-17. Системные симптомы, такие как жар, дискомфорт, потеря аппетита и потеря веса также вызвана высвобождением цитокинов в кровоток. Как и в отношении других аутоиммунных заболеваний, важно различать причины(у), которые запускают процесс, и причины, которые могут способствовать его устойчивости и прогрессированию.
Диагностика
Визуализация
Рентгенограмма рук и ступней, как правило, выполняется у людей со многими затронутыми суставами. При РА может не наблюдаться изменений на ранних стадиях заболевания либо рентгенограмма может показывать околосуставную остеопению, легкое опухание ткани и утрату суставной щели. Так как заболевание развивается, может наблюдаться эрозия костей и подвывих. Может выполняться рентгенограмма других суставов, если симптомы опухания и болезненности возникают в данных суставах. При РА также применяются другие медицинские техники визуализации, такие как магнитно-резонансная томография (МРТ) и ультразвуковое исследование.[1] Ультразвуковое исследование имеет свои технические преимущества. Высокочастотные преобразователи (10 МГц или выше) улучшают пространственное разрешение ультразвуковых изображений; данные изображения могут отображать на 20% больше эрозий, чем простая рентгенограмма. Кроме того, цветовое доплеровское и энергетическое доплеровское ультразвуковое исследование, которое показывает васкулярные сигналы активного синовита в зависимости от степени воспаления, полезно в определении синовиального воспаления. Это важно, поскольку на ранних стадиях РА синовиальная мембрана затрагивается в первую очередь, а синовит является лучшим прогностическим фактором будущего повреждения сустава.[46]
Анализы крови
При подозрении на РА может потребоваться анализ на наличие ревматоидного фактора (RF, неспецифического антитела) и ACPA.[47] Отрицательный результат на наличие ревматоидного фактора не исключает РА; скорее, артрит носит название серонегативный. Он охватывает случаи примерно 15% людей с РА.[48][49] В течение первого года болезни ревматоидный фактор наиболее вероятно отрицателен, при этом у некоторых субъектов он переходит в серопозитивное состояние спустя некоторое время. RF часто встречается при других заболеваниях, например, синдроме Шегрена, гепатите C, системной красной волчанке, хронических инфекциях и приблизительно у 10% здорового населения, таким образом, тест не является в достаточной степени специфичным.[1] По причине данной низкой специфичности был разработан новый серологический анализ, который представляет собой анализ на наличие антител антицитруллинированного белка (ACPA) или анти-CCP. Как и RF, данные анализы положительны только в определенной пропорции (67%) случаев РА, но редко бывают положительными, если РА отсутствует, что дает специфичность около 95%.[48] Как и в случае RF, существуют свидетельства относительно того, что ACPA представлены во многих случаях даже до начала клинического заболевания.[1] Наиболее распространенным анализом на ACPA является анти-CCP (циклический цитруллинированный пептид) анализ и анти-MCV анализ (антитела против мутирующего цитруллинированного виментина). Недавно был разработан тест на месте оказания медицинской помощи (POCT) для раннего выявления РА. Данный анализ объединяет оценку ревматоидного фактора и анти-MCV для диагностики РА и демонстрирует чувствительность в 72% и специфичность в 99,7%.[50][51] Кроме того, существует несколько других анализов крови, обычно выполняемых для выявления других причин РА, таких как эритематозная волчанка. На данной стадии выполняются анализы скорости оседания эритроцитов (СОЭ), C-реактивного белка, общий анализ крови, функции почек, ферментов печени и другие иммунологические тесты (например, антинуклеарные антитела/ANA). Повышенный уровень ферритина может выявить гемохроматоз, подражающий РА, либо быть признаком болезни Стилла, серонегативного, обычно ювенильного, варианта ревматоидного артрита.
Классификационные критерии
В 2010 г. были опубликованы Классификационные критерии ревматоидного артрита Американской коллегии ревматологии и Европейской антиревматической лиги.[52][53] Новые критерии не являются диагностическими критериями, но представляют собой классификационные критерии для выявления болезни с высокой вероятностью развития хронической формы.[1] Тем не менее, балл в 6 и выше однозначно характеризует человека с диагнозом ревматоидный артрит. Данные новые классификационные критерии аннулировали «старые» критерии Американской коллегии ревматологии 1987 г. и адаптированы для ранней диагностики РА. «Новые» классификационные критерии, совместно опубликованные Американской коллегией ревматологии (ACR) и Европейской антиревматической лигой (EULAR), установили стоимость балла от 0 до 10. Диагностика охватывает четыре области:[52]
1. Вовлечение суставов, распространяющееся на пястно-фаланговые суставы, проксимальные межфаланговые суставы, межфаланговый сустав большого пальца, со второго по пятый плюсне-фаланговые суставы и запястье как мелкие суставы, а также плечи, локти, тазобедренные суставы, колени и голеностопные суставы в качестве крупных суставов:
- Вовлечение 1 крупного сустава дает 0 баллов
- Вовлечение 2–10 крупных суставов дает 1 балл
- Вовлечение 1–3 мелких суставов (с или без вовлечения крупных суставов) дает 2 балла
- Вовлечение 4–10 мелких суставов (с или без вовлечения крупных суставов) дает 3 балла
- Вовлечение более 10 суставов (с вовлечением как минимум 1 мелкого сустава) дает 5 баллов
2. Серологические параметры – включая ревматоидный фактор, а также ACPA – «ACPA» означает «антитела против цитруллированного белка»:
- Отрицательный RF и отрицательные ACPA дают 0 баллов
- Низко-положительный RF или низко-положительные ACPA дают 2 балла
- Высоко-положительный RF или высоко-положительные ACPA дают 3 балла
3. Реактанты острой фазы: 1 балл за повышенную скорость оседания эритроцитов, СОЭ, или повышенное значение C-реактивного белка
4. Продолжительность артрита: 1 балл за симптомы, длящиеся шесть недель и больше
Новые критерии содействуют росту понимания РА и улучшению его диагностики и лечения. В «новых» критериях серология и аутоиммунная диагностика играют основную роль, поскольку обнаружение ACPA полезно в диагностике болезни на ранней стадии до возникновения повреждения суставов. Разрушение суставов, наблюдаемое на рентгенографических изображениях, было основной точкой критериев Американской коллегии ревматологии от 1987 г.[54] Данный критерий более не считается актуальным, так представляет собой всего лишь тип повреждения, на избегание которого нацелено лечение.
В клинической практике применяются следующие критерии:
- Два и более опухших сустава
- Утренняя скованность, длящаяся более часа как минимум шесть недель
- Обнаружение ревматоидных факторов или антител против ACPA, таких как антитела к мутирующему цитруллинированному виментину, может подтвердить подозрение на РА. Отрицательный результат анализа на антитела не исключает диагноз РА.
Дифференциальный диагноз
Несколько других медицинских состояний могут напоминать РА, которые требуется отличать от РА во время диагностики:[55][56]
- Микрокристаллический артрит (подагра и псевдоподагра) – обычно охватывает определенные суставы (колено, MTP1, пятки) и может быть отличен за счет аспирации суставной жидкости при наличии сомнений. Покраснение, ассиметричное распределение затронутых суставов, боль наблюдаются ночью, а первоначальная боль при подагре длится менее часа.
- Остеоартрит – можно отличить с помощью рентгенограммы затронутых суставов и анализов крови, возраста (более пожилые люди), первоначальная боль длится менее часа, ассиметричное распределение затронутых суставов и ухудшение боли при длительной нагрузке на суставы.
- Системная красная волчанка (СКВ) – можно отличить с помощью специфических клинических симптомов и анализов крови (антитела против двухцепочечной ДНК)
- Один из тяжелых типов псориатического артрита, напоминающий РА – изменения ногтей и кожные симптомы различаются
- Болезнь Лайма вызывает эрозивный артрит и может иметь тесное сходство с РА – можно отличить посредством анализа крови эндемических областей
- Реактивный артрит (ранее болезнь Рейтера) – ассиметрично охватывает пятки, крестцово-подвздошные суставы и крупные суставы ног. Обычно связывается с уретритом, конъюнктивитом, иритом, безболезненными ротовым язвами и кератодермальной гонореей.
- Анкилозирующий спондилоартрит – охватывает позвоночник, хотя в контексте данного заболевания может возникать напоминающий РА симметричный полиартрит мелких суставов.
- Гепатит C – в контексте данного заболевания может возникать напоминающий РА симметричный полиартрит мелких суставов. Гепатит C также может вызывать аутоантитела к ревматоидному фактору
Более редкие причины, которые действуют различно, но могут вызвать боль в суставах:[55]
- Саркоидоз, амилоидоз и синдром Уипла также напоминают РА.
- Гемохроматоз может вызывать артрит суставов рук.
- Острая ревматическая лихорадка может быть отличена от РА посредством паттерна миграции вовлечения суставов и наличия предшествующей заболеванию стрептококковой инфекции. Бактериальный артрит (такой как вызванный стрептококком) обычно ассиметричен, в то время как РА обычно охватывает обе стороны организма симметрично.
- Гонококковый артрит (другой бактериальный артрит), также в первую очередь мигрирующий, может охватывать связки вокруг запястий и голеностопных суставов.
Контроль прогрессирования
Существует несколько доступных инструментов для контроля за ремиссией ревматоидного артрита. Индекс активности болезни в отношении28 суставов (DAS28) широко используется в качестве индикатора активности РА и реакции на лечение, но не всегда является надежным индикатором эффекта лечения.[57] Суставы, входящие в состав DAS28, включают (билатерально): проксимальные межфаланговые суставы (10 суставов), пястно-фаланговые суставы (10), запястья (2), локти (2), плечевые суставы (2) и колени (2). Что касается данных суставов, учитывается количество суставов со скованностью вследствие касания (TEN28) и опуханием (SW28). Кроме того, измеряется скорость оседания эритроцитов (СОЭ). Также страдающие заболеванием люди выполняют субъективную оценку (SA) активности болезни в течение предшествующих 7 дней по шкале от 0 до 100, где 0 означает «отсутствие активности», а 100 – «максимально возможная активность». На основе данных показателей DAS28 рассчитывается как:[58] Одно значительное ограничение в использовании шкалы DAS28 в клинических условиях заключается в том, что может быть упущен слабый синовит. Другие инструменты контроля за ремиссией ревматоидного артрита включают: Предварительное определение ремиссии ревматоидного артрита Американской коллегии ревматологии и Европейской антиревматической лиги, упрощенный индекс активности болезни (SDAI) и клинический индекс активности болезни (CDAI).[59]
Профилактика
Не известно способов профилактики заболевания помимо снижения воздействия факторов риска.[60]
Управление
Лечения РА не существует, но методы лечения могут облегчать симптомы и замедлять развитие болезни. Модифицирующее заболевание лечение демонстрирует лучшие результаты, когда начинается рано и агрессивно.[61] Цели лечения заключаются в минимизации симптомов, таких как боль и опухание, предотвращении деформации кости (к примеру, костные эрозии, видимые на рентгенограмме) и в поддержании ежедневного функционирования.[62] Это в большинстве случав достигается с использованием двух основных классов лекарственных препаратов: обезболивающих, таких как НПВС, и модифицирующих заболевание противоревматических препаратов (DMARD).[63] РА в целом подвергается лечению с помощью по меньшей мере одного противоревматического препарата.[61] Использование бензодиазепинов (таких как диазепам) для лечения боли не рекомендуется, поскольку они не помогают и связываются с риском.[64] Обезболивающие средства, помимо НПВС, предлагают меньшее, но в некоторой степени полезное действие в отношении боли, но вызывают аналогичный уровень желудочно-кишечного раздражения.[8]
Образ жизни
 Регулярная физическая нагрузка рекомендуется как безопасное и полезное средство поддержания мышечной силы и общей физической функции.[65] Не ясно, обладают ли действием специфические меры в отношении питания.[66] Физическая активность полезна для людей с ревматоидным артритом, имеющих жалобы на утомляемость.[67] Трудовая терапия играет положительную роль в улучшении функциональной способности людей с ревматоидным артритом.[68]
Регулярная физическая нагрузка рекомендуется как безопасное и полезное средство поддержания мышечной силы и общей физической функции.[65] Не ясно, обладают ли действием специфические меры в отношении питания.[66] Физическая активность полезна для людей с ревматоидным артритом, имеющих жалобы на утомляемость.[67] Трудовая терапия играет положительную роль в улучшении функциональной способности людей с ревматоидным артритом.[68]
Модифицирующие заболевание агенты
Модифицирующие заболевание противоревматические препараты (DMARD) представляют собой первоочередное лечение РА.[8] Они являются семейством различных препаратов с разбивкой по использованию и действию. Они облегчают симптомы, снижают повреждение сустава, а также улучшают общие функциональные способности.[8] Прием DMARD следует начинать на ранней стадии заболевания, поскольку они вызывают ремиссию заболевания примерно у половины людей и в целом улучшают результаты.[69] Под DMARD понимаются следующие препараты: метотрексат, гидроксихлорохин, сульфасалазин, лефлуномид, ингибиторы ФНО-альфа, абатацепт и анакинра. Ритуксимаб и тоцилизумаб представляют собой моноклональные антитела, но также являются DMARD. Наиболее широко используемым агентом является метотрексат, другие часто используемые агенты включают сульфасалазин и лефлуномид. Натрий ауротиомалат (золото) и циклоспорин используются реже в связи с более распространенными побочными действиями. Агенты могут применяться в сочетании.[8] Метотрексат является наиболее важным и эффективным DMARD и, как правило, представляет собой первоочередное лечение.[62][63][70] Побочные действия должны регулярно контролироваться в связи с токсичностью, включая желудочно-кишечную, гематологическую, легочную и печеночную.[70] Такие побочные действия как тошнота, рвота и боль в животе могут быть снижены приемом фолиевой кислоты.[71] Наиболее распространенный нежелательный эффект заключается в повышении уровня ферментов печени примерно у 15% людей.[70] Таким образом, для тех, кто постоянно демонстрирует отклоняющиеся от нормы уровни ферментов печени, либо имеют историю заболеваний печени, а также потребления алкоголя, рекомендуется биопсия печени.[72] Биологические агенты, как правило, следует использовать только в том случае, если метотрексат и другие традиционные агенты неэффективны после трехмесячного курса лечения.[73] Данные агенты, применяющиеся для лечения ревматоидного артрита, включают: блокаторы фактора некроза опухолей альфа (ФНОα),[8] такие как инфликсимаб; блокаторы интерлейкина 1, такие как анакинра, моноклональные антитела против B-клеток, такие как ритуксимаб и тоцилизумаб,[74] блокаторы костимуляции T-клеток, такие как абатацепт, среди прочих. Они часто применяются в сочетании с метотрексатом или лефлуномидом.[8] У тех, кто хорошо подвергается контролю блокаторами ФНО, снижение дозы не влияет на общую функцию.[75] Люди должны быть обследованы на скрытый туберкулез до начала терапии любыми блокаторами ФНО во избежание реактивации.[1] Блокаторы ФНО и метотрексат обладают одинаковой эффективностью при использовании в отдельности и дают лучшие результаты при использовании в сочетании. Блокаторы ФНО обладают одинаковой с этанерцептом эффективностью, будучи наиболее безопасными.[76] Абатацепт эффективен при РА с улучшением у на 20% большего количества людей за счет лечения, при этом долгосрочные исследования в отношении безопасности не доступны.[77] Тем не менее, отсутствуют исследования в целях различения биологических препаратов, доступных для лечения РА.[78] Проблемы в отношении биологических препаратов включают их высокую стоимость и связь с инфекциями, включая туберкулез.[8]
Противовоспалительные агенты
НПВС облегчают боль и скованность у страдающих РА.[8] Как правило, они не обладают действием на людей с длительным течением болезни и, таким образом, более не считаются агентами первой линии.[8][79] НПВС следует использовать с предосторожностью у страдающих желудочно-кишечными, сердечно-сосудистыми или почечными проблемами.[80][81][82] Использование метотрексата одновременно с НПВС безопасно, если выполняется надлежащий контроль.[83] Ингибиторы ЦОГ-2, такие как целекоксиб, и НПВС в равной степени эффективны.[84] Они несут такой же желудочно-кишечный риск, как НПВС в сочетании с блокатором протонного насоса.[85] Пожилые люди обладают меньшей желудочно-кишечной непереносимостью целекоксиба, чем НПВС в отдельности.[86] Тем не менее, имеется повышенный риск инфаркта миокарда за счет ингибиторов ЦОГ-2.[84] Постоянный прием противоязвенных препаратов не рекомендуется и допускается только для тех, кто находится в группе повышенного риска возникновения желудочно-кишечных проблем.[87] Глюкокортикоиды могут использоваться в течение короткого времени при обострениях, во время ожидания, пока препараты замедленного действия дадут эффект.[8] Также эффективны инъекции глюкокортикоидов в сустав.[8] В то время как долговременное использование снижает повреждение суставов, оно также вызывает остеопороз и предрасположенность к инфекциям, вследствие чего не рекомендуется.[8]
Хирургическое вмешательство
На ранних стадиях заболевания может быть выполнена артроскопическая или открытая синовэктомия. Она состоит в удалении воспаленной синовиальной мембраны и предотвращении быстрого разрушения затронутых суставов. В тяжелой степени затронутые суставы могут потребовать операцию по замене сустава, например, замену коленного сустава.[8] После операции всегда необходима физиотерапия.
Альтернативная медицина
Национальный центр дополнительной и альтернативной медицины США сделал заключение, что «Как правило, отсутствуют достаточные научные доказательства в поддержку того, что какие-либо меры дополнительной медицины полезны при РА, также имеются сомнения относительно безопасности некоторых из них. Некоторые духовные и телесные практики, а также пищевые добавки могут помочь людям с РА управлять симптомами и, следовательно, они могут быть полезным дополнением к общепринятым методам лечения РА, но доказательств недостаточно, чтобы прийти к выводам.»[7] Системный обзор методов дополнительной и альтернативной медицины (за исключением рыбьего жира) обнаружил, что « Доступные свидетельства не поддерживают их текущее использование в управлении РА.».[6] Исследования, демонстрирующие полезное действие различных методов альтернативной медицины при РА, часто повержены систематической ошибке, связанной с предпочтительной публикацией положительных результатов исследования и в целом представляют собой свидетельства недостаточно высокого качества, такие как рандомизированные контролируемые исследования (RCT).[5] Кокрановский обзор 2005 г. утверждает, что лазерная терапия низкого уровня может быть испробована в отношении облегчения боли и утренней скованности, связанных с ревматоидным артритом, так как обладает меньшими побочными действиями.[88] Существуют некоторые свидетельства, что Тай Цзы улучшает объем движений сустава у людей с ревматоидным артритом.[89] Свидетельства относительно акупунктуры неубедительны,[90] при этом они эквивалентны имитируемой акупунктуре.[91]
Пищевые добавки
Американская коллегия ревматологии заявляет, что ни одно растительное средство, по заявлениям, полезное для здоровья, не поддерживается высококачественными доказательствами и, таким образом, она не рекомендует их использование.[92] Не существует научного доказательства, что растительные добавки, рекламируемые как «натуральные», безопаснее для использования, чем общепринятые лекарственные препараты, также как и химические. Растительные средства, хотя и маркированные как «натуральные», могут быть токсичными или фатальными при употреблении.[92] Некоторые свидетельства поддерживают применение омега-3 жирных кислот и гамма-линолевой кислоты при РА.[93] Полезное действие омега-3 умеренное, но стабильное,[94] хотя имеющиеся свидетельства не настолько сильны, чтобы определить добавки омега-3 полиненасыщенных жирных кислот (обнаружимы в рыбьем жире) в качестве эффективного лечения РА.[95] Гамма-линолевая кислота, которая может облегчать боль, снижать число болезненных суставов и скованность, в целом безопасна.[96] Нижеприведенные средства находятся в процессе исследования в отношении лечения РА, основываясь на предварительных многообещающих результатах (не рекомендуются для клинического использования): босвеллиевая кислота,[97] куркумин,[98] чертов коготь,[99][100] бересклет крылатый[101] и лоза бога грома (триптеригиум Вильфорда).[102] Национальный центр дополнительной и альтернативной медицины США отметил, что, «В частности, растение лоза бога грома (триптеригиум Вильфорда) может обладать серьезными побочными действиями.»[7] В связи с неверным представлением, что растительные добавки всегда безопасны, в некоторых случаях существуют сомнения в отношении сообщения об их использовании, которое может повысить риск побочной реакции.[5] Существуют противоречивые свидетельства относительно действия стимуляторов эритропоэза при лечении анемии у людей с ревматоидным артритом.[103]
Беременность
У более чем 75% людей с ревматоидным артритом наблюдается улучшение симптомов во время беременности, но может возникнуть ухудшение после разрешения беременности.[1] Метотрексат и лефлуномид являются тератогенными (вредоносны для плода) и не используются во время беременности. Женщинам в детородном возрасте рекомендуется использование средств контрацепции во избежание беременности и прекращение их использования, если планируется беременность.[62][70] Низкая доза преднизолона, гидроксихлорохина и сульфасалазина считается безопасной для беременных женщин с ревматоидным артритом.
Вакцины
Люди с РА находятся в группе повышенного риска инфекций и смертности, для снижения данного риска рекомендуется прохождение вакцинации.[104] Уничтожающую вакцинацию от гриппа следует проходить ежегодно.[105] Пневмококковая вакцинация должна проходиться дважды пациентами в возрасте до 65 лет и один раз в год пациентами старше 65 лет.[106] В заключение, ослабляющая жизненную активность вакцина против опоясывающего лишая должна приниматься один раз в год людьми старше 60 лет, но не рекомендуется для пациентов, принимающих блокаторы фактора некроза опухоли альфа.[107]
Прогноз
Течение болезни в значительной степени изменчиво. Некоторые люди демонстрируют кратковременные симптомы, но у большинства болезнь прогрессирует на протяжении жизни. Около 20%–30% имеют подкожные узелки (известные как ревматоидные узелки); они связываются с плохим прогнозом.
Прогностические факторы
Плохие прогностические факторы включают:
- Устойчивый синовит
- Раннее эрозивное заболевание
- Внесуставные обнаружения (включая подкожные ревматоидные узелки)
- Положительные результаты анализа на ревматоидный фактор в сыворотке
- Положительные результаты анализа на анти-CCP антитела в сыворотке
- Носительство HLA-DR4 аллелей «общего эпитопа»
- Семейная история РА
- Плохое функциональное состояние
- Социально-экономические факторы
- Повышенный острофазный ответ (скорость оседания эритроцитов [СОЭ], C-реактивный белок [CRP])
- Повышенная клиническая степень тяжести.
Смертность
РА сокращает продолжительность жизни людей повсеместно от трех до двенадцати лет.[108] Положительные отклики на лечение могут свидетельствовать о лучшем прогнозе. Исследование 2005 г. клиники Мейо отметило, что страдающие РА находятся в группе удвоенного риска сердечно-сосудистых заболеваний[109] независимо от других факторов риска, таких как сахарный диабет, алкогольная зависимость и повышенный уровень холестерина, кровяное давление и индекс массы тела. Механизм, посредством которого РА вызывает данный повышенный риск, остается неизвестным; наличие хронического воспаления предположительно является способствующим фактором.[110] Возможно, что использование новых методов терапии биологическими препаратами увеличивает продолжительность жизни людей с РА и снижает риск развития атеросклероза.[111] Это основано на когортных и реестровых исследованиях, но все же остается гипотетическим. До сих пор не ясно, улучшают ли биологические препараты васкулярную функцию при РА или нет. Наблюдалось повышение уровня общего холестерина и холестерина липопротеинов высокой плотности и отсутствие улучшений в отношении атерогенного индекса.[112]
Эпидемиология
От РА страдает примерно 0,5 и 1% взрослых в развитых странах, при этом у от 5 до 50 на 100000 людей каждый год впервые диагностируется заболевание.[8] В 2010 г. заболевание вызвало около 49000 летальных исходов по всему миру.[114] Развитие заболевания редко встречается в возрасте до 15 лет, с этого времени распространенность растет с возрастом до 80 лет. У женщин заболевание встречается от трех до пяти раз чаще, чем у мужчин.[1] Возраст, в котором заболевание наиболее часто развивается у женщин, - от 40 до 50 лет, у мужчин в некоторой степени позже.[115] РА представляет собой хроническое заболевание, и, хотя и редко, может возникать спонтанная ремиссия, естественное течение болезни представлено практически неизменным одним устойчивым симптомом, является усиливающимся и затухающим по интенсивности, а прогрессирующее ухудшение структуры суставов ведет к деформации и недееспособности.
История
 Первые упоминания артрита датируются по меньше мере 4500 г. до н.э. Текст, датированный 123 г. н.э., впервые описывает симптомы, достаточно сходные с РА. РА был обнаружен в останках скелетов коренных американцев, найденных в штате Теннесси.[116] В Старом свете заболевание было достаточно редким до XVII века.[117] Первое определенное описание ревматоидного артрита в современной медицине было сделано французским врачом доктором Августином Джакобом Ландре-Бове (1772–1840) в 1800 г. в прославленном госпитале Сальпетриер в Париже.[11] Само название «ревматоидный артрит» было придумано в 1859 г. британским ревматологом доктором Альфредом Барингом Гарродом.[118]
Аномалия была обнаружена в исследовании доколумбовых костей. Кости из Теннесси не демонстрируют признаков туберкулеза, даже несмотря на то, что он был преобладающим в то время на территории Америк.[119]
Картина Питера Поля Рубенса предположительно может описывать действие РА. На его поздних картинах руки демонстрируют, по мнению некоторых врачей, составляющую повышенной деформации с симптомами заболевания.[120][121] РА может быть изображен на некоторых картинах XVI века.[122] Тем не менее, он в основном обнаруживается на картинах исторических кругов, на которых в XVI и XVII веках руки рисовали, следуя определенным обычаям стиля, что наиболее выражено на картинах художников-маньеристов. Было обычным, например, изображение поднятой к верху руки Христа, в которой в наши дни усматривается деформированная поза. Данные обычаи могут с легкостью неверно интерпретироваться как изображение заболевания.
Также известно историческое лечение РА: покой, лед, зажатие и поднятие, яблочная диета, мускатный орех, некоторые легкие физические упражнения время от времени, крапива, пчелиный яд, медные браслеты, корень ревеня, удаление зубов, голодание, мед, витамины, инсулин, магниты и электрошоковая терапия (ECT).[123] Колонна Прозорба, устройство фильтрации крови (удаление иммуноглобулина G) было утверждено FDA в 1999 г. для лечения РА.[124] Тем не менее, ее использование было прекращено в конце 2006 г.[125]
Первые упоминания артрита датируются по меньше мере 4500 г. до н.э. Текст, датированный 123 г. н.э., впервые описывает симптомы, достаточно сходные с РА. РА был обнаружен в останках скелетов коренных американцев, найденных в штате Теннесси.[116] В Старом свете заболевание было достаточно редким до XVII века.[117] Первое определенное описание ревматоидного артрита в современной медицине было сделано французским врачом доктором Августином Джакобом Ландре-Бове (1772–1840) в 1800 г. в прославленном госпитале Сальпетриер в Париже.[11] Само название «ревматоидный артрит» было придумано в 1859 г. британским ревматологом доктором Альфредом Барингом Гарродом.[118]
Аномалия была обнаружена в исследовании доколумбовых костей. Кости из Теннесси не демонстрируют признаков туберкулеза, даже несмотря на то, что он был преобладающим в то время на территории Америк.[119]
Картина Питера Поля Рубенса предположительно может описывать действие РА. На его поздних картинах руки демонстрируют, по мнению некоторых врачей, составляющую повышенной деформации с симптомами заболевания.[120][121] РА может быть изображен на некоторых картинах XVI века.[122] Тем не менее, он в основном обнаруживается на картинах исторических кругов, на которых в XVI и XVII веках руки рисовали, следуя определенным обычаям стиля, что наиболее выражено на картинах художников-маньеристов. Было обычным, например, изображение поднятой к верху руки Христа, в которой в наши дни усматривается деформированная поза. Данные обычаи могут с легкостью неверно интерпретироваться как изображение заболевания.
Также известно историческое лечение РА: покой, лед, зажатие и поднятие, яблочная диета, мускатный орех, некоторые легкие физические упражнения время от времени, крапива, пчелиный яд, медные браслеты, корень ревеня, удаление зубов, голодание, мед, витамины, инсулин, магниты и электрошоковая терапия (ECT).[123] Колонна Прозорба, устройство фильтрации крови (удаление иммуноглобулина G) было утверждено FDA в 1999 г. для лечения РА.[124] Тем не менее, ее использование было прекращено в конце 2006 г.[125]
:Tags
Читать еще: Валин , Летрозол (Фемара) , Муира пуама , Панадол , Пиксантрон ,










